经水传播是钩端螺旋体病的主要传播途径,因此,及时有效地对钩体疫区内各种水体进行监测,对控制钩体的传播和流行有重要意义〔1〕。我们曾研制了问号钩端螺旋体检测基因芯片,该芯片可检测中国流行的所有18个血清群钩体代表株〔2〕。本研究应用该芯片检测水中问号钩端螺旋体(简称钩体),结果满意。现报告如下。
1 材料与方法 1.1 菌株致病性钩端螺旋体波摩那血清群波摩那血清型 Luo株、双曲钩端螺旋体(中国药品生物制品检定所钩端螺旋体实验室)。其他经水传播的对照病原微生物为大肠埃希菌 O157、霍乱菌、嗜水气单胞菌、沙门菌、空肠弯曲杆菌、副溶血性弧菌、甲型肝炎病毒、血吸虫等,均由本单位保存。
1.2 模板制备用含10%兔血清的切尔斯基培养基 (Korthof培养基)5 mL加0.1 mL菌种,28%培养12~15 d 〔5〕。取钩体培养液1.0 mL,12 000 r/m in离心5 m in,用灭菌磷酸盐缓冲液(PBS)洗涤1次,沉淀用0.5 mL灭菌去离子水重悬,-20℃保存备用。其他病原样本的模板制备根据各自研究的最佳程序进行。
1.3 芯片制备和靶序列的荧光素标记参照文献〔2〕。
1.4 水样本处理取南京市的自来水、长江水、稻田水、山间小溪水、城郊农村的池塘水、玄武湖水各100 mL,掺入培养的钩体,钩体浓度分别为5条/100 mL和10条/100 mL。各水样以滤膜法浓缩至1~2 mL,12 000 r/m in离心5 m in,沉淀用 20 μL水重悬,95℃煮20 m in。取8 μL作为常规PCR与不对称PCR反应模板,同时设阴、阳性对照。采自福建、江西省疫区20份可疑水标本各100 mL,同上处理。
1.5 芯片检测 1.5.1 芯片预处理将芯片置新鲜配制的0.6%(W/V) NaBH4溶液中,30 m in,0.2%十二烷基磺酸钠(SDS)1 m in×2次;ddH2O,1 m in×2次;吹干待杂交用。
1.5.2 杂交不对称PCR扩增的荧光靶序列2 μL,加含阳性内掺的杂交液3 μL,混匀后加入点样区,置杂交盒内密封,湿盒避光50℃水浴2 h。洗涤:A液﹝2×柠檬酸钠缓冲液(SSC),0.1% SDS]60℃ 5m in×2次;B液(0.1×SSC,0.1% SDS)5 m in×2次; C液(0.1×SSC)5 m in×1次;ddH2O 5m in×1次,吹干。
1.5.3 芯片检测结果判定用Scanarray 3000扫描仪进行结果检测,依据荧光的有无判定是否为问号钩端螺旋体,根据荧光的强弱估测钩体的含量。
1.6 钩端螺旋体的培养分离参照文献〔1〕。
2 结 果 2.1 常规PCR检测(图 1)钩体浓度为10条/100 mL的水单一482 bp的扩增产物,而钩体浓度为5条/100 mL的水样、双曲钩体及其他螺旋体、病原、空白对照均无任何DNA扩增条带。
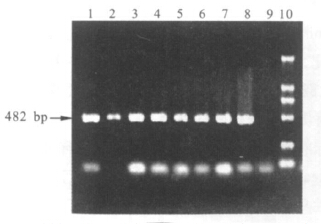 | 注:1~9为部分水样的阳性扩增结果;1~8钩体浓度均> 100条/100mL,9钩体浓度为10条/100 mL;10为DNA Marker。 图 1 部分水样PCR阳性扩增结果 |
钩体浓度分别为5条/100 mL和10条/100 mL的各水样,经常规PR、不对称PCR扩增,扩增产物和芯片杂交,均只在相应探针位置出现阳性信号,与对照、流行性出血热病毒、恙虫病东方体、大肠埃希菌O157、霍乱弧菌、疟疾疫原虫和血吸虫等杂交均为阴性。
 | 注:图中显示的荧光阳性信号为每100 mL含5 条钩体浓度的水样。 图 2 单一PCR扩增产物与芯片杂交结果 |
用芯片对自来水、长江水、稻田水、小溪水、家畜粪便污染的池塘水、玄武湖水、秦淮河水以及其他经水传播的病原微生物进行检测,结果未见任何阳性信号;对疫区20份可疑水标本进行检测,芯片检测结果阳性8份,PCR检测结果阳性5份,培养法检测结果阳性4份。
3 讨 论问号钩体的血清型复杂〔1〕,其生存的水源多变,不仅含有不同的水生生物和其他经水传播的病原,还有可能存在环境污染物,因此,目前对水中钩体的监测方法主要是培养法和 PCR法,PCR法的关键是引物的合理设计〔3〕。但是水环境中杂质的干扰和非特异性对PCR法检测结果影响较大,特别是问号钩端螺旋体与非致病性钩端螺旋体的抗原与基因序列高度同源,容易出现假阳性或假阴性〔3〕。
本研究应用芯片对水中不同浓度钩体检测,最低检测浓度为5条/100 mL,对疫区20份可疑水标本进行检测,阳性结果8份;用PCR检测,钩体最低检测浓度为10条/100 mL,20份可疑水标本仅5份阳性;通过液体培养分离,20份可疑水标本仅4份阳性。将荧光标记的PCR产物稀释10,20,50倍后,凝胶电泳未见条带,但与芯片杂交仍出现阳性信号,表明芯片检测的敏感性明显高于常规PCR法。
用芯片对钩体可能生存的不同生物与理化特性的水体 (非疫区)及嗜水气单胞菌、大肠埃希菌O157、霍乱等其他经水传播的病原进行检测,结果均为阴性,表明芯片的检测结果不受水中其他生物及化学物的干扰。进一步表明研制的芯片具有高度的特异性,对于在钩体病的疫源地调查与分子流行病学研究具有实用价值。
| 〔1〕 | 魏曦.钩端螺旋体病学[J].北京:人民卫生出版社,1982. |
| 〔2〕 | 唐雨德,陶开华,李越希,等.问号钩端螺旋体检测基因芯片的研制[J].中国人兽共患病,2004,20(4):311-314. |
| 〔3〕 | 唐雨德,周东明,陈永红,等.应用PCR技术检测致病性钩端螺旋体[J].中国公共卫生,2004,20(9):1042-1044. |
 2010, Vol. 26
2010, Vol. 26
