2. 遵义医学院珠海校区生理学教研室
糖尿病肾病(diabetic nephro pa thy,DN)是糖尿病最常见、最严重慢性并发症之一,由DN进展为肾功能衰竭和尿毒症是糖尿病病人死亡首要原因〔1〕。糖尿病早期肾脏肥大包括肾小球肥大和肾小管肥大。研究证实,肾小管肥大对整个肾脏肥大起至关重要作用,其中肾小管上皮细胞肥大是造成肾脏肥大主要因素〔2〕。大黄及大黄酸(rhein,4,5 dihydroxyan thraquinone-carboxy licacid)对DN有明显防治作用〔3, 4〕,但大黄酸对糖尿病肾近端小管上皮细胞影响目前尚不清楚。本研究通过观察大黄酸对高糖诱导大鼠肾近端小管上皮细胞肥大影响,进一步探讨大黄酸对糖尿病肾病的肾脏保护作用。
1 材料与方法 1.1 实验动物健康SD大鼠(南方医科大学实验动物中心),雄性,体重(250±20)g,30只。
1.2 主要试剂及仪器RPM I 1640培养基、Ⅱ型胶原酶(美国GIBCO公司);胎牛血清(FBS)(杭州四季青生物工程有限公司);大黄酸(南京替斯艾么中药技术研究所);3H-亮氨酸 (中国科学院上海应用物理研究所);考马斯亮兰蛋白测定试剂盒(南京建成生物工程公司);紫外分光光度计(日本岛津公司);流式细胞仪(美国Becton Dickinson公司)。
1.3 细胞培养参照文献〔5〕方法,大鼠麻醉,玻璃微分针手工分离近球肾小管。加入含10%胎牛血清的RPM I 1640培养液,置37℃、5% CO2孵育。实验分为对照组(10 mmol/LD-葡萄糖),高糖(HG)组(3 mm ol/LD-葡萄糖),高糖+大黄酸30,15,5 mg/L组。将原代肾小管上皮细胞接种于24孔板中,待细胞生长至80%~90%融合,换RPM I 1640(含 1% FBS)培养24 h,加高糖培养液(30 mmol/L),同时加入不同浓度大黄酸。
1.4 指标检测(1)细胞体积检测:培养72h后收集细胞。消化,上流式细胞仪检测,以前向角散射光强度表示细胞体积。(2)3H-亮氨酸掺入量检测:培养48 h后,每孔加入 3H-leucine (2.5μCi),72 h收集细胞,以NaOH (1mol/L)溶解细胞,HC1中和,液闪仪检测。实验设6个复孔。细胞计数,以计数率cpm/105细胞表示。(3)细胞蛋白质含量测定:以考马斯亮兰法测定蛋白含量,cpm/105细胞表示。
1.5 统计分析采用SPSS 13.0软件进行分析。2组间比较采用t检验,多组间比较采用F分析。检验水准α=0.05。
2 结 果 2.1 高糖诱导肾小管上皮细胞肥大与对照组比较,高糖组细胞体积增大,前向角散射光强度(122.84±2.93)明显右移,比对照组(116.80±2.94)增大(P < 0.01)。高糖细胞组3H-亮氨酸掺入量(16 225±1 476.1)增加,明显比对照组 (7 309±1 046.3) cpm/105细胞增高(P <0.01)。高糖细胞组细胞蛋白含量(4.43±0.38)增加,明显比对照组(3.41±0.21)增高(P < 0.01)。
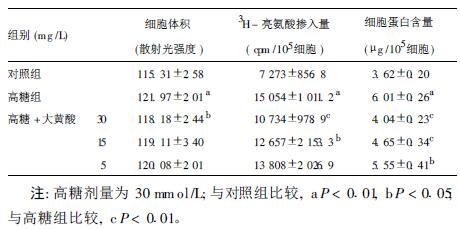
2.2 大黄酸对肾小管上皮细胞肥大影响(表 1)肾小管上皮细胞经大黄酸(30 mg/L)培养72 h后,细胞体积较高糖培养的细胞减小,而中、低剂量大黄酸组对高糖导致的细胞体积增大无明显作用。细胞3H-Leucine掺入量较高糖培养的细胞明显降低;细胞蛋白含量较高糖培养的细胞明显降低。
| 表 1 大黄酸对高糖诱导肾小管上皮细胞肥大影响(x±s, n= 6) |
糖尿病肾病是糖尿病特发性全身微血管病变的肾脏表现,是糖尿病最常见的并发症,也是糖尿病患者的主要死亡原因之一〔6〕。在病因学上高血糖是引起糖尿病肾病的主要原因。但是,高糖血症发展为糖尿病肾病的分子机制还不完全清楚〔7〕。研究证实,高糖可促使体外培养的系膜细胞出现自限性增殖,随即转为细胞肥大〔8〕。本次实验结果表明,高糖培养可导致肾小管上皮细胞肥大,并且呈现剂量依赖性〔9〕。大黄酸是从中药大黄蒽醌衍生物中分离出的一种单体成分。本实验结果表明,大黄酸可以抑制高糖诱导的肾小管上皮细胞肥大,并且呈现剂量依赖性,随着剂量增加,其抑制细胞肥大的作用亦相应增强。大黄酸治疗糖尿病肾病的机制可能与其纠正机体及细胞代射异常、降低TGF 1产生有关〔10〕。大黄酸是否通过抑制TGF 1表达及活性从而抑制高糖诱导的肾小管上皮细胞肥大,尚有待进一步研究。
| 〔1〕 | Zhou H, Tian HM, Long Y, et al. Mesenchymalstem cells transplantation mildlyam eliorates expermiental diabetic neph ropathy in rats[J].Chin Med J(Engl), 2009, 122(21):2573-2579. |
| 〔2〕 | 刘志红, 黎磊石.探索糖尿病肾病防治的新途径[J].肾脏病与透析肾移植杂志, 2002, 11(1):1-2. |
| 〔3〕 | 崔春黎, 马骏, 肖自力, 等.大黄对糖尿病肾病大鼠肾皮质基因表达谱的影响[J].中华肾脏病杂志, 2002, 18(4):285-290. |
| 〔4〕 | 龚传, 黎磊石, 孙骅, 等.大黄酸对糖尿病大鼠转化生长因子及其受体表达的影响[J].肾脏病与透析肾移植杂志, 2006, 15(2):101-111. |
| 〔5〕 | 刘红, 罗蕾, 高原.鼠肾近曲小管微分离技术[J].川北医学院学报, 2004, 19(2):10-12. |
| 〔6〕 | 丰罗菊, 于钧, 卢明俊, 等.糖尿病肾病病变程度影响因素及预测[J].中国公共卫生, 2006, 22(6):695-696. |
| 〔7〕 | 丰罗菊, 王亚龙, 张建陶, 等.糖尿病肾病空腹血糖预测值筛选[J].中国公共卫生, 2008, 24(6):727-729. |
| 〔8〕 | Mahimainathan L, Das F, Venkatesam B, et al. Mesang ial cell hypertrophy by high glucose is mediated by down-regulation of the tum or suppressor PTEN[J].Diabetes, 2006, 55(7):2115-2125. |
| 〔9〕 | 余德芊, 高原, 刘晓红, 等.高糖诱导大鼠近端肾小管上皮细胞肥大[J].遵义医学院学报, 2009, 32(1):13-16. |
| 〔10〕 | 郭啸华, 刘志红, 戴春笋, 等.大黄酸抑制TGFβ1诱导的肾小管上皮细胞肥大及细胞外基质产生[J]. 肾脏病与透析肾移植志, 2001, 10(2):101-105. |
 2010, Vol. 26
2010, Vol. 26

 , 刘晓红1
, 刘晓红1