志贺菌耐药主要通过2种方式获得:(1)通过基因水平转移方式;(2)通过药物自身诱导的垂直方式〔1〕。基因水平转移是指由质粒、转座子、整合子和基因岛等可移动遗传因子介导的在细菌种内和种间获得和传播耐药性的方式〔2〕。药物自身诱导获得耐药性是指细菌在抗生素压力环境中生存,可以通过某种遗传学机制的变化获得耐药性。本课题组曾通过次抑菌浓度连续传代获得了诱导耐多药菌株,并成功构建了抑制性消减杂交文库,初步筛选到诱导耐多药株的相关基因片段〔1〕。本研究在此基础上进一步比较敏感株和诱导耐多药株的差异基因序列,为确定志贺菌诱导耐多药的相关基因和变异方式以及探讨志贺菌耐多药机制提供科学依据。
1材料与方法 1.1材料 1.1.1菌株(1)志贺菌敏感菌株(敏感株Z23;分离自郑州市某医院);(2)志贺菌诱导耐多药株(诱导株YD):由Z23在头孢噻吩(CF)、诺氟沙星(NOR)、庆大霉素(GM)、磺胺甲基异恶唑(SM Z)等4种抗生素次抑菌浓度(1/2M IC)中传代诱导产生的耐多药株;(3)阳性对照菌株pMD18-T-X (分别含 YD菌株的Y16B3、Y16B8、Y16A11基因片段):由诱导耐多药抑制性消减杂交产物与pMD18-T载体连接并转化大肠埃希菌DH5A高效感受态细胞,克隆增殖,蓝白斑筛选阳性克隆而获得。后2种菌株均由本室筛选、构建和保存,参照文献〔1〕方法。
1.1.2药品与主要试剂氨苄青霉素(AM P)、琼脂糖凝胶 DNA回收试剂盒及普通质粒小提试剂盒、DNA M aker Ñ和 DNA Maker (北京天根试剂公司);限制性内切酶EcoRÑ和 Hind
(北京天根试剂公司);限制性内切酶EcoRÑ和 Hind 、PCR相关试剂、pMD19-T Vector (日本TaKaRa公司); DH 5A感受态细胞(郑州创生分子生物学研究所);引物由北京赛百盛生物公司合成。
、PCR相关试剂、pMD19-T Vector (日本TaKaRa公司); DH 5A感受态细胞(郑州创生分子生物学研究所);引物由北京赛百盛生物公司合成。
培养Z23、YD和阳性对照pMD18- T-Y16B3、pMD18-T-Y16B8、pMD18-T-Y16A11,采用煮沸法提取Z23和YD的基因组DNA,参照文献[3[;采用普通质粒小提试剂盒提取阳性对照菌株的质粒。
1.2.2 PCR扩增相关基因序列(1)引物设计:根据本室已经测得的基因序列Y16B3、Y16B8、Y16A11,利用Prim℃r 5.0软件设计引物;引物序列如下:Y16B3的引物序列:上游引物: 5c-ACG GCG AAG ATA CAG GAT TA-3c,下游引物:5c-AAC TGA CGC TGA AGT GAT GC-3c,退火温度:62℃;Y16B8的引物序列:上游引物:5c-CGC TGT CTG AGC AAC CAA-3c,下游引物:5c-GGC ATC CCG TAG TAA CGA AC-3c,退火温度:53℃;Y16A11的引物序列:上游引物:5c-TTC AGC GGT TTC CAG CAC-3c,下游引物:5c-GGT CAT TCA GGG AGA AGC AA- 3c,退火温度:51.3℃。(2) PCR反应:总反应体系25μL,10×PCR反应缓冲液2.5μL,dNTPs 100 Lm o l/L,上下游引物各 7 pm o,l模板DNA 2μL,Taq酶1.3U,加dd H 2O至25μL。反应条件:94℃预变性5 m in,94℃变性45 s,退火45 s,72℃延伸45 s,共进行35个循环,最后72℃延伸7 m in。取5μL产物1.5%琼脂糖凝胶电泳,015 Lg/mL溴化乙锭染色,紫外灯下观察结果并拍照。
1.2.3相关基因的克隆琼脂糖凝胶回收DNA试剂盒回收 PCR产物。(1)连接反应:pMD19-T载体1μL,回收PCR产物3μL,连接反应液5μL,加水1μL,至总体积为10μL,16℃过夜连接。(2)转化DH5A感受态细胞:转化试验按文献 〔4〕。氨苄青霉素抗性和蓝白斑筛选法来筛选阳性重组子。挑取白色菌落进行阳性克隆的鉴定。
1.2.4阳性克隆的鉴定挑取白色菌落接种于LB液体培养基中,37℃培养8 h。(1)菌落PCR鉴定:取2μL菌液为模板,反应体系同上,PCR反应条件:94℃预变性10 min,94℃变性1min,退火1min,72℃延伸1min,共进行35个循环,最后72℃延伸7min。15%琼脂糖凝胶电泳,0.5μLg/mL溴化乙锭染色,紫外灯下观察有无目的条带;(2)提取质粒、酶切鉴定:采用普通质粒小提试剂盒提取质粒。用pMD19-T载体上的酶切位点EcoRÑ和H ind 对质粒进行酶切鉴定。
对质粒进行酶切鉴定。
将阳性克隆菌液交由北京三博远志生物技术有限责任公司用pMD19-T载体通用引物完成测序。在序列相似性搜索工具Blast上对获得的基因片段分别进行核苷酸序列检索,分析其同源性。
2 结 果 2.1 相关基因片段PCR扩增结果(图 1)图 1可见,诱导株分别扩增到长度为320 bp的Y16B3、225 bp的Y16B8、310 bp的Y16A11基因DNA片段,敏感株未扩增出前2种产物,但扩增出554 bp的Y16A11基因DNA片段(诱导株310 bp的 DNA片段命名为Y16A11-Y,敏感株554 bp的DNA片段命名为Y16A11-Z)。
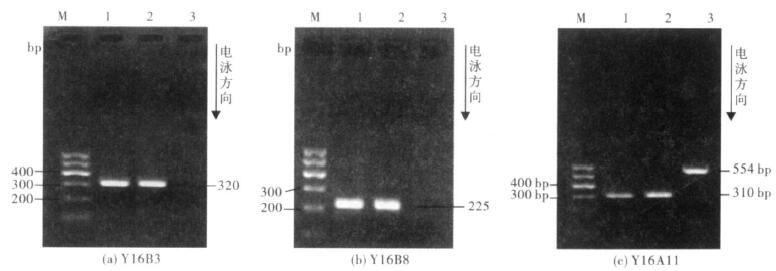 | 注: M: DNA M akerÑ ; 1: 阳性对照; 2: 诱导株; 3: 敏感株。 图 1 相关基因片段PCR 扩增结果 |
将从诱导株和敏感株扩增到的基因片段(Y16B3,Y16B8,Y16A11-Y,Y16A11-Z)分别克隆到载体质粒pMD19-T,转化大肠埃希菌DH5α,获得相应的阳性克隆菌株;对阳性克隆菌株进行菌液PCR扩增鉴定,扩增出的基因片段分别为320,225,310,554 bp,与预期结果一致。
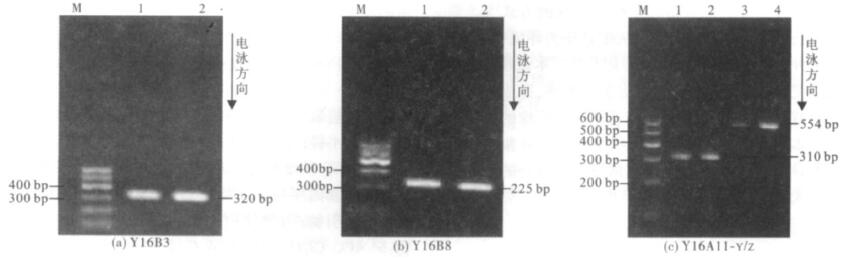 | 注: M: DNA MakerÑ ; 1: 诱导株; 2: 诱导株阳性克隆株; 3: 敏感株; 4: 敏感株阳性克隆株。 图 2 诱导株及其阳性克隆株PCR 扩增鉴定 |
含Y16B3、Y16B8、Y16A11- Y、Y16A11-Z片段的重组质粒经EcoRÑ单酶切,产物长度分别为3,2.9,3,3.2 kb左右,与预期结果一致;经EcoRÑ和Hind 双酶切产物长度分别为216和370,216和270,216和 360,2.6和600 bp左右,与预期结果一致。
双酶切产物长度分别为216和370,216和270,216和 360,2.6和600 bp左右,与预期结果一致。
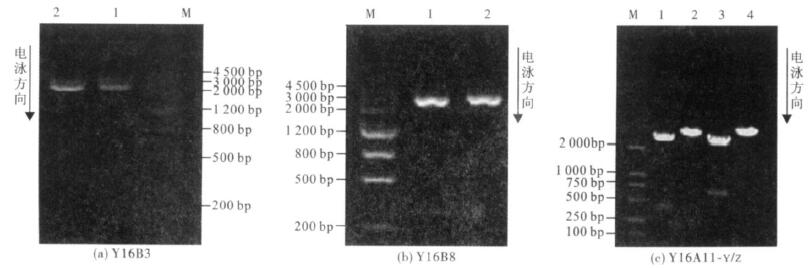 |
注: ( a, b)M: DNA M aker ; 1: 双酶切产物; 2: 单酶切产物; ( c)M: D2000; 1, 2: Y16A11-Y双、单酶切产物; 3, 4: Y16A11-Z双、单酶切产物。
图 3 重组质粒的酶切图谱 ; 1: 双酶切产物; 2: 单酶切产物; ( c)M: D2000; 1, 2: Y16A11-Y双、单酶切产物; 3, 4: Y16A11-Z双、单酶切产物。
图 3 重组质粒的酶切图谱
|
对获得的Y16B3,Y16B8,Y16A11-Y,Y16A11-Z等4个基因片段分别进行核苷酸序列测定。结果显示:(1) Y16B3基因片段的核苷酸序列长度为320 bp;B last检索结果表明,前113 bp基因序列与保守的假定蛋白同源性为99%,后218 bp基因序列与转座酶同源性为99%。(2) Y16B8基因片段的核苷酸序列长度为225 bp;Blast检索结果结果表明,其中前43 bp基因序列为可移动蛋白A的编码序列。(3) Y16A11-Y基因片段的核苷酸序列片段长度为310 bp;Blast检索结果表明,与可移动蛋白A的编码序列同源性为98%。(4) Y16A11-Z基因片段的核苷酸序列片段长度为 554 bp;B last检索结果表明,与脂肪酸代谢调节因子编码序列的同源性为96%~97%。Y16A11-Y和Y16A11-Z基因片段的核苷酸序列同源性极低。
3 讨 论
细菌的耐多药可能是通过多种耐药机制相继获得,这些耐药机制来源于2个方面:基因水平转移和染色体上的遗传变异〔5, 6〕。本实验中,耐药相关基因是自敏感株垂直诱导而获得,所以认为耐药相关基因的变化均源自于内在性耐药机制即染色体上的遗传变异。
细菌染色体上的遗传变异主要由2种机制产生:一种是突变,一种是遗传重组〔7〕。Girg is等〔8〕研究提示,抗生素耐药水平可以通过个别小的有效的染色体序列的突变累积而增加。突变引起的遗传改变是引起基因序列的改变,重组提供一个基因组结构的变化,均通过引起表型的变化,通过自然选择发挥作用。朱静媛等〔9〕研究证明,福氏志贺菌DNA旋转酶 gyrA基因盒拓扑异构酶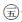 parC基因突变均与喹诺酮类药物耐药有关。本研究在诱导株中测出编码保守的假定蛋白、转座酶和可移动蛋白A的基因,在敏感株中测出编码脂肪酸代谢调节因子的基因,这与喹诺酮类药物耐药的基因突变不同,推测敏感株与诱导株相关基因序列测序结果的差异可能是由于基因重组造成的,但是其具体发生机制还需进一步研究。
parC基因突变均与喹诺酮类药物耐药有关。本研究在诱导株中测出编码保守的假定蛋白、转座酶和可移动蛋白A的基因,在敏感株中测出编码脂肪酸代谢调节因子的基因,这与喹诺酮类药物耐药的基因突变不同,推测敏感株与诱导株相关基因序列测序结果的差异可能是由于基因重组造成的,但是其具体发生机制还需进一步研究。
| 〔1〕 | 宋春花.志贺菌多重耐药的分子机制研究[D].郑州大学博士学位论文, 2007. |
| 〔2〕 | Rowe Magnus DA, Guerout AM, Mezel D.Bacterial resistan ceevolution by recruimtent of super-integron gene cassettes[J].Molecular Microbiology, 2002, 43(6):1657-1669. |
| 〔3〕 | 杨海燕.临床分离志贺菌属细菌多重耐药机制的研究[D].郑州大学硕士学位论文, 2003. |
| 〔4〕 | 张维铭.现代分子生物学实验手册[M].北京:科学出版社, 2003:399-400. |
| 〔5〕 | Llanes C, Neuwirth C, El Garch F, et al. Genetic analysis of amultiresistant strain of Pseudomonas aeruginosa producing PER-1 betalactamase[J].Clin Microbiol Infect, 2006, 12(3):270-278. |
| 〔6〕 | Liver more DM.Multiple mechanisms of antimicrobial resistance in Pseud omonas aeruginosa:our worst nigh mtare?[J].Clin Infect Dis, 2002, 34(5):634-640. |
| 〔7〕 | 张玉静.分子遗传学[M].北京:科学出版社, 2000:290-292. |
| 〔8〕 | Girgis H S, Hottes AK, Tavazoie S.Genetic arch itecture of intrinsic an tibiotic susceptibility[J].PLoS ONE, 2009, 4(5):e5629. |
| 〔9〕 | 朱静媛, 段广才, 范清堂, 耐喹诺酮类福氏志贺菌基因突变分析[J]. 中国公共卫生, 2004, 20(2):154-156. |
 2010, Vol. 26
2010, Vol. 26

 , 宋春花, 张卫东, 郗园林
, 宋春花, 张卫东, 郗园林