2. 青岛大学医学院附属青岛市海慈医院
目前,大肠癌在全世界范围内发病率位于恶性肿瘤的第 3位,并且以每年2%的速度上升。肌醇六磷酸(inos itol hexaphosphate,IP6)是植物体内重要的含磷化合物,可以抑制多种肿瘤细胞系的生长,具有广泛的抗肿瘤活性〔1, 2, 3, 4, 5, 6〕。本研究用不同浓度的IP6以不同时间作用于人结肠癌HT-29细胞,观察IP6对HT-29细胞凋亡的影响,从细胞、蛋白质、基因等水平探讨其抗癌机制。
1 材料与方法 1.1 试剂与仪器人结肠癌细胞系HT-29(北京协和医科大学细胞库);IP6(美国Sigma公司);DMEM/Ham F12培养基、 胎牛血清、胰蛋白酶(美国GIBCO公司);双标记流式细胞术 (Annexin V.F ITC/P I)双染试剂盒(中国晶美生物技术公司); Fura-2(美国Biotium公司);反转录试剂盒(美国Promega公司)。XDS-1B倒置显微镜(日本Olympus公司);JEM-1200EX 透射电镜、RF-540荧光分光光度计(日本JEOL公司);FACS Vantage流式细胞仪(美国BD公司);PCR仪(美国Biometra 公司)。
1.2 分组与处理将HT-29细胞用含有5%胎牛血清、100 U/mL青霉素和100μg/mL链霉素、DMEM/Ham F12培养基培养至对数生长期,收获细胞进行试验。IP6浓度分为0,1.8,和3.3 mmoL/L,作用时间分别为3 d,3,6个月,共9组。 每组3瓶细胞,浓度调整为1 ×106个/mL。
1.3 透射电镜观察收集细胞,2.5%戊二醛4℃固定4 h; 用磷酸盐缓冲液(PBS)漂洗细胞3次。1%锇酸4℃固定2 h,用PBS冲洗3次。乙醇梯度脱水。Epon812环氧树脂包埋,固化。超薄切片,醋酸双氧铀硝酸铅染色后透射电镜观察。
1.4 流式细胞术检测收集细胞,1 000 r/min离心5 min;用 100μL标记溶液重悬细胞,室温下避光孵育10 min;加入荧光溶液4℃孵育20 min;流式细胞仪激发光波长488 nm,515 nm检测F ITC荧光,560 nm检测P I。
1.5 Fura-2法测定Ca2+浓度收集细胞,调整细胞密度为 107个/mL;37℃预温10 min,细胞悬液中加入3μL Fura-2,终浓度为3μmol/L;洗涤细胞并调整密度为3 ×106个/mL。 参照Fura-2荧光法上机进行测定〔6〕。
1.6 半定量R-PCR检测按照Trizol试剂说明书提取 RNA。反应体系及反应条件参照试剂盒说明书;反转录产物 -20℃保存备用。Caspase 3 PCR扩增反应体系25μL:10 × buffer 2.5μL,MgCl2 2μL,dNTP 0.5μL,Taq酶0.2 μL,上下游引物各1.5μL,cDNA模板3μL。反应条件:94℃预变性5 min,94℃ 30 s,52℃ 1min,72℃ 1min,循环35次;72℃充分延伸7 min。4℃浸润。扩增产物片段长度400 bp;β-actin反应体系及反应条件与Caspase 3相同,扩增产物片段长度152 bp。扩增产物经15 g/L琼脂糖凝胶电泳,紫外透射仪下观察结果,通过天能凝胶图像分析软件读取目的电泳条带斑点密度扫描值,每个样本均检测3次。将目的基因条带与β-action 条带的比值作为目的基因表达相对量。
1.7 统计分析采用SPSS 11.5软件进行分析,多组比较采用单因素方差分析,两两比较采用t检验。
2 结 果 2.1 电镜观察HT-29细胞超微结构变化经IP6作用的HT2 29细胞出现凋亡现象,形态改变典型,染色体固缩,电子密度增高,细胞浆浓缩,细胞膜完成,表面微绒毛和伪足减少,可见凋亡小体,呈球形或月牙形,核膜消失、染色体断裂成碎片与细胞器等胞质成分聚集。
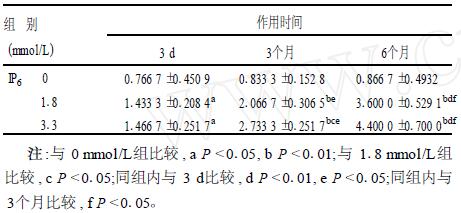
2.2 HT-29细胞凋亡率变化(表 1)| 表 1 IP6对HT-29细胞凋亡速率影响( %, x ±s, n = 3) |
结果表明,与各时间段内的0 mmol/L组比较,经IP6作用后,HT-29细胞凋亡率均升高 (P < 0.05);其中IP6作用6个月时间组与对照比较,差异有统计学意义(P < 0.01)。
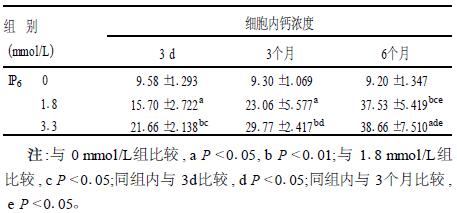
2.3 HT-29细胞胞内Ca2+浓度变化(表 2)| 表 2 IP6对HT-29细胞内钙浓度的影响(nmol/L, x ±s, n = 3) |
各IP6作用组 Ca2+浓度均升高(P < 0.05),其中IP6以3.3 mmol/L作用3 d,3,6个月后,Ca2+浓度随作用时间的延长而升高,差异有统计学意义(P < 0.05)。
2.4 HT-29细胞caspase-3m RNA表达变化(图 1)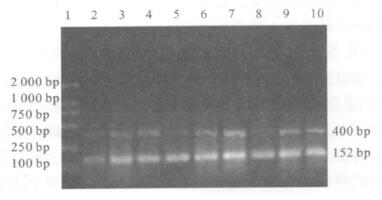
|
注: 1: DNA marker; 2: 0 mmol/L 3 d; 3: 1.8 mmol/L 3 d; 4: 3.3 mmol/L 3 d; 5: 0mmol/L 3个月; 6: 1.8 mmol/L 3个月; 7: 3.3 mmol/L 3个月; 8: 0 mmol/L 6 个月; 9: 1.8 mmol/L 6 个月; 10: 3.3 mmol/L 6个月。 图 1 IP6 对HT-29细胞Caspase-3 mRNA表达影响 |
与对照组比较,各IP6作用组caspase-3 mRNA表达均升高(P < 0105),其中,与3 d和3个月组比较,6个月组Caspase-3mRNA 表达升高(P < 0.01);IP6作用3 d和3个月的组间差异无统计学意义(P > 0.05)。
3 讨 论IP6对多种肿瘤细胞系具有良好抑制作用,包括恶性胶质瘤细胞系〔1〕、宫颈癌细胞系〔2〕、前列腺癌细胞系〔3, 4, 5〕和 HepG2肝癌细胞系〔6〕。研究表明,IP6以不同浓度(0~13.0 mmol/L)持续作用HT-29细胞2~6 d,对结肠癌细胞系生长具有浓度依赖性和时间依赖性抑制作用〔7, 8〕。细胞凋亡与肿瘤的发生、发展及退化密切相关。各种诱导因素作为细胞凋亡发生的第一信号系统,与细胞内受体结合,刺激细胞内第二信号系统,如Ca2+、cAMP等促进凋亡基因表达,引发第三信号系统即线粒体跨膜电位与线粒体通透性改变以及caspase 系统激活,最终导致细胞凋亡〔9〕。通过线粒体释放凋亡酶激活因子激活caspases是细胞凋亡信号传导的主要途径之一〔10, 11〕。
IP6对HT-29细胞凋亡的促进作用可能是通过调控细胞信号转导,调节相关凋亡基因表达来实现的。IP6及其次级磷酸化形式可以促进HT-29细胞内Ca2+浓度增高,从而引发钙超载介导的细胞凋亡活动,其中包括激活caspase家族非活化酶原,引起caspase-3级联放大效应,可能导致细胞内一系列蛋白底物裂解作用,促进HT-29细胞凋亡发生,发挥抗结肠癌的作用。
| 〔1〕 | Karmakar S,Banik NL,Ray SK.Molecularmechanism of inositol hexaphosphate-mediated apoptosis in human malignant glioblastoma T98G cells[J].Neurochem Res,2007,32(12):2094-2102. |
| 〔2〕 | Ferry S,MatsudaM,Yoshida H,et al.Inositol hexakisphosphate blockstumor cell growth by activating apoptotic machinery as well as by inhibiting the Akt/NFkappaB 2mediated cell survival pathway[J].Carcinogenesis,2002,23(12):2031-2041. |
| 〔3〕 | Singh RP,Agarwal C,Agarwal R.Inositol hexaphosphate inhibits growth,and induces G1 arrest and apop totic death of prostate carcinoma DU145 cells:modulation of CDKI-CDK-cyclin and pRb-related protein-E-F complexes[J].Carcinogenesis,2003,24(3):555-563. |
| 〔4〕 | Vucenik I,Shamsuddin AM.Protection against cancer by dietary IP6 and inositol[J].Nutr Cancer,2006,55(2):109-125. |
| 〔5〕 | Zi X,Singh RP,Agarwal R.Impairment of erbB1 receptor and fluid-phase endocytosis and associated m itogenic signaling by inositol hexaphosphate in human p rostate carcinoma DU145 cells[J].Carcinogenesis,2000,21(12):2225-2235. |
| 〔6〕 | Vucenik I,Tantivejkul K,Zhang ZS,et al.IP 6in treatment of liver cancer..IIP6 inhibits growth and reverses transformed phenotype in HepG-human liver cancer cell line[J].Anticancer Res,1998,18(6A):4083-4090. |
| 〔7〕 | 张铮,宋扬,兰克涛.植酸对大鼠结直肠癌形成的抑制作用与NK细胞变化关系的探讨[J].营养学报,2004,26(4):308-310,314. |
| 〔8〕 | 宋扬,张海平.肌醇六磷酸和膳食纤维对诱癌大鼠大肠癌发生的作用[J].营养学报,2005,27(2):135-137. |
| 〔9〕 | 戈全治,赵洪礼,董萍.Apoptin基因诱导A375细胞凋亡信号转导机制[J].中国公共卫生,2007,23(4):441-443. |
| 〔10〕 | Shamsuddin AM,Vucenik I,Cole KE.IP 6:a novel anti-canceragent[J].L ife Sci,1997,61(4):343-354. |
| 〔11〕 | El2Sherbiny YM,CoxMC,Ismail ZA,et al.G0/G1 arrest and Sphase inhibition of human cancer cell lines by inositol hexaphosphate(IP6)[J].Anticancer Res,2001,21(4A):2393-2403. |
 2010, Vol. 26
2010, Vol. 26