禽流感病毒H5N 1引起的高致病性禽流感,被列入国际生物武器公约动物传染病名单,是当今世界面临的健康威胁之一〔1, 2〕。目前以核酸扩增为基础的禽流感快速侦检技术主要针对病毒的血凝素(HA)、神经氨酸酶(NA)及基质蛋白M 的编码基因〔3〕。本研究以克隆H5N1禽流感病毒HA、NA、M 的全长基因序列,分别构建至PGEM-T Easy载体,进行体外转录,获得含目的基因序列的RNA转录体。此研究可为H5N1 致病机制、疫苗构建、基因组功能等研究提供基础依据,并为核酸快速检测方法的建立和改进提供阳性定量标准品。
1 材料与方法 1.1 材料(1)病毒、菌株和质粒:H5N1禽流感病毒培养液 (军事医学科学院五所微生物检验中心);大肠埃希菌XL 10 -Go ld株(美国Stratagene公司);线性化质粒载体pGEM-T easy (美国Prom ega公司)。(2)主要试剂:RNA提取试剂盒 (德国QIAGEN公司);Pyrobest Taq DNA聚合酶、Nde I内切酶及DNA连接酶、DNAM arker DL2000、DNA纯化及片段回收、抽提质粒、RNA转录纯化试剂盒(大连TaKaRa公司);Su-perScr ipt III One-Step实时PCR (RT-PCR)试剂盒(美国In-v itrogen公司);R iboprobe System-T7体外转录试剂盒(美国 Promega公司)。
1.2 方法 1.2.1 引物合成根据Genebank上H5N1的HA〔4〕、NA〔5〕、 M〔6〕基因序列,设计扩增全长基因的引物,由大连TakaRa公司合成。引物序列:(1) H 5N1-HA:HAp1 5´GGAGCGAAAG- CAGGGGTCCAATCTG 3´,HAp2 5´GGAGTAGAAACAAGGGT- GTTTTTAA 3´,扩增长度1 779 bp;(2) H5N1-NA:NAp1 5´ GGAGCAAAAGCAGGAGTTCAAAATG 3´,NAp1 5´GGAG- TAGAAACAAGGAGTTTTTTGA 3´,扩增长度1 398 bp;(3) H 5N1-M:M p1 5´GGAGCGAAAGCAGGTAGATGTTGAA 3´,M p2 5´GGAGTAGAAACAAGGTAGTTTTTTA 3´,扩增长度1 027 bp。
1.2.2 提取RNA和RT-PCR扩增采用Q IAGEN试剂盒提取病毒RNA,按照说明书进行操作。采用SuperScript III One-tep RT-PCR试剂盒,进行目的基因扩增。反应体系:2 ×混合反应液 25μL,酶混合物 2μL,RNA模板5 μL,上下游引物(50 pmol/L)各1μL,去离子水补足至 50μL。反应条件为:50℃反转录30 min;94℃预变性5 min;94℃变性30 s,54℃退火30 s,68℃延伸100 s,循环40次;最后68℃延伸5 min。
1.2.3 HA、NA、M基因连接与转化在T 4 DNA连接酶作用下,PCR产物分别与PGEM-T easy载体于20℃反应1 h 后,4℃连接过夜。用CaC l2法制备感受态细胞,将过夜连接产物转化至XL 10-Gold细胞中。
1.2.4 重组质粒筛选与鉴定使用蓝白斑试验筛选重组质粒,挑取白色菌落转接至含氨苄青霉素100 μg/mL的Luria- B ertan i (LB)培养液中,37℃,230 r/m in培养过夜,提取质粒 DNA。以质粒为模板,进行PCR扩增,检查插入片段的大小; 与目的片段大小相同,则判定为阳性,送交上海捷瑞生物公司进行双向测序。
1.2.5 测序结果比对利用DNAStar Laserg ene 7.1的 M ega lign软件对正反双向测序结果进行拼接和比对,然后用 C lusta lW软件,将测序结果与Genebank上的相应序列进行比对。
1.2.6 重组质粒载体线性化处理与浓度测定为了获得确定长度的含插入基因全长序列的转录产物,需将质粒进行线性化处理。质粒用Nde-I内切酶经37℃消化2 h。酶切产物用0. 8%琼脂糖凝胶电泳进行鉴定,观察线性化结果。
1.2.7 体外转录、模板RNA标准品的制备利用R iboprobe System-T 7试剂盒,体外转录获得模板RNA。室温下采用20 μL体系:磷酸盐缓冲液(5 ×)4 μL,二硫苏糖醇(DTT,100 mmol/L)2 μL,核酸酶抑制剂(RNasin,40 U)1 μL,核糖核苷三磷酸(rNTP,终浓度各为0.5 mmol/L)5 μL (0.3 μg/μL) 线性化质粒2 μL,T 7 RNA聚合酶(18 U)1 μL,去离子水5.5 μL。反应条件为37.0℃ 1 h。转录产物加1.5 μL脱氧核糖核酸酶(RQ 1 RNase-Free Dnase,1 U/μL),继续反应20 min 除去DNA模板后,使用RNA转录纯化试剂盒进行纯化并用核酸测定仪(NanoDrop ND 1000)测定含量。
1.2.8 RT-PCR法鉴定体外转录RNA产物将已测度浓度的体外转录RNA产物溶液浓度换算为拷贝/μL。拷贝数= 浓度×阿伏加德罗常数/(1个碱基对的平均分子质量×总长度),其中阿伏加德罗常数为6.02× 1023;用去离子水将其分别依次梯度稀释。取各稀释液作模板,进行RT-PCR,引物和扩增条件与前述步骤相同。
2 结果 2.1 HA、NA和M基因扩增与重组质粒PCR鉴定(图 1)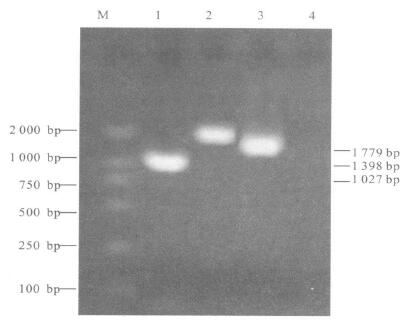
|
注: M: DNA 标准( DL 2000) ; 1: HA扩增产物; 2: NA扩增产物;3: M 扩增产物; 4: 空白对照。 图 1 1.0%琼脂糖凝胶检测结果 |
RT-PCR产物及重组阳性质粒的PCR扩增产物在1℃琼脂糖凝胶中电泳,HA、NA和M基因扩增片段大小与预期结果相符,分别约为1.7,1.3和1.1 kb。表明已成功获得全长目的片段,并被克隆到PGEM-T easy载体上。
2.2 测序结果比对登录Genbank,将插入片段测序结果进行比对。结果显示,克隆的HA、NA、M基因序列DNA序列与相应的DQ 997538、EU 263355、DQ 997537的同源性为100℃,证实了碱基序列的正确性,能够进入下一步的体外转录等试验。
2.3 cRNA标准品浓度测定体外转录的cRNA经核酸蛋白测定仪测定,HA、NA、M的质量浓度分别为503.9,379.2,437.8 ng/μL,D 260 nm/D 280 nm分别为1.98,1.87,2.06,符合纯度要求。根据拷贝数换算公式,将体外转录产物分别梯度稀释成5 × 1011~5 × 102拷贝/μL的标准品。
2.4 体外转录结果鉴定(图 2)
|
注:M:DNA标准(DL 2000);1:pGEM-T-HA质粒模板扩增产物;2:浓度5.0 × 105 copy/μL模板;3:浓度5.0 × 104 copy/μL模板;4:浓度5.0 × 103 copy/μL模板;5:浓度5.0 × 102 copy/μL模板;6:空白对照。 图 2 HA基因体外转录产物的RT-PCR琼脂糖凝胶检测结果 |
以HA、NA、M基因的体外转录RNA产物不同拷贝数的稀释液为模板,进行RT-PCR。 由HA基因体外转录产物结果可见,能扩增出1 027 bp条带,转录产物浓度为5.0 × 102拷贝/μL时,仍可见目的条带。 NA、M基因的体外转录鉴定结果与HA相同,均在浓度为5.0 × 102拷贝/μL时仍可见目的条带。
3 讨 论近年来,禽流感在世界范围内不断暴发,尤其是H 5N1亚型病毒引起的HPA I成为研究的热点〔7〕。HA裂解位点的碱性氨基酸数量及排列方式,在病毒入侵细胞及决定病毒致病力方面起着关键作用〔8〕;NA也是主要的病毒表面糖蛋白〔9〕; M基因片段编码M 1和M 2基质蛋白、是病毒的主要结构蛋白,免疫识别的重要表位〔10〕。因此,对H 5N1禽流感病毒的 HA、NA、M片段进行全长克隆,对其致病机制、疫苗研制开发、基因组功能等研究具有重要意义。
本研究构建了含有T 7启动子的HA、NA、M全长片段的重组质粒,经测序完全正确;直接用T 7 RNA聚合酶进行体外转录获得RNA片段,并准确定量,可作为H 5N1病毒的核酸扩增快速侦检技术方法的阳性对照。无生物安全隐患,同时也避免了以往研制的商品化试剂盒中质粒标准品不能很好的对样品处理及逆转录过程进行有效控制的问题。获得的 HA、NA、M基因的RNA转录产物,质量浓度分别为503.9,379.2,437.8 ng/μL。经连续倍比稀释,含量换算成拷贝数为 5.0 × 102~5.0 × 1011拷贝/μL,进行RT- PCR扩增,均出现目的条带。
本研究为进一步进行H 5N1型禽流感病毒的功能、疫苗等研究提供了基础依据,同时为后续建立和优化核酸快速检测的方法学研究提供了科学依据。
| 〔1〕 | 王天宇, 赵景波. 我国禽流感预防控制战略管理与实施[ J ]. 中国公共卫生, 2007, 23 ( 6) : 765 - 766. |
| 〔2〕 | Uyek i TM. Global ep idem iology of hum an in fect ion s w ith h igh ly pathogen ic avian in fluenza A ( H 5N1 ) viruses [ J] . Resp irology,2008, 43( 1) : 2 - 9. |
| 〔3〕 | M ackayWG, van Loon AM, N iedrig M, et a.l M olecu lar detection and typ ing of in flu enza viruses: A re w e ready for an in fluen za pan-dem ic? [ J] . J C lin V iro,l 2008, 42 ( 2) : 194 - 197. |
| 〔4〕 | 美国国家生物信息中心基因库( NCB I G enB ank) [ EB ] . 登录号: DQ 997538. |
| 〔5〕 | 美国国家生物信息中心基因库( NCB I G enB ank) [ EB ] . 登录号: EU 263355. |
| 〔6〕 | 美国国家生物信息中心基因库( NCB I G enB ank) [ EB ] . 登录号: DQ 997537. |
| 〔7〕 | 甄世祺, 王民生, 鲍昌俊, 等. 人感染致病性禽流感应急演练存在问题与对策[ J]. 中国公共卫生, 2007, 23( 11 ) : 1386- 1387. |
| 〔8〕 | WunderliW. From d iagnosis to the detection of avian in fluenza vi-rus[ J] . TherUm sch, 2007, 64( 11) : 609 - 612. |
| 〔9〕 | Gyarmat iP, Con ze T, Zohari S, et a.l S im u ltaneous genotyp ing ofallh em agglut in in and neu ram in idase subtypes of av ian in fluenza v irusesby u se of padlock probes[ J]. J C l inM icrob io,l 2008, 46 ( 5) : 1747- 1751. |
| 〔10〕 | ImaiM, N inom iya A, M inekaw aH, et a.l Rap id d iagnos is ofH 5N1 a-vian influenza virus in fect ion by new ly developed inf luenza H 5 he-m agglutinin gene-specif ic loop-m ed iated isoth erm al am p lificat ionm ethod[ J] . J V iro lM ethod s, 2007, 141 ( 2) : 173 - 180. |
 2010, Vol. 26
2010, Vol. 26

