2. 江苏大学临床医学院
随着锂盐应用的增多,锂的生物学作用逐渐为人们所认 识。巨噬细胞是机体的重要防御细胞,在抗感染、抗肿瘤及免 疫调节中起重要作用,能通过多种途径介导肿瘤免疫,破坏和 清除肿瘤细胞,增强的生成活性氧和一氧化氮的能力[1]。近 年来研究结果表明,锂有神经营养和神经元保护作用,可拮抗 多种因素,锂盐对免疫细胞功能的增强作用。锂盐增强人自 然杀伤( NK )细胞活性,但对大鼠的NK 细胞及多形核白细胞 的吞噬作用却有抑制作用。为了解氯化锂( L iC l)对巨噬细胞 功能影响,本研究巨噬细胞加载不同浓度的氯化锂,观察L iC l 对巨噬细胞巨噬功能、产生NO,O-2及H2O2 能力的影响,为 锂盐的治疗机制提供实验依据。
1 材料与方法 1.1 主要材料F12 培养基( 美国Promega 公司); 脂多糖 ( LPS,上海西唐科技公司); 辣根过氧化物酶( 美国S igm a 公 司) ; 细胞色素C ( 美国Sigm a 公司); 二甲基亚砜( D im ethy l sulfox ide,DMSO); 四甲基偶氮噻唑蓝(MTT,南京卓尔生化技 术有限公司); 胎牛血清( feta l ca lf serum,FCS); Gr iess检测试 剂盒(美国Prom eg a公司); 酶标仪(美国B io-RAD公司); LiC l (上海中锂实业有限公司)。
1.2 实验动物分组昆明种小鼠(江苏大学动物中心) 80 只,体重20~ 22 g,雌雄各半,随机分为4个组,每组20 只。 其中3组每天给予L iC l 014,01 6,112 mg / ( kg· bw ) 连续灌胃 20 d,另1组不作处理为对照组。
1.3 小鼠腹腔巨噬细胞的获取[2]于实验前3 d给小鼠腹 腔注射3%硫乙醇酸钠2 mL。实验当天处死小鼠,用酒精消 毒腹部,剪开小鼠腹部皮肤,向腹腔内注射无菌磷酸盐缓冲液 ( PBS) 2 mL,轻揉小鼠腹部后,将液体吸出,再用PBS 冲洗2 次,进行细胞计数,分别用F12培养液及PBS 缓冲液调整细 胞浓度为1 × 106 /mL。
1.4 吞噬功能的中性红测定[3]取1 mL 1 × 106 /mL腹腔巨 噬细胞加入24孔板内,置37 ℃ 、5% CO2 条件下贴壁2 h,取 出弃上清,漂洗,再加入01 1% 中性红生理盐水液1 mL ,置 37 ℃ 、5% CO2 条件下培养20 m in,取出,弃上清漂洗,加入1 mL细胞溶解液(乙醇B乙醇/1:1),充分溶解后于540 nm 波长 处比色。抑制率(% ) = ( 1- 实验组的吸光度变化值/对照组 吸光度变化值) × 100%。
1.5 NO的诱生及测定[4]取1 mL 1 × 106 /mL小鼠腹腔巨 噬细胞加入24孔板内,置37 ℃ 、5% CO2 培养箱中贴壁2 h,弃上清,漂洗后再每孔加入1 mL F12,同时加入LPS 使其终 浓度为5 Lg /mL。置37 ℃ 、5% CO2 条件下培养24 h,取出上 清至试管内,向试管中加入1 mL 格里斯( Gre iss) 试剂( 011% N- a-萘基乙二胺,1% 磺胺,3% H3 PO4 ) ,显色10 m in,于450 nm 波长下进行比色。
1.6 H2O2 的测定取0.7mL 1 × 106 /mL 小鼠腹腔巨噬细 胞,加入0115mL( 1 m g /mL)辣根过氧化物酶,01 15 mL( 1 mg / mL)酚红液,011 mL( 10 m g /mL) 经血清调理后的酵母聚糖,于37 ℃ 水浴2 h 取出,置于冰浴中,经2 000 r /m in 离心10 m in,取上清加入PBS 2 mL,再加入4 m o l/L NaOH 40 LL,于 610 nm 波长下比色。
1.7 O- 2的测定取1 mL 1 × 106 /mL小鼠腹腔巨噬细胞,于 37 ℃ 保温5 m in,加入011 mL( 10 m g /mL)经调理后的酵母聚 糖,再加入细胞色素C使其终浓度为( 60 Lm o l/L)。于37 ℃ 水浴2 h取出,置于冰浴中,再于2 000 r /m in离心10 m in,取 上清加入PBS 1 mL,于550 nm 波长下比色。
1.8 统计分析采用Stata 710统计软件进行F 检验。
2 结 果 2.1 L iC l对小鼠腹腔灌洗液细胞数的影响在LiC l 01 4,01 6,112 mg /( kg· bw )连续灌胃染毒20 d后,细胞总数分别 为( 10. 4± 2. 4),( 10. 8 ± 3. 6) ,( 10. 6 ± 2. 3 ) × 106 /mL,与对 照组( 14. 2 ± 4. 2) × 106 /mL比较,差异有统计学意义( P < 0.05),组间差异无统计学意义(P > 0.05) 。
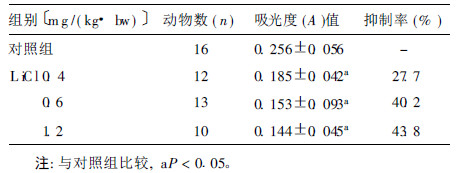
2.2 LiC l对小鼠腹腔巨噬细胞吞噬功能的影响(表 1)| 表 1 不同剂量LiC l对小鼠腹腔巨噬细胞吞 噬功能的影响(x± s ) |
表 1 可见,由于对小鼠腹腔注射,剂量过高、时间长等因素,导致部 分动物死亡。出现不同剂量L iC l对腹腔巨噬细胞的吞噬功 能有不同程度的影响,且随剂量增加,抑制率也逐渐增高,呈 剂量- 反应关系; 与对照组比较,差异有统计学意义( P < 0.05),组间差异也有统计学意义(P < 0.05) 。
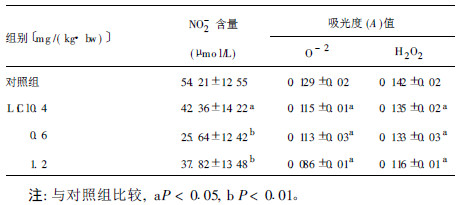
2.3 LiC l小鼠腹腔巨噬细胞NO生成的影响( 表 2)| 表 2 不同剂量L iC l对小鼠腹腔巨噬细胞产生NO、O-2 和H2O2 影响(x± s, n= 5) |
表 2可 见,3种不同L iC l染毒剂量,对巨噬细胞生成NO能力都产 生抑制,与对照组比较差异均有统计学意义( P < 0.05) ,剂量 组之间比较,差异有统计学意义( P < 0.01)。同时对巨噬细 胞产生O-2的能力产生抑制,与对照组比较差异有统计学意 义,且随剂量的增高,O-2产生逐渐下降( P < 0.05 )。11 2 mg /( kg· bw )对巨噬细胞产生的H2O2 出现明显抑制,与对照 组比较差异有统计学意义。而0.4,0.6 m g / ( kg· bw ) 组的 L iC l未见明显抑制,但随剂量的增高,H2O2 产生的量逐渐减 少( P < 0.01) 。
3 讨 论本实验结果表明,在3种剂量作用下,巨噬细胞的吞噬功 能均受到明显抑制。吞噬功能却呈剂量- 反应关系,表明在 本试验条件下吞噬功能损伤细胞数的减少。同时研究发现 L iC l在3种剂量下,LiC l均对小鼠腹腔巨噬细胞生成NO 能 力产生抑制作用。本实验L iCl对巨噬细胞产生NO 能力的影 响,可能直接抑制其在机体内发挥各种杀伤异物,体内活性氧 不断产生,也不断被体内抗氧化系统清除,保持动态平衡状态 [5, 6]。超氧阴离子自由基( O2- ) 是多种自由基的派生源,当 O2- 生成过多或清除不足时,O2- 及其衍生物就可以直接损伤 细胞。对小鼠腹腔巨噬细胞产生O-2的能力产生抑制。而在 112 mg /( kg· bw )时,巨噬细胞产生的过氧化氢( H2O2 )量也 明显受到抑制。结果表明,发现O-2下降速度快,即在低剂量 014 mg /( kg # bw ) 出现抑制作用,而H2O2 则在11 2 mg /( kg· bw )时观察到明显抑制。推测在较低剂量时,O-2产 生受到明显抑制,但由于其他一些还原剂如还原型细胞色素 C,还原型谷胱甘肽的存在,使已产生的O-2可转化为H2O2,因而H2O2 抑制不如O-2明显,而随单O-2进一步降低,同时 巨噬细胞还参与免疫、炎症反应的重要机制。随单核细胞发 育成巨噬细胞,其生成O-2的能力逐渐降低。因此,出现 H 2O2 产量降低,可能与LiC l剂量有关。但具体抑制机制有 待进一步研究。
| 〔1〕 | Stout RD,Jiang C,Matta B,et al. Macroph ages sequentially change their functional phenotype in response to changes in microenvironmental in fluences[J].Immunol, 2005,175(1):342-349. |
| 〔2〕 | 王以薇,曹永安,胡晓玲,等.神经生长因子对小鼠腹腔巨噬细胞神经胶质细胞释放一氧化氮的影响[J].中国药物与临床,2005,5(11):845-853. |
| 〔3〕 | 刘峰,姚咏明,董宁,等.高迁移率族蛋白B1对小鼠腹腔巨噬细胞免疫活性的影响[J].解放军医学杂志,2007,32(5):420-422. |
| 〔4〕 | 嵇扬,陆红.神经生长因子对小鼠腹腔巨噬细胞释放一氧化氮的影响[J].中国药房,2002,13(7):796-797. |
| 〔5〕 | Song M,Kellum JA,Kaldas H.Evidence that glutahtione depletion is a mechanism responsible for the anti-inflammatory effects of ethyl pyruvate in cultured lipopolysaccharide-stimulated RAW 264.7 cells[J].J Pharmacol Exp The,r2004,308:307-316. |
| 〔6〕 | Cai H,Harrison DG.Endothelial dys function in card iovascular diseases:the role of oxidant stress[J].Circ Res,2000,87:840-844. |
 2010, Vol. 26
2010, Vol. 26