2. 山西大学环境医学与毒理学研究所
内毒素(Endotoxin)是存在于革兰阴性细菌细胞壁外膜中的脂多糖(Lipopolysaccharide, LPS)成分, 在菌体分解时释放并发挥各种效应〔1〕。其性质比较稳定, 广泛存在于室内灰尘和室外细颗粒物等多种环境中。目前, 有关细菌内毒素的研究主要是从细胞和分子水平上阐述其造成肺部炎症以及急性肺损伤的机制〔2-3〕, 而内毒素对于动物不同脏器氧化损伤的毒理学研究报道较少。本研究观察内毒素腹腔注射染毒对小鼠肺、肝、心等组织器官的氧化损伤作用, 以了解内毒素对小鼠脏器的氧化损伤作用, 为内毒素的毒性机制研究提供科学依据。
1 材料与方法 1.1 主要仪器设备U-3010紫外分光光度计、F-4500荧光分光光度计(日本日立公司); 低温冷冻离心机(美国Sigma公司); 恒温水浴等。
1.2 试剂内毒素脂多糖(LPS)(血清型O55:B5), 无菌生理盐水配置, 4℃储存; 考马斯亮蓝G250、牛血清白蛋白、还原型谷胱甘肽(GSH)(美国Sigma公司)。1, 1, 3, 3-四乙氧基丙烷(1, 1, 3, 3-tctraethoxyp ropane, TEP); 硫代巴比妥酸(thiobar bituric acid, TBA); 磷酸盐缓冲液; 4%磺基水杨酸; 5, 5-二巯基-2, 2-二硝基苯甲酸(5, 5′-dithio-bis-nitro-benzoic acid, DTNB); 其他试剂盐酸、醋酸钠、醋酸、无水乙醇、磷酸等均为国产分析纯。
1.3 实验方法 1.3.1 动物分组及组织匀浆液制备动物为ICR纯系雄性小鼠, 7~8周龄, 体重18~23g (北京动物中心)。将24只小鼠随机分为4组, 每组6只小鼠, 1个生理盐水对照组和3个LPS染毒组[5, 10, 15mg/kg]。采用腹腔注射进行LPS染毒。小鼠于恒温条件下驯养1周, 期间动物自由进食和饮水。1周后对染毒组小鼠进行不同浓度LPS腹腔注射染毒, 对照组注射生理盐水。染毒结束后禁食6h脱颈处死, 立即取出其肺、肝、心组织, 在冰冷的生理盐水中洗净, 剪碎, 加入各组织10倍量的4℃预冷的生理盐水, 在0~4℃下制成匀浆液, 4℃ 14000r/min离心5min, 取上清液即得各脏器粗酶提取液。
1.3.2 各组织谷胱甘肽(GSH)含量测定谷胱甘肽含量测定采用文献〔4〕方法。根据测得的对应组织蛋白质含量计算出各组织中GSH含量(nmol/mg蛋白)。
1.3.3 各组织中脂质过氧化(LPO)水平测定以脂质过氧化产物-丙二醛(MDA)含量来表示细胞脂质过氧化水平〔5〕。采用硫代巴比妥酸荧光比色法〔6〕进行测定。
1.3.4 蛋白含量测定用考马斯亮蓝染色法测定蛋白含量〔7〕。
1.4 统计分析采用SPSS 12.0统计软件进行t检验。
2 结果 2.1 不同浓度LPS染毒对小鼠肺、肝、心中GSH含量影响(图 1)
|
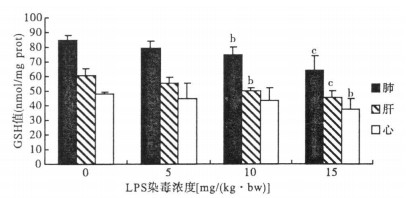
注:与对照组比较, a P < 0.05, b P < 0.01, c P < 0.001。 图 1 不同浓度LPS对小鼠肺、肝、心GSH含量影响 |
随着LPS染毒浓度的增加, 小鼠肺、肝和心脏中的GSH含量较对照组差异均依次降低, 并呈明显的剂量-反应关系(相关系数r分别为:肺-0.98, 肝-0.99, 心-0.97)。
由图 1可知, 当LPS染毒浓度为5mg/(kg·bw)时, 小鼠肺、肝和心脏中GSH含量较对照组差异均无统计学意义(P > 0.05)。当LPS染毒浓度为10mg/(kg·bw)时, 小鼠肺和肝脏中GSH含量明显降低, 与对照组比较差异有统计学意义(P < 0.01), 心脏中GSH含量与对照组比较差异无统计学意义(P > 0.05)。当LPS染毒浓度为15mg/(kg·bw)时, 小鼠肺、肝和心脏中GSH含量与对照组比较差异均有统计学意义(肺、肝为P < 0.001, 心为P < 0.01)。
2.2 不同浓度LPS染毒对小鼠肺、肝、心脂质过氧化(LPO)水平影响(图 2)
|
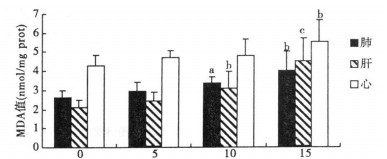
注:与对照组比较, a P < 0.05, b P < 0.01, c P < 0.001。 图 2 不同LPS浓度对小鼠肺、肝、心中LPO水平影响 |
随着LPS染毒浓度的增加, 小鼠肺和肝组织中MDA含量较对照组依次升高, 并呈明显的剂量-反应关系(相关系数r分别为:肺-0.99, 肝-0.95)。当LPS染毒浓度为5mg/(kg·bw)时, 小鼠肺和肝组织中的MDA含量与对照组比较差异无统计学意义(P>0.05);当LPS染毒浓度分别为10和15mg/(kg·bw)时, 小鼠肺和肝组织中MDA含量明显升高, 与对照组比较差异有统计学意义(肺为P < 0.05和P < 0.01, 肝为P < 0.01和P < 0.001)。
与肝和肺的情况相似, LPS不同染毒浓度均引起小鼠心脏中MDA含量增高, 但剂量-反应关系不明显。当LPS染毒浓度分别为5和10mg/(kg·bw)时, 小鼠心脏中MDA含量较对照组升高, 但差异无统计学意义(P > 0.05)。当LPS染毒浓度为15mg/(kg·bw)时, 小鼠心脏中MDA含量与对照组比较差异有统计学意义(P < 0.01)。
3 讨论本研究结果表明, 内毒素具有促进脂质过氧化、引起氧化损伤的作用。其机制可能是内毒素进入机体后, 诱导机体产生并释放大量的细胞因子、过氧化自由基以及其他活性氧自由基, 继而攻击生物膜使不饱和脂肪酸分子发生过氧化。由于不饱和脂肪酸是生物膜的重要组成成分, 所以脂质过氧化将导致细胞膜及其它膜系统结构和功能的破坏, 最终导致膜的变性和功能丧失, 并产生丙二醛(MDA)等一系列脂质过氧化产物。体内GSH能自行或经GSH-Px的还原, 消除自由基造成的损伤, 是细胞抵抗氧化损害的主要非酶性物质〔5〕。内毒素诱导产生的大量自由基会消耗GSH, 从而导致组织中GSH含量明显下降。
本研究结果表明, 内毒素可以导致小鼠肺、肝、心等脏器氧化损伤, 且损伤程度随LPS染毒浓度增加而加重。内毒素对小鼠肝、肺的氧化损伤较心脏更为严重。内毒素可引起多种器官组织损伤。其氧化损伤机制可能是通过产生活性氧自由基而造成器官组织的氧化损伤作用。
| [1] | 卢明芹, 许烂漫, 陈永平, 等. 内毒素耐受对D-GalN/LPS致大鼠肝损伤保护[J]. 中国公共卫生, 2008, 24(12) : 1493–1494. |
| [2] | 杜可军, 常文辉, 候立朝, 等. 环境内毒素相关新基因的克隆测序及生物信息学分析[J]. 环境与健康, 2006, 23(3) : 211–213. |
| [3] | 俞晓峰, 黄策. 细菌内毒素及其诱导的细胞因子在革兰氏阴性菌败血症休克中的作用[J]. 上海免疫学杂志, 1996, 16(3) : 190–192. |
| [4] | 孟紫强, 张波, 秦国华. 二氧化硫对小鼠不同组织器官的氧化损伤作用[J]. 环境科学学报, 2001, 21(6) : 768–773. |
| [5] | Wasoxicz W, Neve J, Pevetz A. Optimized steps in fluorometric determination of thiobarbituric acid-reactive substance in serum: importance of extraction pH and influence of samplep reservation and storage[J]. Clin Chem, 1993, 39(12) : 2522–2526. |
| [6] | 陈肖, 曾因明, 顾卫东, 等. 低温对内毒素性ARDS大鼠肺脂质过氧化的影响[J]. 徐州医学院学报, 2004, 24(4) : 292–294. |
| [7] | 孟紫强. 环境毒理学基础[M]. 北京: 高等教育出版社, 2003: 337-338. |
 2009, Vol. 25
2009, Vol. 25
