细胞内环境的稳定需要一整套复杂信号传导网络的严格调控, 使细胞增殖、生长阻滞、分化、衰老和凋亡在时间和空间上有序的进行.细胞周期关卡对于细胞增殖和凋亡的调控以及维护基因组的稳定性有重要意义; 关卡功能失调导致突变积累和染色体畸变从而可以引起多种疾病, 包括癌症〔1〕.研究提示, BaP与人类多种肿瘤的发生有密切关系〔2〕.为探讨低遗传损伤剂量苯并(a)芘(BaP)对人胚肺成纤维细胞(HE LF)细胞周期调控的影响, 为BaP致癌机制的研究提供新的线索, 本研究以正常HEL F为实验对象, 采取细胞同步化方法, 研究BaP对HEL F细胞周期调控的影响.
1 材料与方法 1.1 材料 1.1.1 细胞系HELF (中国医学科学院基础所细胞中心).
1.1.2 主要仪器与试剂FACS Calibur流式细胞仪(美国BD公司); I X70型倒置相差显微镜(日本Olympus公司).BaP (瑞士Fluck公司); Dulbecco’s modified Eagle medium (DMEM)、胰酶、辅酶Ⅱ(NADP)、6-磷酸葡萄糖(G-6-P)、二甲基亚砜(DMS O)、丙烯酰胺、N, N'-亚甲双丙烯酰胺(美国Sigma公司); 胎牛血清(FBS, 天津TBD公司); P53、P21、P16、细胞周期蛋白Cyclins (CyclinD、CyclinE、CyclinA和CyclinB)等抗体(美国B D公司); 增强化学发光法(ECL)试剂(美国SantaCruz公司).
1.2 方法 1.2.1 细胞培养HELF每2~3d传代1次, 实验细胞均为第10~15代细胞.
1.2.2 细胞同步化采取含0.5%灭活FBS的DMEM饥饿培养48 h及含10% FBS的DMEM再刺激培养的方法获得同步于不同时相的细胞群, 方法参照文献[2-3].
1.2.3 BaP染毒液配制及细胞处理BaP染毒前经大鼠肝匀浆上清(S9, 本实验室制备)代谢活化〔3〕, 经Ames实验证明具有代谢活化间接致癌物的能力.根据细胞同步化试验结果, 于血清刺激后10~12, 16~18, 22~24h进行BaP染毒处理, 设置溶剂对照组(与BaP高浓度组含等量的DMSO溶剂和0.25%S9代谢活化剂)及BaP低、中、高浓度组(浓度分别为2, 10, 50μmol/L), 处理2h后换液去除BaP, 继续培养12h, 收获HELF, 分析细胞周期分布情况和相关蛋白表达的改变.每组实验设3个平行样, 重复3次.
1.2.4 流式细胞术与蛋白印迹实验(Western Blotting)按照文献[3]方法, 收获HELF, 进行流式细胞术检测, 并采取蛋白印迹实验分析HELF细胞周期调控蛋白Cyclins (CyclinD、CyclinE、CyclinA和CyclinB)、P53、P21和P16表达的改变.
1.3 统计分析流式细胞图用DNAANALYSIS软件进行分析.
2 结果 2.1 细胞同步化对HELF细胞周期和蛋白表达影响(图 1)
|
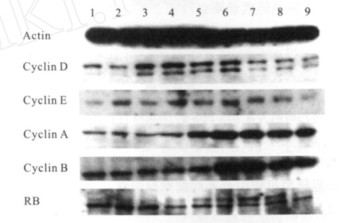
注: 1:含0.5% FBS的DMEM饥饿培养48h; 2~9:含10% FBS的DMEM再刺激培养1, 4, 8, 12, 18, 24, 30, 36 h。 图 1 细胞同步化过程中HELF细胞周期调控蛋白的表达 |
流式细胞术检测发现, 含0.5%FBS的DMEM饥饿培养HELF48h后, G0和或G1期细胞占总细胞群的百分比(G0/G1%)为96.04%, 而S期细胞比例(S%)为1.87%, G2和或M期的细胞比例(G2/M%)为2.08%.含10%FBS的DMEM继续培养后, 细胞较为同步地进入细胞周期, 血清再刺激后24h是细胞时相转换最重要的时间段.
图 1细胞同步化过程中HELF细胞周期调控蛋白的表达蛋白印迹试验发现, 4种重要的细胞周期蛋白CyclinD、CyclinE、CyclinA和CyclinB在血清饥饿后明显下降, 血清饥饿48h达到最低点, 血清再刺激后4种蛋白依次呈现出明显的时序性表达(CyclinD、CyclinE、CyclinA、CyclinB分别于再刺激后4, 4~8, 8, 12~18h开始出现表达增强), 24h后4种蛋白的表达均逐渐下降.
调节G1/S期转换的关键蛋白视网膜母细胞瘤(Rb)蛋白出现明显的下降, 保持低表达和去磷酸化状态, 在血清刺激后8~12h, RB蛋白表达量逐渐增加, 24~36h达到最高.而细胞周期蛋白激酶抑制剂(CKI) P21和P16蛋白在此过程中变化不大, 甚至有一过性的下降.
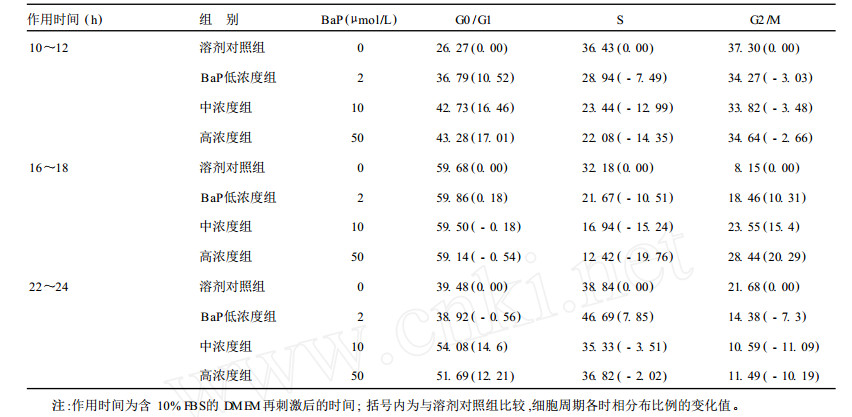
2.2 BaP对不同时相HELF细胞周期分布的影响(表 1)| 表 1 BaP对HELF细胞周期分布的影响(%) |
与溶剂对照组比较, 除血清刺激后22~24h用2μmol/LBaP染毒处理引起S期百分比较弱的增加效应, 其他时间、各BaP浓度作用下均出现明显的S期百分比下降的效应, 该效应随BaP浓度增加而明显; 针对G1和S期细胞作用10~12和16~18h组比针对G2期细胞作用的22~24h组明显.10~12和22~24h作用组引起G0/G1期细胞百分比增加, 16~18h作用组引起G2/M期细胞百分比增加.
2.3 BaP对不同时相HELF细胞周期调控蛋白表达的影响BaP对G1早期(10~12h) HELF作用, 引起细胞周期蛋白Cy-clinD表达的明显下降, 其他细胞周期蛋白CyclinE、CyclinA和CyclinB则变化不明显; 细胞周期调控蛋白P21出现表达增强, 而P53和P16则改变不甚明显.BaP对S期(16~18h) HELF作用, 引起P53和P21表达出现增强, 但未见明显的Cyclins表达改变.BaP对G2/M期(22~24h) HELF作用, 引起P53和P21表达出现增强, 也未见明显的Cyclins表达改变.
3 讨论既往研究表明, BaP对不同细胞的周期干扰效应不同, 不同的细胞模型可能引起不同的细胞阻滞结局, 并有不同的机制参与其调控过程〔4-7〕.未同步化的细胞群中, 处于G1期的细胞占绝大多数, 其对BaP作用后的细胞周期调控效应会掩盖其他时相(S、G2、M期)细胞的反应.本研究通过血清饥饿方法获得的同步化细胞, 能够较好地反映S期和G2/M期细胞的周期反应.血清再刺激后HELF再次进入细胞周期, 在24~36h后完成1次倍增, 而12h之前的大部分细胞未越过R点, 主要处于G1早期〔3〕.本实验发现, BaP于G1早期作用激起G1期关卡的响应; 于S期作用则引起G2期阻滞; 血清再刺激后22~24h为G2/M增长速度并达到高峰的时期, 覆盖了S晚期和G2/M期, G1期细胞在此阶段比例 < 20%, BaP作用后G1期细胞比例增加为下一周期G1期阻滞的结果.
本研究中, BaP针对G1早期细胞作用时, 细胞周期调控蛋白CyclinD出现明显下降, 说明CyclinD降解参与了BaP所致的G1阻滞机制.Reuven Agami等〔8〕发现, 电离辐射引起的G1/S期关卡的启动有2步独立的反应.首先是早期的、快速的、Cyclin D1降解介导的G1期的快速阻滞; 然后才是P53依赖的涉及多调控蛋白的G1期阻滞.本研究的结果与此相似, 证明Cyclin D1降解途经和P53-P21途径同时参与了BaP致HELF细胞G1期阻滞过程.P53蛋白是参与遗传损伤和细胞周期调控的重要分子之一.BaP代谢产物(7R, 8S)-二羟基-(9S, 10R)-环氧-7, 8, 9, 10-四氢苯并(a)芘(BPDE)与DNA形成的加合物能够引起多基因突变, 是BaP致癌的关键起始步骤〔9〕; 依赖P53的全基因组碱基切除修复机制参与BPDE-DNA加合物损伤的修复〔10〕; 继而转录激活下游p21、生长抑制和DNA损伤基因45(GADD45)等分子介导周期阻滞、启动细胞内损伤修复机制〔11〕.本研究发现, 该P53-P21途径参与了BaP致HELFG1和G2期关卡调控, 但P21下游的分子网络在BaP致周期阻滞中的响应模式, 有待进一步研究.
| [1] | 詹启敏. 细胞周期信号转导研究与信号转导治疗[J]. 医学研究通讯, 2004, 33(11) : 5–6. |
| [2] | 严丽萍, 陶茂萱. 苯并(a)芘对不同时相人胚肺成纤维细胞细胞周期的影响[J]. 环境与健康杂志, 2007, 24(5) : 287–290. |
| [3] | 严丽萍, 陶茂萱. Cyclins时序性表达与人胚肺成纤维细胞周期进程关系研究[J]. 中华预防医学杂志, 2009, 43(6) : 208–209. |
| [4] | Vaziri C, Fallcr DV. A benzo[a] pyrene-induced cell cycle checkpoint resulting in P53-independent G1 arrest in 3T3 fibroblasts[J]. J Biol Chem, 1997, 272(5) : 2762–2769. DOI:10.1074/jbc.272.5.2762 |
| [5] | 金明华, 石龙, 刘晓梅, 等. 苯并(a)芘对雄性小鼠睾丸细胞周期的影响[J]. 中国公共卫生, 2004, 20(2) : 153–154. |
| [6] | Drukteinis JS, Medrano T, Ablordeppey EA, et al. Bcnzo[a]pyrene, but not 2, 3, 7, 8-TCDD, induces G2/M cell cycle arrest, P21CIP1 and P53 phosphorylation in human choriocarcinoma JEG-3 cells: a distinct signaling pathway[J]. Placenta, 2005, 26(SuppI A) : S87–S95. |
| [7] | Guo N, Faller DV, Vaziri C. A novel DNA damage checkpoint involving post-transcriptional regulation of cyclin A expression[J]. J Biol Chem, 2000, 275(3) : 1715–1722. DOI:10.1074/jbc.275.3.1715 |
| [8] | Agami R, Bernards R. Distinct initiation and maintenance mechanisms cooperate to induce G1 gell cycle arrest in response to DNA damage[J]. CeU, 2000, 102 : 55–66. |
| [9] | Kaufmann WK, Paules RS. DNA damage and cell cycle checkpoints[J]. FASEB J, 1996, 10(2) : 238–247. |
| [10] | Lloyd DR, Hanawalt PC. P53-dependent global genomic repair of benzo[a] pyrene-7, 8-dio-9, 10-epoxide adducts in human cells[J]. Cancer Res, 2000, 60(3) : 517–521. |
| [11] | Hwang BJ, Ford JM, Hanawalt PC, et al. Expression of the p48 xeroderma pigmentosum gene is P53-dependent and is involved in global genomic repair[J]. Proc Natl Acad Sci USA, 1999, 96(2) : 424–428. DOI:10.1073/pnas.96.2.424 |
 2009, Vol. 25
2009, Vol. 25