金黄色葡萄球菌分型方法包括表型分型和基因分型2大类, 其中优化金黄色葡萄球菌细菌基因组重复序列PCR (REP -PCR)技术是一种比较新的细菌基因分型方法〔1〕, 与脉冲场凝胶电泳(PFGE)相比, 该法操作更简便, 无须特殊仪器试剂、成本低、扩增带不过于复杂, 分辨能力强, 更适合基层开展工作。REP-PCR反应体系和循环条件可能影响图谱清晰性, 故优化反应条件, 建立标准方法非常必要。本研究选择金黄色葡萄球菌标准株ATCC 25923为对象, 优化REP-PCR反应体系Mg2+浓度、模板量、引物浓度和退火温度, 建立了金黄色葡萄球菌REP-PCR指纹图谱分型方法, 并用该法对金黄色葡萄球菌临床分离株分型, 为构建金黄色葡萄球菌感染疾病的同源性追踪体系提供依据。
1 材料与方法 1.1 材料金黄色葡萄球菌标准株ATCC 25923, 金黄色葡萄球菌临床分离株(本室保藏)。REP引物〔2〕:REP1R-Ⅰ: 3′-CGGICTACIGCIGCIIII-5′; REP2-Ⅰ:5′-ICGICTTA TCIGGCCTAC-3′; 树脂型基因组DNA提取试剂盒(北京赛百盛基因技术有限公司); Taq DNA聚合酶、dNTPs、500 bp DNA Ladder (北京天根生化科技有限公司)。
1.2 方法 1.2.1 细菌基因组DNA提取与定量用树脂型基因组DNA提取试剂盒提取金黄色葡萄球菌标准菌株基因组DNA。为保证破壁充分, 先将收集的新鲜菌体用溶菌酶(20 mg/mL)于37℃处理60 min, 再用蛋白酶K (20 mg/mL)于50℃处理2 h。将提取的DNA用BioSpec-mini紫外可见分光光度计(SHIMADZU CORPORATION, 日本)定量DNA浓度。
1.2.2 PCR扩增反应体系及循环参数参照文献〔3〕初步确定反应体系各成分量:在25 μL反应体系中, 含MgCl2 2.0 mmol/L, dNTPs0.2 mmol/L, 引物REP1R-1和REP2-1各0.4 μmol/L, DNA模板100 ng, Taq DNA聚合酶2.5 U。按文献〔4〕初步设定循环参数:95℃, 4 min, 94℃ 1 min, 40℃ 1 min, 65℃ 3 min, 进行35个循环, 最后65℃延伸10 min。
1.3 条件优化试验在不同Mg2+浓度(0.5, 1.0, 1.5, 2.0, 2.5 mmol/L)下进行PCR检测, 其他条件一致; 在不同引物浓度(0.2, 0.4, 0.6, 0.8, 1.0 μmol/L)下进行PCR检测, 其他条件一致; 在不同的DNA模板量(25, 50, 75, 100, 125 ng/25 μL)下进行PCR检测, 其他条件一致; 在不同退火温度(38, 40, 42℃)下进行PCR检测, 其他条件一致。PCR扩增结果经10 g/L琼脂糖凝胶电泳后; 应用Touching1000B凝胶图像分析仪(上海天呈科技有限公司)观察DNA指纹图谱。
1.4 金黄色葡萄球菌临床分离株REP-PCR指纹图谱分析按1.2.1提取基因组DNA并测定其浓度。根据优化实验确定的反应体系和循环参数进行PCR
2 结果 2.1 Mg2+浓度的优化(图 1)
|
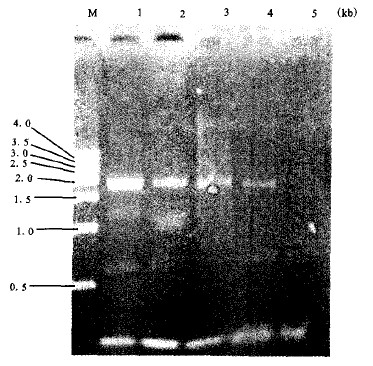
注:M: 500 bp DNA Ladder; 1~5:Mg2+浓度2.5, 2.0, 1.5, 1.0, 0.5 mmol/L。 图 1 REP-PCRMg2+浓度优化电泳图谱 |
图 1可见, Mg2+浓度为2.5 mmol/L时电泳图谱较为明亮, 包括长约2.0 kb和长度在0.5~1.0 kb之间的2条稳定条带, 且条带形态整齐, 故选择Mg2+浓度为2.5 mmol/L为反应最优条件。
2.2 模板量的优化(图 2)
|
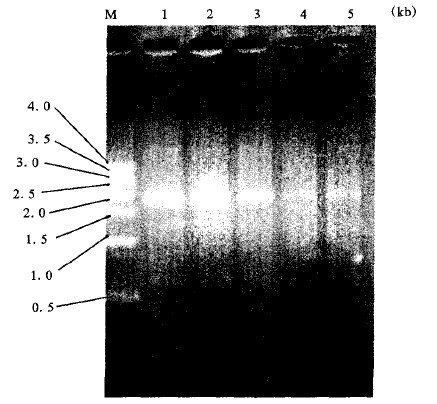
注:M:500 bp DNA Ladder;1-5:模板浓度125,100,75,5O,25 ng/25p~L。 图 2 REP-PCR模板浓度优化电泳图谱 |
图 2可见, DNA模板量为100、125 ng/25 μL时的电泳图谱均较为明亮, 包括长约2.0 kb和长度在0.5~1.0 kb之间的2条稳定条带。但DNA模板量为125 ng/25 μL时条带形态更整齐、明亮, 故选择DNA模板量为125 ng/25 μL为反应最优条件。
2.3 引物浓度的优化(图 3)
|
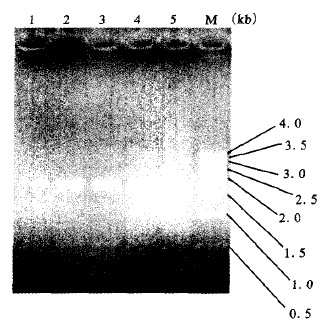
注:M:500 bp DNA Ladder;1-5:引物浓度0.2,0.4,0.6,0.8,1.0 μmol/L。 图 3 REP-PCR引物浓度优化电泳图谱 |
图 3可见, 引物浓度为0.6 μmol/L时的电泳图谱较为明亮, 且包括长约2.0 kb和长度在0.5~1.0 kb之间的2条稳定条带, 故选择0.6 μmol/L为最优引物浓度。
2.4 退火温度的优化设置38, 40和42℃3个退火温度。优化结果可见, 退火温度为40℃时电泳图谱条带清晰、明亮、整齐, 并包括长约2.0 kb和长度在0.5~1.0 kb之间的2条稳定条带, 故选择40℃为最优退火温度。
2.5 金黄色葡萄球菌临床分离株REP-PCR指纹图谱分析(图 4)
|
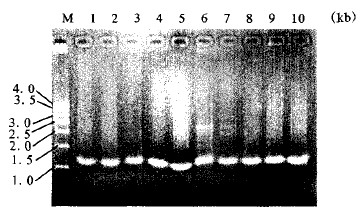
注:M:500 bp DNA Ladder;1~1O:临床分离株1~10。 图 4 金葡菌临床分离株DNA REP-PCR电泳图谱 |
图 4可见, 所有菌株均在0.5~1.0 kb之间出现1条长度相同条带; 其中1~3, 4, 5, 8, 9号菌株图谱完全相同; 7号和10号菌株图谱相同, 除在0.5~1.0 kb有1条条带外, 还在1.0~1.5 kb有1条条带, 在1.5~2.0 kb有1条条带; 6号菌株共产生5条条带, 分别为0.5~1.0 kb 2条, 1.0~1.5 kb 2条和1.5~2.0 kb 1条。
3 讨论重复DNA序列是20世纪90年代发现存在于原核生物基因组中的DNA片段, 主要为重复基因外回文序列(REP)和肠细菌重复基因基准序列(ERIC)。REP-PCR即以REP序列为引物, 对细菌基因组DNA进行PCR扩增, 可根据得到的电泳指纹图谱的差异, 对细菌进行分型或同源性检测。该法操作方便, 分辨效果好〔5〕。本研究以金黄色葡萄球菌标准株ATCC 25923为对象, 对REP-PCR反应体系Mg2+浓度、模板量、引物浓度和退火温度进行优化, 成功建立了金黄色葡萄球菌REP-PCR指纹图谱分型方法。结果表明, 在25 μL反应体系中, DNA模板量为125 ng, Mg2+浓度为2.5 mmol/L, REP1R、REP 2引物浓度分别为0.6 μmol/L, 退火温度为40℃时, 扩增产物的电泳图谱条带最清晰、明亮。其中Mg2+浓度与文献〔3〕相同, 退火温度与文献〔4〕一致, 模板量和引物浓度则与文献〔3〕有所不同。用本优化方法可将10株金葡菌临床分离株分为3型。与文献〔6〕比较, 使用另一种重复序列ERIC为引物的ERIC-PCR所得的指纹图谱与REP-PCR指纹图谱完全不同。前者扩增条带在0.25~2.5 kb之间, 可辨区带的数目为9~11条, 表明引物不同, 指纹图谱也不相同。本研究结果显示, 金黄色葡萄球菌标准株和临床分离株REP -PCR指纹图谱均在0.5~1.0 kb之间出现了1条长度相同条带, 该条带是否为金黄色葡萄球菌特征条带还需进一步研究。
| [1] | 孔秀凤, 祁伟. 金黄色葡萄球菌基因分型方法的研究进展[J]. 国外医药抗生素分册, 2008, 29(3) : 104–108. |
| [2] | 彭颖, 吕建新, 叶嗣颖, 等. 幽门螺杆菌临床分离株的REP-PCR分析[J]. 遗传, 2002, 24(6) : 684–686. |
| [3] | 朱林江, 郑飞云, 赵亚洲, 等. Rep-PCR应用于快速鉴定啤酒污染菌的研究[J]. 生物工程学报, 2006, 22(6) : 1013–1020. |
| [4] | 彭源东, 张忠泽, 丁鉴. 用Rep-PCRDNA指纹鉴别Frankia菌[J]. 微生物学杂志, 1998, 18(1) : 1–5. |
| [5] | 金莉莉, 董雪, 王秋雨, 等. 沈阳市副溶血弧菌重复序列PCR分型[J]. 中国公共卫生, 2008, 24(3) : 351–353. |
| [6] | 黄革, 董婷, 侯铁英, 等. 重复序列引物聚合酶链反应追踪金黄色葡萄球菌所致医院感染[J]. 中国感染与化疗杂志, 2006, 6(4) : 260–262. |
 2009, Vol. 25
2009, Vol. 25

