2. 大连医科大学组织人事部师资科;
3. 大连医科大学资产管理处
氧化应激是砷中毒的作用机制之一, 氧化应激的产物活性氧群(ROS)在砷所引起的各类细胞损伤中起主要作用〔1〕。ROS可能引起DNA、蛋白质和脂质的损伤, 并且可能与细胞内许多抗氧化系统功能的改变有关, 如影响体内重要的抗氧化酶和抗氧化物如超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽(GSH)及其相关酶类等〔2-3〕。抗坏血酸(VC)是经典的抗氧化剂, 能减轻或拮抗多种因素所致的氧化损伤, 其对砷中毒的保护作用也有报道〔4〕。本研究通过使小鼠摄入三氧化二砷(As2O3)并用VC拮抗后检测其肝脏中脂质过氧化物MDA含量、抗氧化酶SOD和抗氧化物GSH的含量, 探讨VC对砷毒性的抗氧化拮抗作用, 为砷中毒的有效防治提供基础依据。
1 材料与方法 1.1 主要试剂As2O3(美国Sigma公司); VC (沈阳新兴试剂厂); 考马斯亮兰(上海卓康生物科技有限公司); Nitritekit和MDA测定试剂盒(南京建成公司)。
1.2 实验动物与分组清洁级昆明种健康小鼠, 雌雄各半, 体重(20±2) mg。按体重将小鼠随机分为3组, 即对照组、染砷组(4 mg/L的As2O3)和VC拮抗组(4 mg/L的As2O3+45 mg/kgVC), 每组10只。
1.3 染毒方式与剂量对照组小鼠饮用自来水, 染砷组小鼠饮用含20 μmol/L As2O3的自来水, VC拮抗组饮用含20 μmol/LAs2O3的自来水, 同时灌胃给予45 mg/kg的VC。连续染砷60 d。
1.4 MDA含量、SOD活力和GSH含量测定按照试剂盒说明, 分别用硫代巴比以法测定MDA含量, 用亚硫酸盐试剂盒(Mitrite-kit)法检测SOD的活力, 用二硫双硝基苯酸(DTNB)法测定GSH含量, 用Bradford方法测定肝脏中蛋白含量, 计算每mg蛋白中MDA含量、SOD活力和GSH含量。
1.5 统计分析采用SPSS11.5软件进行分析, 组间均值比较采用单因素方差分析。
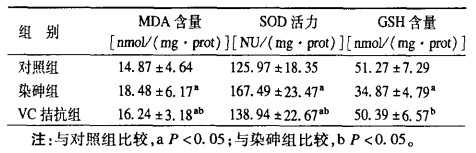
2 结果(表 1)| 表 1 VC对砷中毒小鼠肝脏中MDA、SOD和GSH的影响(x±s) |
20 μmol/L的As2O3单独作用于小鼠后, 肝脏中MDA的含量与对照组比较显著增高(P < 0.05);SOD活力和GSH含量则显著下降(P < 0.05)。而在VC灌胃的小鼠中, 肝脏MDA含量与单纯染砷组比较显著下降(P < 0.05), 但仍未达到正常水平; SOD活力和GSGH含量与单纯染砷组比较显著增高, 其中GSH含量已基本达到对照组水平。
3 讨论砷可引起机体的氧化应激〔5〕。MDA含量的多少可反应组织细胞的脂质过氧化速率或强度。本研究发现, VC可拮抗砷作用后引起的MDA含量降低, 表明VC可拮抗砷所引起的脂质过氧化。GSH是细胞内重要的抗氧化剂, 参与细胞的防御、解毒及损伤修复。GSH在对砷的解毒过程中发挥了主要作用〔6〕。本研究发现, 小鼠摄入高剂量As2O3后肝脏中GSH含量显著下降, 表明砷进入小鼠体内后可能产生各种自由基, 消耗了GSH, 而加入VC后, GSH含量增高, 表明VC可以拮抗砷对GSH的毒性, 提示VC可能通过保护抗氧化物GSH而增强清除自由基的能力。SOD可清除体内的超氧化物自由基, 在维持体内氧化和抗氧化系统平衡中发挥着重要的作用。本实验结果提示, 砷可降低小鼠肝脏中的SOD活力, 而VC则可拮抗砷的毒作用, 提示VC降低细胞氧化应激水平的另一可能机制, 即通过诱导抗氧化酶SOD的活性增加细胞的清除自由基的能力实现其抗氧化作用。
| [1] | Veyersmann D, Hartwig A. Carcinogenic metal compounds: recent insight into molecular and cellular mechanism[J]. Arch Toxicol, 2008, 82(8) : 493–512. DOI:10.1007/s00204-008-0313-y |
| [2] | Nandi D, Patra RC, Swarup D. Oxidative stress indices and p lasma biochemical parameter during oral exposure to arsenic in rats[J]. Food Chem Toxicol, 2006, 44(9) : 1579–1584. DOI:10.1016/j.fct.2006.04.013 |
| [3] | 蒋玲, 李玲, 吴君, 等. 氧化应激致慢性水砷暴露小鼠肝损伤作用[J]. 中国公共卫生, 2008, 24(5) : 593–595. |
| [4] | 朴丰源, 杨光, 李秋娟, 等. 牛黄酸和VC对染砷小鼠脑神经损伤保护作用[J]. 中国公共卫生, 2007, 23(12) : 1467–1469. |
| [5] | Haider SS, Najar MS. Arsenic induces oxidative stress, sphingolip i2 dosis, dep letes p roteins and some antioxidants in various regions of rat brain[J]. Kathmandu UnivMed J, 2008, 6(1) : 60–69. |
| [6] | Maiti S, Chatterjee AK. Effects on levels of glutathione and some re2 lated enzymes in tissues after an acute arsenic exposure in rats and their relationship to dietary p rotein deficiency[J]. Arch Toxicol, 2001, 75 : 531–537. DOI:10.1007/s002040100240 |
 2009, Vol. 25
2009, Vol. 25