乳酸杆菌(Lacotobacillus)是存在于人和动物体内的一种重要益生菌, 广泛应用于食品及医药领域中。另外, 乳酸杆菌也可以作为表达载体制成口服疫苗〔1-2〕。pEDM27/5质粒载体是大肠埃希菌和乳酸杆菌的穿梭载体, 该质粒携带LacZ基因及红霉素抗性基因, 可进行外源基因的克隆表达, 因此, 本研究选择pEDM27/5作为A组轮状病毒VP7基因表达载体, 将VP7基因导入pEDM27/5载体, 通过转基因工程导入乳酸杆菌, 并在乳酸杆菌中持续表达活性VP7蛋白, 为高效、安全的轮状病毒疫苗研制提供基础依据。
1 材料与方法 1.1 材料A组轮状病毒标准株(中国疾病预防控制中心病毒所); 嗜酸乳酸杆菌标准株(ATCC4356)、pEDM27/5质粒(德国MLC分子实验中心)。Trizol提取试剂盒(美国Invitro-gen公司); 逆转录聚合酶链反应(RT-PCR)扩增核心试剂盒(上海睿诚生物科技有限公司); 吸附柱式琼脂糖胶DNA回收试剂盒(上海闪晶生物科技公司); 质粒小量抽提试剂盒(上海闪晶生物科技有限公司)。电穿孔仪(美国Bio-Rad公司)。
1.2 A组轮状病毒培养与总RNA提取A组轮状病毒接种敏感细胞株MA-104细胞进行培养, 当病变细胞约达到70%~80%, 感染病毒的MA-104细胞有部分脱落, 界面模糊、间隙增大、细胞质内颗粒增多、溶解形成大小不一的空隙时收获细胞, 参照试剂盒说明书提取病毒总RNA。
1.3 重组质粒的制备A组轮状病毒VP7基因克隆并导入pEDM27/5载体, 转化大肠埃希菌, 抽提质粒进行PCR反应: 95 ℃, 15 min后, 以95 ℃ 30 s, 55 ℃ 45 s, 72 ℃ 60 s为一个循环, 循环30次, 产物电泳分析, 将回收、纯化产物导入pEDM27/5载体, 转化大肠埃希菌DH5α, 并抽提质粒, 蓝白斑筛选阳性质粒〔3〕。
1.4 基因序列分析选取实验阳性质粒送上海生物工程公司进行基因测序。
1.5 重组乳酸杆菌的电穿孔制备提取重组质粒pEDM27/ 5-VP7, 通过电穿孔转化乳酸杆菌〔4〕, 将乳酸杆菌均匀涂布牛肉膏蛋白胨琼脂培养基(MRS, 含有5 μg/mL红霉素)筛选阳性克隆菌落, 于37 ℃活化表达克隆, 并接种于MRS液体肉汤培养基扩增, 用乳糖进行诱导表达, 分别于4, 8, 12 h后取样, 冰上放置5 min, 4 ℃, 8000 r/min离心, 收集菌体。
1.6 vp7蛋白表达SDS-PAGE电泳分析收集菌体后取15 μL进行SDS-PAGE分析。
1.7 表达蛋白相对含量的薄层扫描仪测定用薄层扫描仪对经乳糖诱导4, 8, 12 h后电泳蛋白表达条带进行扫描分析。1.8重组表达蛋白的Western blot分析〔5〕将上述诱导菌液进行SDS-PAGE后转至硝酸纤维素(NC)膜上, 进行Western blot检测, Western-blot分析应用鼠抗vp7McAb及辣根过氧化物酶(HRP)标记羊抗鼠IgG抗体。
2 结果 2.1 A组轮状病毒VP7基因RT-PCR产物电泳A组轮状病毒经RT-PCR扩增后, 1 %琼脂糖电泳检测可见一条约1.0 kb的特异性条带, 与预期目的基因(VP7基因)大小相符。
2.2 质粒测序结果蓝白斑筛选阳性质粒送上海生物工程公司测序, 测得序列与Internet网GeneBank中获得A组轮状病毒VP7蛋白编码的基因序列进行比对其同源性高达99%, 结果表明本研究成功构建了A组轮状病毒VP7基因载体。
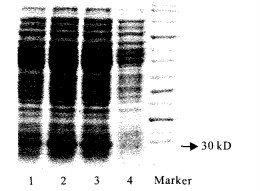
2.3 表达产物SDS-PAGE电泳结果(图 1)
|
注:1~3:诱导4, 8, 12h后; 4:标准乳酸杆菌; Marker:蛋白分子量标准。 图 1 表达产物的SDS-PAGE电泳 |
将重组质粒转入乳酸杆菌, 乳糖诱导后不同时间收获的菌体与乳酸杆菌标准株进行SDS-PAGE分析, 经过染色和脱色后发现诱导菌在约28 kD处有1粗条带, 而标准菌株在约28 kD处没有出现相同的条带, 表明VP7蛋白(分子量为28kD)已被成功地诱导表达。
2.4 表达蛋白相对含量的薄层扫描仪测定扫描分析显示:诱导4, 8, 12 h后表达目的蛋白分别约占菌体总蛋白的2.30%, 5.12%, 5.38%, 表明A组轮状病毒VP7蛋白得到了表达, 且表达量随着时间延长表达持续增加。
2.5表达产物的Western blotting鉴定(图 2)

|
注:1~3:诱导4,8,12h后;4:标准乳酸杆菌;Marker:蛋白分子量标准。 图 2 表达产物的Western blotting鉴定 |
应用鼠抗vp7 McAb及HRP标记羊抗鼠IgG抗体进行Western bloting鉴定, 结果出现一条特异性的抗原-抗体结合带。结果显示, 诱导的裂解物中确实存在能特异地与抗vp7McAb结合的蛋白, 分子量约为28kD, 其产物的抗原性与A组轮状病毒vp7蛋白相同。
3 讨论本研究利用RT-PCR技术扩增了A组轮状病毒VP7基因, 通过转基因方法成功地将其转入到乳酸杆菌中, 经乳糖诱导重组乳酸杆菌, 产生表达蛋白, SDS-PAGE电泳分析得出, 诱导4, 8, 12 h后均可见一条约28kD的蛋白带表达, 且与乳酸杆菌标准株对比其蛋白的表达量明显增加, 说明重组乳酸杆菌中VP7基因成功得到了高效表达; 同时, 经扫描分析发现, 当经乳糖诱导4, 8, 12 h后, 测定表达蛋白量分别约占总体蛋白量2.30%, 5.12%, 5.38%, 随着时间的增加其表达蛋白的量也逐步增多。另外, 对表达产物进行Western blotting分析表明, 表达的VP7蛋白具有较好的生物活性, 能够和鼠抗VP7McAb进行特异性结合, 其结合的量随着产物表达的量的增加而增加, 且明显高于对照的标准乳酸杆菌菌株, 说明A组轮状病毒VP7基因重组质粒在乳酸杆菌中表达的蛋白抗原活性与VP7蛋白抗原性一致。因此, 通过本次研究可以得出, A组轮状病毒VP7基因重组乳酸杆菌, 经诱导可持续高效表达VP7基因, 产生活性VP7蛋白, 为进一步构建新型的轮状病毒VP7基因工程疫苗提供了基础依据。
致谢 (衷心感谢中国疾病预防控制中心病毒所段召军老师在实验材料方面给予的帮助。)| [1] | Nga BH. Genome analysis of lactic acid bacteria in food fermentations and biotechnological appIications[J]. Curr Op in Microbiol, 2005, 8(3) : 307–312. DOI:10.1016/j.mib.2005.04.001 |
| [2] | Morello E, Bermúdez-Humarán LG, UuIl D, et al. Lactococcuslactis, an efficient cell factory for recombinant protein production and secretion[J]. J Mol Nficrobiol Biotechnol, 2008, 14(1-3) : 48–58. |
| [3] | 马士恒, 陈宇萍, 安洪明, 等. 汉坦病毒全NP蛋白及其型特异区编码基因的克隆及表达[J]. 中国公共卫生, 2002, 18(12) : 1436–1438. |
| [4] | 贾士芳, 王萌榆, 郭兴华, 等. 乳酸杆菌电转化条件的研究[J]. 生物工程学报, 1998, 14(4) : 429–433. |
| [5] | Walker JM, Rapley R. Medical biomethods handbook[M].New York: Humana Press, 2005: 644. |
 2009, Vol. 25
2009, Vol. 25
