骨形态发生蛋白-7(BMP-7)能拮抗转化生长因子-β1(TGF-β1)作用而延缓肾小管间质纤维化〔1〕。多种信号途径〔2-4〕如蛋白激酶Cα(PKCα)可增加糖尿病(DM)肾组织TGF-β1及结缔组织生长因子(CTGF)的表达, 参与糖尿病肾病(DN)的发生发展; 给予依那普利阻断血管紧张素Ⅱ (ANGⅡ)可降低DM肾小管PKCα的活性, 减少细胞外基质沉积而延缓DN肾小管间质损害。有研究发现〔5〕, 依那普利可促进DM大鼠肾脏表达BMP-7。为探讨依那普利促进内源性BMP-7表达上调与其阻断PKCα和ANGⅡ的表达关系进行了本研究。
1 材料与方法 1.1 试剂依那普利(江苏扬子江制药厂); 链脲佐菌素(STZ, 美国Sigma公司); 山羊抗大鼠BMP-7多克隆抗体(美国Santa cruz公司); 兔抗大鼠PKCα、ANGⅡ、CTGF和纤维连接蛋白(FN)多克隆抗体和生物素化山羊抗兔IgG (武汉博士德公司); UltraSensitiveTMSP超敏试剂盒(KIT-9709/9719, 批号: 707189709)和DAB显色试剂盒(批号: 705150031, 福州迈新公司); 二步法免疫组化检测试剂(PV-6001);二甲基氨基偶氧苯浓缩型DAB试剂盒(ZLI-9032)(批号: K72331B, 北京中杉公司); Taq PCR Master Mix、D2000(北京天根生化科技有限公司); 逆转录(RT)试剂盒(美国Fermentas公司); 血糖、血肌酐和尿蛋白检测试剂盒(四川迈克公司); Glucometer 4型血糖仪(美国Baer公司)。
1.2 糖尿病模型的制备、分组及药物剂量雄性SD大鼠18只, 体重174~204 g (上海西普尔-必凯实验动物有限公司)许可证号: SCXK (沪)2003-0002。随机选取6只大鼠作为正常对照组, 于尾静脉注射0.01 mol/L的无菌柠檬酸-柠檬酸钠缓冲液(pH 4.5)。其余大鼠尾静脉注射溶于0.01 mol/L的无菌柠檬酸-柠檬酸钠缓冲液的STZ (pH 4.5), 剂量为50 mg/kg。注射后48 h尾静脉采血测血糖, 凡血糖值≥16.7 mmol/L大鼠作为糖尿病大鼠〔6〕。将糖尿病大鼠随机分为2组, 每组6只, 糖尿病组和依那普利治疗组。治疗组灌胃给予依那普利10 mg/(kg·dw), 连续12周。大鼠喂以普通饲料, 自由饮水。
1.3 检测方法 1.3.1 血、尿及肾组织采集大鼠处死前代谢笼收集24 h尿; 心脏穿刺采血; 肾脏经充分灌洗后, 称重, 一侧肾脏置-80 ℃冰箱保存供RT-PCR检测用, 另一侧肾脏用4%多聚甲醛固定, 供石蜡切片用。
1.3.2 免疫组织化学3 μm厚肾组织石蜡切片, 微波修复抗原, 采用链霉素抗生物素蛋白-过氧化物酶(SP)法检测BMP-7、PKCα、ANGⅡ和链酶亲和素-过氧化物复合物(SABC)法测CTGF、FN, 以PBS作阴性对照, DAB染色。在高倍镜(400倍)下计数肾皮质10个不重复视野的BMP-7、PKCα、ANGⅡ和CTGF染色阳性肾小管数, 取均值; FN在显微镜测微尺(0.5网形目镜尺)下计数十字交叉点与FN阳性染色重合的点数, 计数10个视野(400倍), 取均值。
1.3.3 RT-PCR用Trizol试剂提取肾皮质总RNA, 1 μg总R NA按逆转录试剂盒方法进行RT-PCR检测。引物自行设计, 委托上海Generay Biotech公司合成。BMP-7产物长度451 bp, PKCα产物长度100 bp, β-actin产物长度490 bp。PCR反应参数根据各不同目的片段进行最优化。PCR反应条件: 94 ℃预变性2 min, 94 ℃变性30 s, 退火30 s (BMP-7温度为57.5 ℃, PKCα温度为54.3 ℃), 72 ℃延伸30 s, 40个循环后充分延伸10 min。最后将扩增产物于1.5%琼脂糖凝胶电泳, 应用凝胶成像系统进行扫描并用ChmioDox软件分析图像, PCR产物量以吸光度×面积表示, 与β-actin比值表示目的基因的相对含量。
1.3.4 其他指标检测氧化酶法测血糖, 终点法测血肌酐, 考马斯亮蓝法测尿蛋白, 按试剂盒说明书操作。
1.4 统计分析采用SPSS11.5软件进行分析, 组间数据比较采用单因素方差分析; 用Pearson's方法进行相关分析。
2 结果 2.1 各组生化指标变化(表 1)| 表 1 各组血糖、血肌酐、24 h尿蛋白和肾脏指数比较(x±s) |
糖尿病组的血糖、血肌酐及肾脏指数均明显高于正常对照组, 出现明显的尿蛋白; 依那普利治疗组与糖尿病组比较, 血肌酐和24 h尿蛋白量均明显下降, 肾脏指数相对减小。
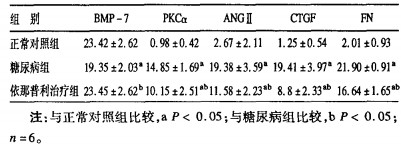
2.2 免疫组化结果(表 2)| 表 2 各组BMP-7、PK、ANGⅡ、CTGF和FN蛋白的表达(x±s) |
正常对照组BMP-7高表达于集合管和肾小管胞浆, 肾间质及肾血管外膜也有少量表达, 但肾小球未见阳性表达; 肾小管上皮细胞胞浆靠管腔侧有少量PKCα、ANGⅡ和CTGF的表达; FN沿肾小管基膜呈线性分布。糖尿病组BMP-7表达明显低于正常对照组; 同时肾小管上皮细胞PKCα、ANGⅡ和CTGF明显增多, FN表达也明显增多。依那普利治疗组肾小管BMP-7的表达高于糖尿病组, 与正常对照组比较差异无统计学意义; PKCα、ANGⅡ和CTGF表达比糖尿病组显著减少, 但3者表达仍高于正常对照组, 同时FN的表达也明显低于糖尿病组。
2.3 RT-P C R结果(图 1)

|
注:M:Marker;1:正常对照组;2:糖尿病组;3:依那普利治疗组。 图 1 RT -PCR示各组大鼠肾皮质中BMP-7和PKCom~RNA水平 |
正常对照组肾皮质BMP-7 mRNA呈强表达, PKCαmRNA有少量表达; 糖尿病组BMP-7 mRNA表达明显减少, 同时PKCαmRNA的表达明显增多; 与糖尿病组比较, 依那普利治疗组BMP-7 mRNA表达表显上调, 而PKCαmRNA的表达明显降低。
2.4 相关性分析糖尿病组BMP-7蛋白分别与PKCα、ANGⅡ、CTGF、FN蛋白呈显著负相关(r=-0.992, -0.997, -0.539和-0.977, P < 0.01); ANGⅡ蛋白与CTGF、FN呈明显著正相关(r=0.602, P < 0.05和0.975, P < 0.01)。依那普利治疗组BMP-7蛋白分别与PKCα、ANGⅡ、CTGF、FN蛋白也同样呈显著负相关(r=-0.838, -0.885, -0.829, P < 0. 05和-0.931, P < 0.01); ANGⅡ蛋白与CTGF、FN呈显著正相关(r=0.829和0.886, P < 0.05)。
3 讨论研究发现〔7-9〕, DM大鼠肾小管BMP-7表达与肾脏病变相关联, 而给予依那普利可上调内源性BMP-7表达。但是, 依那普利调节DM大鼠肾小管BMP-7的作用机制尚不清楚。本研究观察到, 糖尿病组大鼠肾小管BMP-7 mRNA和蛋白减少, 尤其mRNA减少更明显, 而ANGⅡ表达增多, 并且2者呈显著负相关。依那普利治疗则使肾小管ANGⅡ表达减少约40%, 而BMP-7 mRNA和蛋白表达增加, 提示依那普利可能通过抑制ANGⅡ的生成而上调BMP-7 mRNA和蛋白的表达。
DM时肾小管表达PKCα增多, 高糖和AngⅡ对PKCα激活有协同作用; 使用ANGⅡ受体(AT1)阻断剂可以减少PKCα表达〔4, 10-11〕。研究表明, 给正常大鼠注射ANGⅡ可显著上调肾小管CTGF的表达〔12〕; CTGF可以抑制BMP-7的下游Smad1/5信号通路而抑制BMP-7对肾脏的保护作用〔13〕。本研究显示, 糖尿病组大鼠肾小管PKCα蛋白和mRNA表达增多, 并且与ANGⅡ表达增多相一致, 糖尿病组和依那普利治疗组大鼠肾小管ANGⅡ蛋白与CTGF和肾小管间质FN蛋白呈显著正相关, 并且FN蛋白与BMP-7呈负相关, 提示依那普利可能通过抑制ANGⅡ的生成, 减少PKCα表达从而减弱CTGF对BMP-7下游信号的抑制作用, 使FN的沉积减少和改善肾功能。
| [1] | Motazed R, Colville-Nash P, Kwan JT, et al. BMP-7 and proximal tubule epithelial cells: activation of multiple signaling pathways reveals a novel anti-fibrotic mechanism[J]. Pharm Res, 2008, 25(10) : 2440–2446. DOI:10.1007/s11095-008-9551-1 |
| [2] | Yu T, Khraibi AA. Enalapril treatment restores the decreased proximal tubule reabsorption in response to acute volume expansion in diabetic rats[J]. Life Sci, 2008, 29(9-10) : 364–368. |
| [3] | Kellner D, Chen J, Richardson I, et al. Angiotensin receptor blockade decreases fibrosis and fibroblast expression in a rat model of unilateral ureteral obstruction[J]. J Urol, 2006, 176(2) : 806–812. DOI:10.1016/j.juro.2006.03.076 |
| [4] | 肖瑛, 石明隽, 张国忠, 等. 糖尿病大鼠肾小管PKC-和CTGF表达的动态变化[J]. 中国病理生理杂志, 2007, 23(1) : 183–185. |
| [5] | 程虹, 田雪飞, 董鸿瑞, 等. 波生坦及依那普利对糖尿病肾病模型干预的对比研究[J]. 中华肾脏病杂志, 2004, 20(3) : 154–158. |
| [6] | 方开云, 娄晶磊, 肖瑛, 等. 转化生长因子β1和Snail1参与糖尿病大鼠肾小管上皮细胞向间充质细胞转变[J]. 生理学报, 2008, 60(1) : 125–134. |
| [7] | Hruska KA, Guo G, Wozniak M, et al. Osteogenic protein-1 prevents renal fibrogenesis associated with ureteral obstruction[J]. Am J Physiol Renal Physiol, 2000, 279(1) : F130–F143. |
| [8] | Morrissey J, Hruska K, Guo G, et al. Bone morphogenetic protein-7 improves renal fibrosis and accelerates the return of renal function[J]. J Am Soc Nephrol, 2002, 13(Suppl 1) : S14–S21. |
| [9] | 周剑锋, 李娜, 袁发焕, 等. 依那普利对大鼠肾间质损害骨形成蛋白-7及其受体表达的影响[J]. 中国现代医学杂志, 2007, 17(14) : 1693–1696. |
| [10] | Li S, Duan P, You G. Regulation of human organic anion transporter 1 by ANGⅡ: involvement of protein kinase alpha[J]. Am J Physiol Endocrinol Metab, 2009, 296(2) : E378–E383. |
| [11] | Yao LJ, Wang JQ, Zhao H, et al. Effects of telmisartan on expression of proten kinase Cα in kidney of diabetic mice[J]. Acta Pharmacol Sinica, 2007, 28(6) : 829–838. DOI:10.1111/aphs.2007.28.issue-6 |
| [12] | Nguyen TQ, Roestenberg P, Van Nieuwenhoven FA, et al. CTGF inhibits BMP-7 signaling in diabetic nephropathy[J]. J Am Soc Nephrol, 2008, 19(11) : 2098–2107. DOI:10.1681/ASN.2007111261 |
| [13] | Ruperez M, Ruiz-Ortega M, Esteban V, et al. Angiotensin Ⅱ in-ceases connective tissue growth factor in the kidney[J]. Am J Pathol, 2003, 163(5) : 1937–1947. DOI:10.1016/S0002-9440(10)63552-3 |
 2009, Vol. 25
2009, Vol. 25