2. 四川大学公共卫生学院医学检验教研室
目前, 健康人群流脑带菌调查主要是用传统分离培养法〔1-6〕。该法确诊脑膜炎奈瑟菌(Neisseria meningitidis, Nm)感染至少需要2~3 d, 其中血清学鉴定因其灵敏度不够高, 影响因素较多, 有时难于作出可靠诊断, 尤其在大规模流行病学调查时, 常因工作量大, 检测者经验不足、情绪波动等主观因素而影响结果可信度。常规PCR方法受多种因素影响, 灵敏度较低、对细菌含量低样本检测困难、检测结果易出现假阳性或假阴性, 而荧光定量PCR是近年发展迅速的基因诊断新技术〔7-12〕。为了比较新型水解探针(TaqMan-MGB探针)荧光定量PCR法、常规PCR法和传统分离培养法在检测脑膜炎奈瑟菌上的优劣, 本文应用3种方法检测230份咽拭子标本, 探讨TaqMan-MGB探针荧光定量PCR法在流脑流行病学调查中应用价值。现将结果报告如下。
1 材料与方法 1.1 材料(1)标本来源: 2007年3月采集泸州市某地农村健康中小学学生的咽拭子标本230份, 男性119份, 女性111份。(2)仪器与试剂: SLAN荧光定量PCR检测系统(上海宏石医疗科技有限公司); 普通PCR扩增仪(德国Biometra公司); 凝胶成像系统(英国UVI tec lomited公司); Biospecmini DNA/RNA /Protein analyzer (日本岛津公司)。dNTPs、Taq DNA聚合酶, 分子量标准等(大连宝生物工程有限公司)。(3)标准品:以脑膜炎奈瑟菌29021为参考菌株, PCR扩增porA基因并克隆到质粒载体。提取纯化重组子DNA, 稀释至108 Copies/mL作为强阳性质控标准品, 10倍梯度稀释至103 Copies/mL作为弱阳性质控标准品。
1.2 方法 1.2.1 引物设计采用Primer Express 2.0等软件, 针对脑膜炎奈瑟菌PorA基因设计引物和MGB探针, 上游引物: 5'-GCGGAAGTGCGTTTGGAA-3', 下游引物: 5'-CGCGGTAAAAAAGGCGAAA-3', 扩增产物长度为80 bp。探针序列: 5' FAM-ATCATAATCAACGCCGGCG-MGB 3'。引物和MGB探针均由上海基康生物技术有限公司合成。
1.2.2 反应模板制备参照文献〔7, 13〕, 咽拭子在1 mL生理盐水中振荡30 s, 挤压后弃去, 离心, 去上清, 余50 μL液体, 100 ℃煮沸10 m in, 取上清5 μL用于PCR检测。
1.2.3 荧光定量PCR扩增加入模板后荧光定量PCR反应体系为: 25 μL, 引物各0.6 μmol/L, 探针0.1 μmol/L, MgCl2 7.0 mmol/L, dNTP各300 μμmol/L, Taq DNA聚合酶1.0 U, 10×Buffer 2.5 μL。循环条件: 94 ℃预变性3 min, 然后94 ℃变性20 s, 58℃退火30 s, 72 ℃延伸20 s, 循环40次。在每一循环延伸阶段采集荧光信号。试验设定阳性对照、弱阳性对照与空白对照(no template control, NTC)。PCR反应的前6~12个循环的荧光信号作为荧光本底信号。按照荧光定量PCR分析软件设定基线与阈值, 以模板原始拷贝浓度的对数值(logC0)为横坐标, 临界循环数值(threshold cycle, Ct) Ct值为纵坐标, 绘制标准曲线。荧光定量PCR结果判定:扩增曲线规则, 呈对数增长, Ct值≤38即可判定为阳性; 如扩增曲线荧光增量(∆Rn) < 阈值或Ct值> 40, 则为阴性; 若Ct值在38~40之间, 且扩增曲线呈对数增长, 重复测定, 若Ct值仍在38~40之间, 则为阴性。
1.2.4 常规PCR加入模板后PCR反应纱为: 25 μL, 引物各0.3 μmol/L, MgCl2 3.0 mmol/L, dNTP各100 μmol/L, Taq DNA聚合酶1.0U, 10×Buffer 2.5 μL。循环条件: 94 ℃预变性3 min; 94 ℃变性30 s、56 ℃退火30 s、72 ℃延伸20 s, 35个循环; 2 ℃延伸3 min。产物用2.5%的琼脂糖凝胶电泳, 凝胶成像系统下观察结果。电泳结果判断:用PorA引物扩增出80 bp的阳性条带为脑膜炎奈瑟菌, 未出现80 bp条带为非脑膜炎奈瑟菌。
1.2.5 常规分离培养法采集调查对象咽拭子直接接种在含多粘菌素和万古霉素双抗的巧克力平板, 37 ℃, 5% CO2培养18~24 h, 转种或挑取可疑菌落分离培养, 并按国标方法(GB16884-1997)进行鉴定。
1.3 统计分析采用SPSS 13.0软件进行统计分析, 配对四格表χ2检验。
2 结果 2.1 荧光定量PCR法标准曲线以10倍梯度稀释配置原始拷贝数101~108 Copies/mL的标准品系列, 取5 μL进行荧光定量PCR, 绘制标准曲线, 其回归方程为Ct=3.673 14 logC0 + 45.298 59, 线性范围为4×103~4×108 Copies/mL, 最低可检测5 Copies/反应体系。Ct值与原始拷贝数对数值的相关系数r2=0.995 06, 定量准确。根据公式E=10-/k -1计算得到PCR的扩增效率E=0.87, 在PCR扩产效率的理想范围0.8~1.2之间。
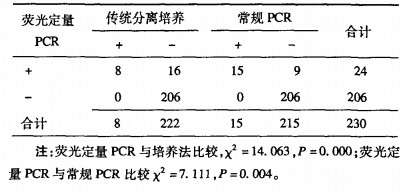
2.2 咽拭标本检测结果(表 1)| 表 1 咽拭标本中脑膜炎奈瑟茵检测结果 |
230例咽拭标本, 分别用TaqMan-MGB探针荧光定量PCR法、常规PCR法和传统分离培养法进行检测。传统分离培养法检出阳性标本8例, 阳性率为3.48%;常规PCR法阳性15例, 阳性率为6.52%;荧光定量PCR法阳性24例, 阳性率为10.43%。荧光定量PCR法的阳性率高于其他法(P=0.000, P=0.004)。对培养法和常规PCR法检出的阳性样本, 荧光定量PCR法的灵敏度均为100%, 特异度分别为92.8%和95.8%。
3 讨论本文结果显示, 荧光定量PCR法、常规PCR法和传统分离培养法检测咽拭子中的脑膜炎奈瑟菌, 阳性率分别为10.43%, 6.52%和3.48%, 荧光定量PCR方法的阳性率明显高于常规PCR法和传统培养法, 差异有统计学意义(P < 0.001)。荧光定量PCR方法灵敏度高, 特异性好; 并且2~4 h可获得结果, 200多份标本1个人1 d内即可完成检测, 操作步骤简单, 自动化程度高, 检测速度快, 可实现高通量, 节省人力、物力。
较大规模流行病学调查中, 咽拭标本的采集更简便、安全, 易被调查对象接受。本文结果表明, 直接从咽拭子提取模板DNA进行检测, 既可提示咽拭子中脑膜炎奈瑟菌DNA的存在, 评估健康人群带菌情况, 也可作为筛查手段用于流行病学调查, 提高脑膜炎奈瑟菌的检出率, 为处理突发公共卫生事件提供可靠的技术保障。
| [1] | 张艳梅, 王海, 胡中旺, 等. 脑膜炎双球菌的PCR法快速检测[J]. 中国公共卫生, 2006, 22(3) : 297–298. |
| [2] | 刘美真, 杨华可, 廖国东, 等. 2005年广东省健康人群流脑免疫水平和带菌状况调查[J]. 中国卫生检验杂志, 2007, 17(2) : 325–326. |
| [3] | 温群文, 段永翔, 鞠长燕. 深圳市健康人群流脑带菌状况调查[J]. 预防医学情报杂志, 2006, 22(5) : 427–529. |
| [4] | 伏晓庆, 尹建雯, 高援. 云南省2005年健康人群流脑带菌调查结果分析[J]. 实用预防医学, 2006, 13(2) : 341–342. |
| [5] | 高秀媛, 曹淑媛, 李征, 等. 华东某省进京人群的流脑带菌调查[J]. 中国中西医学杂志, 2006, 4(7) : 120–121. |
| [6] | 林云万, 刘俊华, 张欣强. 广州市健康人群流脑带菌状况的调查[J]. 中国公共卫生管理, 2005, 21(3) : 223–224. |
| [7] | Jordens JZ, Heckels JE. A novelporA-based real-time PCR for detection of meningococcal carriage[J]. JM edMicrobiol, 2005, 54 : 463–466. |
| [8] | Lole K S, Arankalle VA. Quantiatation of hepatitis B virus DNA by realtime PCR using internal amplification control and dual TaqM an MGB probes[J]. JViro lMethods, 2006, 135 : 83–90. |
| [9] | Pas SD, Noppornpanth S, et al. Quantification of the newly detected lamivudine resistant YSDD variants of hepatitisB virususing molecular beacons[J]. J C linVirol, 2005, 32(2) : 166–172. |
| [10] | Matin M, Videma DG, Serrano M JR, et al. Rapid direct detection of multiple rifampin and isoniazid resistance mutations in Mycobacterium tuberculosis in respiratory samples by real-time PCR[J]. Antimicrob Agents Chemother, 2004, 48 : 4293–4300. DOI:10.1128/AAC.48.11.4293-4300.2004 |
| [11] | 匡红, 陈庆海, 府伟灵. 分子信标探针荧光芯片检测结核分枝杆菌的实验研究[J]. 中华医院感染学杂志, 2007, 17(5) : 509–512. |
| [12] | Kesanopoulos K, Tzanakaki G, Levidiotou S, et al. Evaluation of touch-down real-time PCR based on SYBR Green If luorsecent dye for the detection of Neisseriameningitid is in clinical samples[J]. FEMS Immunology and Medical Microb, 2005, 43 : 419–424. DOI:10.1016/j.femsim.2004.10.011 |
| [13] | Jordens JZ, Williams, Jones GR, et al. Detection of meningococcal carriage by culture and PCR of throat swabs and mouth gargles[J]. JClin Microbi, 2002, 40(1) : 75–79. |
 2009, Vol. 25
2009, Vol. 25