2. 山西医科大学公共卫生学院流行病学教研室
母婴垂直传播是造成我国乙肝病毒携带者众多的主要原因之一。虽然胎盘有物理屏障对抗病原体的入侵, 但胎盘仍可通过此途径发生感染。近年来已有研究显示〔1-2〕, 多数病毒如人类免疫缺陷病毒、乙肝病毒、细小病毒、血浆壳抗原抗体(EB)病毒等可感染胎盘从而波及胎儿; 在HBsAg阳性孕妇中, 胎盘乙型肝炎病毒(HBV)感染率约为15%~40%〔3〕, HBV通过感染孕妇胎盘进而感染胎儿是宫内传播的途径之一〔4〕。探讨胎盘HBV感染机制的体外研究可选用胎盘细胞原代培养和细胞系来进行。本研究旨在探讨胎盘滋养层细胞系Bewo被HBV感染的可能性, 为HBV母婴传播过程中胎盘细胞感染机制的研究建立合适的体外模型。
1 材料与方法 1.1 材料(1)细胞、培养基及其添加物:人胎盘滋养层细胞来源的Bewo细胞系(协和医科大学基础医学细胞中心); F12培养基(美国Hyclone公司); 标准胎牛血清(天津市灏洋生物制品科技有限责任公司); 青霉素、链霉素(华北制药公司)。(2)试剂:鼠抗人HBsAg IgG (美国Santa Cruz公司); 生物素化鼠抗人卵白素-生物素过氧化物酸复合物(ABC)试剂盒(美国Vector Laboratories Inc公司); HBV PCR荧光定量检测试剂盒(中山大学达安基因股份有限公司)。
1.2 方法 1.2.1 Bewo细胞的HBV体外感染试验选择处于对数生长期的Bewo细胞作为研究对象, 设HBV感染组和对照组; HBV感染组:移去旧培养基, 加入100 μL 108 copies的HBV DNA阳性血清与5 mL新鲜完全培养基共同培养。1或2 d后, 留取各瓶中培养上清备检; 用0.01 mol/L磷酸盐缓冲液(PBS)充分洗涤细胞10次, 并留存第10次洗液备检; 洗净细胞后加入5 mL完全培养基继续培养, 分别收集洗后1, 2, 3 d上清液备检; 对照组:移去旧培养基, 加入与感染血清等量的0.01 mol/L PBS及5 mL新鲜完全培养基, 其余处理同感染组。
1.2.2 细胞培养上清中HBV DNA检测按照荧光定量PCR方法试剂说明书进行。
1.2.3 细胞爬片的制作选择处于对数生长期的Bewo细胞, 接种入预先放置无菌盖玻片的培养皿中, 设HBV感染1, 2 d组和阴性对照组, 每组6份; 培养1或2 d后, 常规0.01 mol/L PBS漂洗, 1%多聚甲醛固定。
1.2.4 免疫细胞化学ABC法检测细胞爬片中HBsAg以HBV DNA阳性血清共孵育的Bewo细胞爬片为检测对象, 以未加HBV DNA阳性血清的Bewo细胞爬片为阴性对照, 以不加一抗而以PBS代替的Bewo细胞爬片为空白对照进行HBsAg检测。按试剂说明书进行操作。
2 结果 2.1 人胎盘滋养层细胞系Bewo体外生长曲线在培养Bewo细胞0, 1, 2, 3, 4, 5, 6 d后, 用台盼兰计数活细胞个数, 来观察细胞的生长状况和细胞增殖周期。培养时间与细胞增殖的关系显示, Bewo细胞接种后1 d即进入对数生长期, 活细胞数开始快速增长; 至接种第5 d开始生长缓慢, 第6 d进入生长停滞期。因此, 选择接种后第1, 2, 3 d的细胞进行各项干预试验和指标测定。
2.2 胎盘滋养层细胞系Bewo形态(图 1, 2)
|
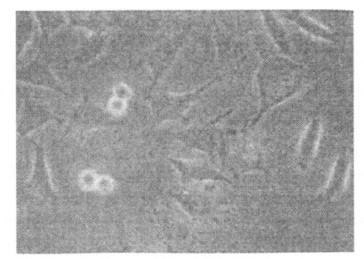
图 1 人胎盘滋养层细胞来源的Bewo细胞(培养第2 d, 200×) |
|
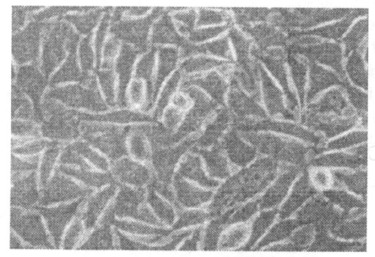
图 2 人胎盘滋养层细胞来源的Bewo细胞(培养第5 d, 200×) |
倒置显微镜下观察, Bewo细胞接种2 h后开始贴壁, 24 h绝大多数细胞明显贴壁。贴壁的Bewo细胞呈立方多角形或圆形、卵圆形, 细胞核大、较圆; 传代1 d后细胞进入对数生长期, 细胞分裂相增多。
2.3 与HBV DNA阳性血清共同培养Bewo细胞形态(图 3)
|
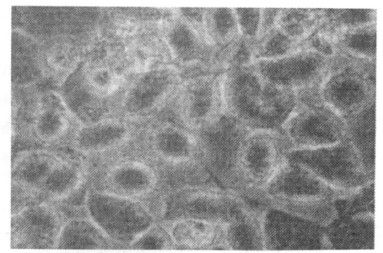
图 3 与HBV DNA阳性血清共同培养的Bewo细胞(400 ×) |
HBV DNA阳性血清共同培养对细胞形态无明显变化, 加入感染血清后细胞继续生长, 培养1 d后进入对数生长期, 细胞分裂相多见, 贴壁情况与对照组无明显不同; 但与对照组相比, 随着培养时间的延长(从培养第3 d开始), 细胞生长状况明显不良, 死亡细胞数量明显增多。死亡细胞表现为细胞变小变圆, 核皱缩, 脱壁。
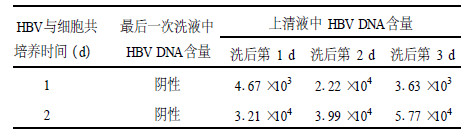
2.4 HBV DNA阳性血清与Bewo共孵育后培养上清中HBV DNA含量(表 1)| 表 1 HBV DNA阳性血清与Bewo细胞共培养后上清中HBV DNA含量 |
HBV DNA阳性血清与Bewo细胞共培养1, 2 d组, 细胞感染后不同时段1, 2, 3 d在培养上清液中均可检出HBV DNA。
215 HBsAg在感染细胞中的表达收集细胞爬片后, 用免疫细胞化学技术检测细胞内HBsAg的表达, 可见阳性细胞散在分布于爬片上; 阳性物质呈细小棕黄色颗粒, 多呈胞浆均质型, 少数呈胞浆不均质型; 少数细胞核内亦可见阳性表达。光镜下阳性细胞未见形态学上的明显变化。
3 讨论HBV的产前传播过程中, 胎盘组织在其中起重要作用。滋养层细胞是胎盘屏障的第一层细胞, 在妊娠过程中, 胎盘滋养层细胞与母体血液直接接触, 是HBV通过胎盘屏障的第一步, 所以研究滋养层细胞的HBV感染对探讨HBV宫内感染机制很有意义〔5, 7〕。
本研究用乙肝患者HBV DNA阳性血清直接感染体外培养的人胎盘绒毛滋养层细胞来源的细胞系Bewo, 建立HBV感染和复制的细胞模型, 实验中未添加任何辅助因子, 在实验实施过程中采用了各种措施防止污染, 进行质量控制, 并设置了空白对照, 初步证实HBV可成功感染细胞。用自然存在于病人血液中的HBV直接感染培养细胞, 可建立接近自然感染状态的细胞模型, 适用于HBV感染靶细胞的方式、复制机制的研究。
用HBV DNA阳性血清体外直接感染Bewo后, 在培养上清中检出了HBV DNA; 免疫组化检测细胞爬片中的HBsAg, 在Bewo细胞中检出较强的阳性信号, 证实细胞内HBsAg亦有较好的表达。因此, 可以认为血清中的乙型肝炎病毒在体外可直接感染Bewo细胞系; 培养上清及细胞中检测到的HBV标志物是新复制出的, 而非感染血清残留。根据为细胞与HBV DNA阳性血清共同孵育1或2 d后经10次洗涤留取的最后1次洗液, 经荧光定量PCR检测证实HBV DNA为阴性; 在洗净残留血清后的细胞再培养1, 2, 3 d后, 又可检出HBV DNA。由于细胞爬片能较好地保持培养细胞的形态和结构, 所以在实验中用细胞爬片对细胞内乙肝表面抗原的表达和定位进行观察, 结果与人体内胎盘组织的乙肝表面抗原检测结果相似, 提示HBV在体外胎盘细胞中的复制、表达可能与体内接近。
Bewo细胞系通常被用来进行胎盘屏障生理功能研究〔8〕, 也被用来进行人类免疫缺陷病毒(HIV)的体外研究〔9〕。2007年Bhat P等〔10〕首次用其模拟胎盘屏障进行鸭乙肝病毒穿越胎盘的研究。本研究采用该细胞系构建HBV体外直接感染胎盘细胞模型, 以研究HBV宫内感染或胎盘感染机制。实验表明, 本研究构建模型操作简便易行、价格适中、易于推广使用。
| [1] | Kaplan C. The placenta and viral infection[J]. Clin Obstet Gynecol, 1990, 33(2) : 232–241. DOI:10.1097/00003081-199006000-00005 |
| [2] | Lucifora G, Calabro S, Carroccio G, et al. Immunocytochemical HB-sAg evidence in placenta of asymptomatic carriermothers[J]. Am J Obster Gynecol, 1988, 159 : 839–842. DOI:10.1016/S0002-9378(88)80149-2 |
| [3] | 王素萍, 李铁钢, 魏俊妮, 等. 乙型肝炎病毒宫内感染相关因素的研究[J]. 中华妇产科杂志, 2005, 40(10) : 670–672. |
| [4] | 徐德忠, 闫永平, 王素萍, 等. 胎盘组织在乙肝病毒宫内传播中的作用及其机制研究[J]. 中华医学杂志, 2001, 81(3) : 176–177. |
| [5] | 王安辉, 门可, 阎永平, 等. 乙型肝炎免疫球蛋白阻断胎盘滋养层细胞感染乙型肝炎病毒的试验研究[J]. 中华妇产科杂志, 2006, 41 : 165–168. |
| [6] | 张磊, 门可, 张景霞, 等. 亚洲人早孕胎盘绒毛滋养层细胞株的建立及其生物学特征研究[J]. 实用妇产科杂志, 2006, 22 : 232–235. |
| [7] | 李淑珍, 王素萍, 原琛利, 等. 孕妇HBV感染与胎盘组织TLR3表达关系[J]. 中国公共卫生, 2008, 24(2) : 129–131. |
| [8] | Zhou F, Hong M, You G. Regulation of human organic anion transporter 4 by progesterone and protein kinase C in human placental Bewo cells[J]. Am J Physiol endocrinolMetab, 2007, 293(1) : E57–61. DOI:10.1152/ajpendo.00696.2006 |
| [9] | Ayouba A, Cannou CmNgeyre MT, Barre-Sinoussi F, et al. Distinct efficacy of HIV-1 entry inhibitors to prevent cell-to-cell transfer of R5 and X4 viruses across a human placental trophoblast barrier in a reconstitution model in vitro[J]. Retrovirology, 2008, 5(1) : 31. DOI:10.1186/1742-4690-5-31 |
| [10] | Bhat P, Anderson DA. HepatitisB virus translocates across a troph-oblastic barrier[J]. J Virol, 2007, 81(13) : 7200–7207. DOI:10.1128/JVI.02371-06 |
 2009, Vol. 25
2009, Vol. 25

 , 宋秀霞2, 李晓燕2
, 宋秀霞2, 李晓燕2