近年来,地方性砷中毒对机体毒性作用研究正日益深入。研究已确认,砷能引起皮肤、肝、肾、免疫系统、外周神经系统等的损伤〔1-3〕,但砷对脑神经中枢的毒性作用和机制尚不十分清楚。虽有报道,砷可引起一定程度的智力低下和记忆减退〔4-5〕,但砷的中枢毒性作用仍需进一步明确,尤其对仔代的影响更应重视。因此,本研究以慢性砷中毒成年大鼠及其仔鼠为研究对象,以脑细胞能量代谢和超微结构为观察指标,探讨慢性砷暴露对中枢神经系统的毒性作用和可能机制,为砷中毒的研究和预防提供科学依据。
1 材料与方法 1.1 材料 1.1.1 动物分组及染砷100~120 g健康清洁级SD大鼠,雄雌各半,共100只〔贵阳医学院省实验动物中心,批号:SCXK (黔)2002-0001〕。大鼠随机分为对照、低砷、中砷、高砷和繁殖仔代组,每组20只; 染砷组自由饮用蒸馏水配制的As2O3水溶液; 低、中、高砷组As2O3浓度分别为3,15,75 mg/L〔6〕; 对照组饮蒸馏水。染砷剂量根据受试物半数致死量(LD50)确定〔7〕。分别染砷6和16周。繁殖仔代组10只正常配对产仔为对照,10只高砷暴露配对产仔,仔鼠继续高砷喂养16周。
1.1.2 主要试剂三氧化二砷(As2O3),分析纯(北京化工厂); 二磷酸腺苷(ADP)和己糖激酶(美国Sigma公司); K2HPO4、乙二胺四乙酸二钠盐(EDTA)、Tris-HCl、KH2PO4、蔗糖、葡萄糖、苹果酸和琥珀酸等(上海生工公司,进口分装)。
1.1.3 主要仪器透射电镜(日立H-7600);高速低温冷冻离心机(美国Sigma公司)、岛津UV-17000E、紫外可见分光光度计(日本岛津公司)、电动玻璃匀浆器(吉林贝尔公司)。
1.2 方法 1.2.1 大鼠处理成年鼠染砷6和16周,高砷孕产的仔鼠出生后持续高砷喂养16周,断头处死,分离左大脑半球,电子天平称重0.75 g,于脑组织匀浆缓冲液中剪碎,玻璃匀浆管中研磨和电动玻璃匀浆器匀浆(1 200 r/min)。
1.2.2 脑细胞线粒体制备差速离心法提取脑细胞线粒体〔8〕; 考马斯亮蓝法〔9〕定量线粒体蛋白。
1.2.3 脑细胞线粒体三磷酸腺苷(ATP)合成量测定制备磷标准曲线,参照文献〔8〕方法。分光光度法在660 mm波长下测出各管液中吸光度(A)值,从磷标准曲线中查出相应磷酸(Pi)的含量。对照管与空白管Pi含量的差值即为ATP产生量。结果用ATP nmol/(mg·pro)×min表示。
1.2.4 透射电镜制备取6, 16周成年染砷鼠和高砷孕产的仔鼠高砷喂养16周后,断头取大脑皮层组织,2.5%戊二醛固定,常规电镜技术制片,透射电镜观察。
1.3 统计分析采用SPSS统计软件进行t检验。
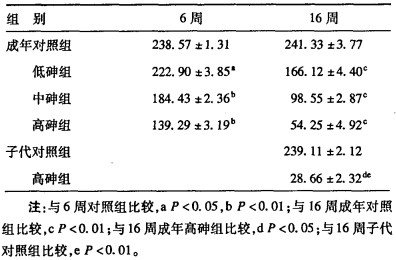
2 结果 2.1 不同剂量染砷成鼠6,16周后脑细胞线粒体ATP合成量(表 1)| 表 1 不同染砷时间和剂量大鼠脑细胞线粒体ATP合成量测定[nmol/(mg·pr)×min, x±s, n=10] |
表 1可见,成年鼠染砷6和16周后,脑细胞线粒体ATP合成量与对照组比较明显降低,并随染砷剂量和时间的增加降低更明显,即有剂量-效应和时间-效应关系; 其中6周低砷组与对照组比较,差异有统计学意义(P < 0.05);中、高砷组6和16周与对照组比较, 差异有统计学意义(P < 0.01)。
2.2 仔鼠高砷暴露16周脑细胞线粒体ATP合成量(表 1)高砷孕产的仔鼠继续高砷暴露16周后,脑细胞线粒体ATP合成量与仔代对照组比较明显降低,差异有统计学意义(P < 0.01);与成年高砷16周组比较降低更为明显,差异有统计学意义(P < 0.01)。
2.3 透射电镜观察大脑皮层神经细胞超微结构改变对照组大脑皮层神经细胞胞膜界线清晰,胞核大圆,核染色质均匀,胞质内质网、线粒体形态规则,分布均匀。6周低砷组可见皮层神经细胞胞浆增多,线粒体肿胀、粗面内质网扩张; 6周中、高砷组可见胞核染色质边集,胞质内细胞器减少,线粒体肿胀、数目减少; 16周低砷组可见异染色质明显减少,线粒体肿胀,粗面内质网扩张; 16周中、高砷组皮层神经细胞胞浆肿胀,异染色质明显减少,线粒体明显肿胀,细胞器减少; 16周高砷子代组皮层神经细胞核肿胀,异染色质明显减少,核内结构疏松,胞浆线粒体等细胞器明显减少,部分区域细胞器丢失,出现空泡征象。
3 讨论本研究发现,成年鼠长期水砷暴露,脑细胞线粒体ATP合成量比对照组明显减少,脑细胞超微结构也发生显著损伤改变。表明砷能通过成鼠血脑屏障进入脑组织,造成脑细胞能量代谢功能和超微结构严重受损,并且损伤具有剂量-效应和时间-效应关系。高砷环境孕产的仔鼠,脑细胞能量代谢功能和超微结构受损情况比成年高砷鼠表现得更严重,这提示砷能通过胎盘进入胎鼠血液中〔10〕,并且更易通过胎、幼鼠血脑屏障进入脑组织,对脑细胞产生直接的毒性损伤作用,胎幼鼠脑组织比成鼠对砷的毒性更为敏感。
脑组织是能量代谢较高的组织器官,正常情况下脑细胞线粒体经三羧酸循环产生ATP,为脑神经细胞的生物电及代谢活动提供丰富的能源,维持脑细胞的正常形态和生理功能〔11〕,当砷进入脑组织后,可能与脑细胞线粒体上含巯基的酶结合〔12〕,致使这些酶活性受到抑制,线粒体氧化磷酸化过程发生障碍,ATP产生量将会不足,脑细胞能量代谢发生紊乱,最终导致脑神经细胞线粒体和一些细胞器的形态以及脑细胞的多种功能受到严重损害。因此,推测砷对脑细胞能量代谢功能的损伤可能是砷的中枢毒性作用重要途径之一。
| [1] | Santra A, Maiti A, Das S, et al. Hepatic damage caused by chronic arsenic toxicity in experimental animals[J]. J Toxicol Clin Toxicol, 2000, 38 : 395–405. DOI:10.1081/CLT-100100949 |
| [2] | 朱筑霞, 费樱, 张爱华, 等. 燃煤型慢性砷中毒患者免疫功能改变的观察[J]. 中国地方病学杂志, 2004, 23(1) : 13–15. |
| [3] | 洪峰, 张爱华, 金泰廙, 等. 燃煤砷污染地区砷中毒患者的肾功能损害[J]. 环境与职业医学, 2007, 24(6) : 580–583. |
| [4] | 李军, 王三祥, 王正辉, 等. 砷中毒病区儿童智力水平调查[J]. 中国公共卫生, 2006, 22(7) : 856–857. |
| [5] | 孙贵范, 席淑华, 孙文娟, 等. 砷对仔代大鼠神经行为和学习记忆功能影响[J]. 中国公共卫生, 2006, 22(5) : 559–560. |
| [6] | 张晨, 马龙, 等. 染砷母鼠子代砷和脑砷含量[J]. 中华预防医学杂志, 1993, 27 : 59–61. |
| [7] | 顾学箕.中国医学百科全书[M]//毒理学.上海:上海科学技术出版社, 1982: 85-92. |
| [8] | 汪谦. 现代医学实验方法[M]. 北京: 人民卫生出版社, 1998: 338-344. |
| [9] | 张龙翔. 生化实验方法和技术[M].2版. 北京: 高等教育出版社, 1997: 138. |
| [10] | Waalkes MP, Ward JM, Liu J, et al. Transplacental carcinogenicity of inorganic arsenic in the drinking water:induction of hepatic, ovarian, pulmonary, and adrenal tumors in mice[J]. Toxicology and Applied Pharmacology, 2003, 186(1) : 7–10. DOI:10.1016/S0041-008X(02)00022-4 |
| [11] | Jerome YY, Robert MB, Robert CV. Cerebral energy metabolism during hypoxic-ischemia and early recovery in immature rats[J]. Am J Physiol, 1992, 262 : 672–677. |
| [12] | 李昕, 皮静波, 孙洋, 等. 长期染砷致家兔肝脏蛋白巯基水平及巯基代谢相关酶活力下降[J]. 中国地方病学杂志, 2004, 23(1) : 10–12. |
 2009, Vol. 25
2009, Vol. 25