手足口病(HFMD)是由多种人肠道病毒感染引起,其中以EV 71及Cox A16型最为常见〔1-3〕。由于肠道病毒传统的检测方法是病毒分离中和法定型,繁琐费时,不适合早期诊断。逆转录-聚合酶链反应(RT-PCR)方法敏感、特异、快速,但由于PCR扩增产物需要凝胶电泳检测,易造成实验室交叉污染。本研究建立的肠道病毒EV71 TaqMan荧光定量RT-PCR方法,具有敏感、特异、快速和实时在线检测等特点,较RT-PCR法具有更多的优点,适合于突发疫情的实验室早期诊断,该方法的建立为手足口病感染实验室检测提供了有效的分子生物学检测手段。现报告如下。
1 材料与方法 1.1 病毒株与临床标本肠道病毒EV71、柯萨奇A4(CA4)、CA9、CA16、CA21、CA24v、柯萨奇B3(CB3)、CB5、艾柯病毒6(E6)、E30、Sabin Ⅰ等病毒株(中国医学科学院、北京生物制品研究所和本省病毒所分离株)。临床样本来源于2008年上半年浙江省手足口病暴发疫情疑似患者的脑脊液、疱疹液、粪便等,样本采集后带冰运输到实验室。
1.2 引物与探针EV71引物和TaqMan探针的设计:从GenBank上下载不同年份和地区的肠道病毒EV71基因序列,用生物学软件进行同源性比较。在VPl区设计特异性引物和TaqMan探针。序列为EV71 F1:5′-TGATTGAGACACGSTGTGTYCTTA-3′,EV71 R1:5′-CCCGCTCTGCTGAAGAAACT-3′,EV71 Pb1:5′-TCGCACAGCACAGCTGAGACCACTC-3′。肠道病毒荧光定量RT-PCR引物和探针参照文献〔4〕。引物和探针由上海基康生物工程有限公司合成。
1.3 病毒定量标准与RNA的提取以肠道病毒EV71为标准株,用人横纹肌瘤细胞(RD)进行病毒效价滴定(106.2 TCID50/mL)后作为参考株,将其稀释至1 000,100,10,1.0,0.1,0.01 TCID50/mL。病毒RNA的提取采用The RNeasy Mini Kit试剂盒(德国QIAGEN公司),按说明书操作。
1.4 荧光RT-PCR反应体系和条件选用一步法荧光RT-PCR Kit (宝生物工程公司),试剂代码DRR064A,反应体系为25 μL,其中2×RT-PCR缓冲液12.5 μL,Ex Taq HS 0.5 μL,RT酶混合物Ⅱ0.5 μL,上游与下游引物(20 μmol/L)各0.6 μL,探针(20 μmol/L)0.3 μL,模板RNA8 μL,焦碳酸二乙酯(DEPC)处理水1.5 μL。反应条件为42 ℃ 30 min,95 ℃ 2 min进行逆转录,然后95 ℃ 5 s,55 ℃ 35 s,进行40个循环,在55 ℃进行单点荧光检测。根据荧光定量RT-PCR扩增曲线和Ct值判断结果。
1.5 RT-PCR反应体系和条件EV71 PR-PCR引物序列,上游159S:5′-ACYATGAAAYTGTGCAAGG-3′,下游162A:5′-CCRGTAGGKGTRCACGCRAC-3′,扩增片段448 bp,采用一步法RT-PCR Kit,试剂代码DRR024A,反应体系为25 μL,其中10×RT-PCR缓冲液2.5 μL,MgCl2 25 μL,dNTPmix (10 mmol/L)2.5 μL,RNase抑制剂(5 U/μL)0 5 μL,AMV酶0.5 μL,Taq酶0.5 μL,上游与下游引物(20 μmol/L)各0.5 μL,模板RNA 8 μL,DEPC水4.5 μL。反应条件为50 ℃ 30 min,95 ℃ 3 min进行逆转录,然后95 ℃ 20 s,50 ℃ 25 s,72 ℃ 30 s进行40个循环后转入72 ℃ 10 min,取8 μL产物跑琼脂糖凝胶电泳后,根据DNA分子量标准判断有无特异性条带。
1.6 荧光RT-PCR特异性、敏感性和重复性试验选择肠道病毒EV71、CA16、CA4、CA9、CA21、CA24v、E6、E30、CB3、CB5、SabinI和2008年手足口病暴发疫情疑似患者的脑脊液、疱疹液和粪便等临床样本,对上述病毒株和样本分别提取病毒核酸,用EV71荧光定量RT-PCR方法进行检测,验证方法的特异性。对已标定TCID50滴度(106.2 TCID50/mL)的EV71病毒做1 000,100,10,1.0,0.1 TCID50/mL系列稀释后分别提取RNA,平行进行荧光定量RT-PCR与RT-PCR反应,比较其灵敏度。此外,对不同浓度的病毒稀释液作3次重复检测,得到的Ct值计算标准差,验证方法的重复性。
2 结果 2.1 特异性试验荧光RT-PCR方法对肠道病毒EV71具有较好的特异性,对其他肠道病毒如CAl6、CA4、CA9、CA21、CA24v、E6、E30、CB3、CB5 and Sabin I等无交叉反应,对2008年手足口病暴发疫情患者的临床样本如疱疹液等呈阳性反应。
2.2 敏感性试验对肠道病毒EV71毒株,采用RD细胞进行病毒效价测定(106.2 TCID50/mL,然后稀释成1 000,100,10,1.0,0.1,0.01 TCID50/mL提取病毒RNA,分别用荧光RT-PCR与常规RT-PCR方法进行检测。结果荧光RT-PCR方法检测敏感性达到0.1 TCID50/mL,RT-PCR方法检测敏感性达1.0 TCID50/mL,荧光RT-PCR方法比常规RT-PCR方法的灵敏度高10倍。
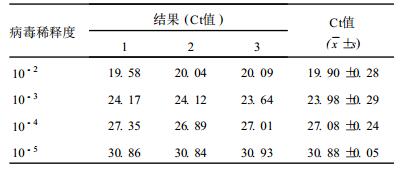
2.3 重复性试验(表 1)| 表 1 荧光定量RT-PCR法检测肠道病毒EV71重复性试验 |
EV71毒株按10倍梯度稀释成4个不同的浓度,对每一个浓度的样本作3个重复检测。结果不同核酸浓度各自的检测Ct值标准差在0.05~0.29之间,具有较好的重复性。
2.4 手足口病患者临床样本的检测从2008年浙江省各地送检的手足口病暴发疫情疑似患者的疱疹液、脑脊液和粪便等临床样本中直接提取病毒RNA,用肠道病毒荧光定量RT-PCR方法、EV71荧光定量RT-PCR方法和EV71 RT-PCR方法同时对120份临床样本进行检测。结果,肠道病毒核酸阳性84份,荧光定量RT-PCR方法检测EV71核酸阳性49份,RT-PCR法检测EV71核酸阳性41份,荧光定量RT-PCR方法比RT-PCR法检出的阳性率高。所有EV71核酸阳性的样本肠道病毒核酸均阳性。
3 讨论近年来,随着分子生物学技术的发展,采用RT-PCR技术对传染病突发疫情进行实验室诊断国内外已有报道,它具有灵敏度高,特异性强,所需时间短等优点,已在各个领域得到广泛应用〔5-6〕,但由于RT-PCR法检测时间仍需6~7 h,且容易由于PCR扩增产物污染而产生假阳性。有关Real-time PCR法检测EV71核酸的文献报道较少〔7-8〕,而且也存在着各种不足。如有的文献报道,其荧光探针是杂交探针,不是常用的水解探针且必须在特定型号的荧光PCR仪上进行,缺乏通用性;有的文献使用的虽是特异性TaqMan水解探针,但只适合于检测国外某些国家或区域流行的EV71基因亚型,对引起我国手足口病流行的EV71 C4基因亚型不易检出。本研究从美国的NCBI基因库上下载了近20年来世界各地的肠道EV71毒株,对其进行了同源性比较,在EV71的VP1区设计若干对引物与TaqMan探针,对该区域进行特异性扩增,从中筛选出最佳的引物和探针,并对荧光RT-PCR方法进行优化,验证其敏感性、特异性和重复性。经肠道病毒标准株、分离株、EV71毒株与2008年上半年我国手足口病暴发疫情疑似患者临床样本的检测和比较,该方法具有高特异性,只能检出肠道病毒EV71型,与其他肠道病毒CA16、CA4、CA9、CA21、CA24v、E6、E30、CB3、CB5和Sabin Ⅰ等毒株均无交叉反应,而且比常规RT-PCR法更敏感、快速和简便。从病毒核酸提取至完成检测,仅需3~4 h左右,能同时对几十个样本进行高通量检测,敏感度达0.1 TCID50/mL,可直接从手足口病患者的疱疹液、脑脊液和粪便等临床样本中检测EV71核酸。该方法与肠道病毒荧光定量RT-PCR方法同时使用,两者检测结果可以相互验证,EV71核酸阳性的样本肠道病毒核酸也均阳性。用新建立的方法对2008年上半年浙江省疑似手足口病暴发疫情患者120份样本进行实验室快速诊断,均获得了令人满意的结果。
| [1] | Ho M, Chen ER, Hsu KH, et al. An epidemic of enterovirus 71 infection in Taiwan[J]. N Engl J Med, 1999, 341 : 929–935. DOI:10.1056/NEJM199909233411301 |
| [2] | 杨智宏, 朱启镕, 李秀珠, 等. 2002年上海儿童手足口病病例中肠道病毒71型和柯萨奇病毒A组16型的调查[J]. 中华儿科杂志, 2005, 43(9) : 648–652. |
| [3] | Singh S, Chow VTK, Phoon MC, et al. Direct detection of enterovirus 71 (EV71) in clinical specimens from a hand, foot and mouth disease outbreak in Singapore by reverse transcription-PCR with universal enterovirus and EV71-specific primers[J]. J Clin Microbiol, 2002, 40 : 2823–2827. DOI:10.1128/JCM.40.8.2823-2827.2002 |
| [4] | 严菊英, 卢亦愚, 徐昌平, 等. 肠道病毒TaqMan荧光定量RT-PCR法快速检测[J]. 中国公共卫生, 2007, 23(7) : 818–820. |
| [5] | 严菊英, 卢亦愚, 翁景清, 等. 3例SARS患者的RT-PCR与ELISA确认[J]. 中国人兽共患病杂志, 2004, 20(9) : 754–756. |
| [6] | Chen TC, Chen GW, Hsiung CA, et al. Combining multiplex reverse transcription-PCR and a diagnostic microarray to detect and differentiate enterovirus 71 and coxsackievirus A16[J]. J Clin Micro, 2006, 44 : 2212–2219. DOI:10.1128/JCM.02393-05 |
| [7] | Tan EL, Chow VTk, Quak SH, et al. Development of multiplex real-time hybridization probe reverse transcriptase polymerase chain reaction for specific detection and differentiation of Enterovirus 71 and Coxsackievius A16[J]. Diagn Microbiol Infect Dis, 2008, 61(3) : 294–301. DOI:10.1016/j.diagmicrobio.2008.02.009 |
| [8] | Tan EL, Yong LL, Quak SH, et al. Rapid detection of Enterovirus 71 by real-time TaqMan RT-PCR[J]. J Clin Virol, 2008, 42(2) : 203–06. DOI:10.1016/j.jcv.2008.01.001 |
 2009, Vol. 25
2009, Vol. 25