花色苷(Anthocyanin)是广泛存在于蔬菜、水果等植物中的一类水溶性天然色素。近20年来, 许多研究〔1-3〕证实, 花色苷具有抗氧化、抗炎及抗肿瘤等一系列生物学特性, 但其具体的分子机制及涉及的信号通路尚未完全明确。人白血病单核细胞株(THP-1)源性巨噬细胞是THP-1细胞株经诱导后形成的, 既保留了肿瘤细胞的一般特性, 又具有巨噬细胞介导炎症反应的功能。因此, 本研究拟通过信号转导通路发现者基因芯片观察花色苷作用THP-1源性巨噬细胞后基因表达谱的改变, 了解花色苷在抗炎、抗肿瘤作用中涉及的相关信号通路及可能的靶作用基因。
1 材料与方法 1.1 材料 1.1.1 主要仪器与试剂核酸分析仪(德国Beckman公司); HB-1000杂交炉(美国UVP公司); 梯度PCR仪(英国Hybaid公司); 凝胶成像分析系统(法国Vilber Lourmat公司)。矢车菊素-3-葡萄糖苷(C3G, 挪威Polypenol AS公司); 生物素标记dUTP (Biotin-16-dUTP, 瑞士Roche公司); 线性DNA扩增试剂盒、cDNA纯化试剂盒和信号转导通路发现者基因芯片(美国SuperArray Bioscience公司); RNA逆转录试剂盒(日本Toyobo公司); PCR试剂盒(大连TaKaRa公司)。
1.1.2 细胞THP-1细胞株(武汉大学中国细胞保藏中心)。
1.2 方法 1.2.1 细胞培养使用含10%胎牛血清的RPMI-1640培养基, 于37 ℃、5% CO2的培养箱中培养, 每2 d传代1次。细胞离心收集后, 将细胞密度调度整至4 × 106个/mL, 种至6孔板, 每孔重新加入含10%胎牛血清的RPMI-1640培养基2 mL, 加入佛波脂(phorbol-12-myristate-13-acetate, PMA), 使培养基中其终浓度达到167 nmol/L, 刺激48 h诱导成巨噬细胞, 磷酸盐缓冲液(PBS)冲洗3遍, 换新鲜培养基继续培养2 h, 实验组加入C3G, 使培养基中终浓度达到100 μmol/L; 溶剂对照组加入二甲基亚砜(DMSO), 使培养基中其终浓度达到0.1%(v:v), 12 h后收集对照组及实验细胞的总RNA。
1.2.2 芯片检测及分析每孔细胞加入1 mL Trizol试剂, 提取总RNA, 样品置于-80 ℃冰箱中保存待测, 样品的探针标记、纯化, 芯片的杂交和信号检测按照信号转导通路发现者基因芯片实验操作说明书进行, 最后进行芯片数据标准化处理分析, 差异基因筛选标准设定为实验组≥2为上调基因, 实验组/对照组≤0.5为下调基因。
1.2.3 逆转录-聚合酶链反应(reverse transcription-poly-merase chain reaction, RT-PCR)cDNA第1链的合成参照RNA逆转录试剂盒的说明书进行。诱导型一氧化氮合酶(NOS2A)、前列腺素内过氧化物合酶2(PTGS2)及看家基因3-磷酸甘油醛氢酶(G3PDH)的PCR扩增引物根据文献〔4, 5〕由上海生工生物工程公司合成。其序列为NOS2A: (F: 5′-ACAAGCCTACCCCTCCAGAT-3′, R: 5′-CTTGGATGGTTGACTGCCCT-3′); PTGS2: (F: 5′-GGGCAAAGACTGCGAAGAAG-3′, R: 5′-CCCATGTGACGAAATGACTG-3′); G3PDH: (F: 5′-ACCACAGTCCATGCCATCAC-3′, R: 5′-TCCACCACCCTGTTGCTGTA-3′)。PCR反应条件为: 94 ℃ 2 min, 94 ℃ 30 s, [57.8 ℃ 30 s (NOS2A); 60.8 ℃ 30 s (PTGS2); 60 ℃ 30 s (G3PDH)], 72 ℃ 1 min, 循环30次; 72 ℃ 10 min。取PCR产物于2%琼脂糖凝胶中电泳后凝胶像系统上观察、拍照, 最后以目的条带与G3PDH条带的亮度比值作为目的条带的含量值, 进行统计检验。
2 结果 2.1 基因芯片杂交结果及生物学分析芯片图像经扫描及统计分析后, 共检出花色苷C3G作用后表达上调的基因有5个, 包括TP53、核因子κB抑制因子α (NFκBIA)、alpha-2巨球蛋白(alpha-2 Macroglobulin, α2M)、视黄醇结合基因2(RBP2)及核受体相互作用蛋白1 (Nuclear receptor interacting protein 1, NRIP1);表达下调的基因有10个, 包括FBJ鼠科骨肉瘤病毒癌基因同源物(V-jun)、果蝇无翼基因同源物1(WNT1)、WNT1诱导信号通路相关蛋白3 (WNT1 inducible signaling pathway protein 3, WISP3)、鼠双微基因2(murine double mimute 2, mdm2)、NOS2A、PTGS2、端粒体反转录酶(TERT)、血管内皮细胞粘附分子1 (Vascular cell adhesion molecule 1, VCAM1)和趋化因子配体9 (chemokine ligand 9, CXCL9), 共涉及有丝分裂、WNT、p53、磷脂酶C、核因子κB (Nuclear factor κB, NFκB)、Janus激酶/信号转导和转录活化因子(JKA/STAT)和维甲酸7条信号转导通路。
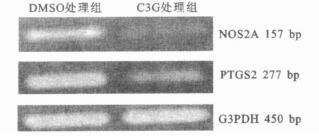
2.2 基因芯片分析结果的半定量RT-PCR验证(图 1)
|
图 1 C3G干预前后的NOS2A、PTGS2、G3PDH的mRNA电泳图 |
为验证基因芯片结果, 本研究采用半定量RT-PCR技术检测C3G干预前后THP-1源性巨噬细胞内NOS2A及PTGS2基因的mRNA水平。实验结果表明, 在C3G干预12 h后, THP-1源性巨噬细胞内NOS2A及PTGS2的mRNA表达水平分别比0.1%DMSO处理组(溶剂对照组)下调了58%及54%。
3 讨论本研究芯片结果及RT-PCR实验均显示, 花色苷干预后炎性因子NOS2A及PTGS2的mRNA表达水平下调, 说明花色苷具有抑制炎症的能力。但由于炎症反应是由各种炎症细胞及炎性因子所共同参与的, 涉及多条炎症相关信号通路, 而调控炎症反应的这些信号通路, 如有丝分裂、磷脂酶C、NFκB和LAK-STAT等, 存在着交汇作用, 相互影响〔6-7〕。所以, 花色苷作用的具体靶位点和信号转导通路还有待特异性的相关信号通路芯片的进一步检测。有研究认为, TP53是一种抑癌基因, 可以调节细胞周期/凋亡通路下游靶基因的表达; 而鼠双微基因2(mdm 2)蛋白是高度保守的原癌基因mdm 2的表达产物, 在细胞核内抑制p53介导的转录和凋亡活性, 从而促进了肿瘤的发生〔8〕。本次基因芯片的检测结果显示, C3G干预后, p53信号通路中TP53基因上调而mdm 2基因下调。因此, 推测p53信号通路可能是花色苷调节肿瘤免疫的重要信号通路之一。结果显示, C3G还可能通过提高维甲酸信号通路中抑癌基因RBP2及NRIP1的表达, 下调有丝分裂通路中的原癌基因V-fos、V-jun, NFκB通路中的端粒体反转录酶(TERT), Jak-Stat通路中的CXCL9, WNT通路中原癌基因WNT1及WISP3的表达, 发挥其抑制肿瘤发生的功能。
| [1] | 周波, 王晓红, 郭连营, 等. 玉米紫色植株花色苷色素抗脂质过氧化作用[J]. 中国公共卫生, 2008, 24(1) : 50–51. |
| [2] | Xia M, Ling W, Zhu H, et al. Anthocyanin prevents CD40-activated proinflammatory singaling in endothelial cells by regulating cholerol distribution[J]. Arrerioscler Thromb Vasc Biol, 2007, 27 : 519–524. DOI:10.1161/01.ATV.0000254672.04573.2d |
| [3] | Jing P, Bomser JA, Schwart SJ, et al. Structure-function relationships of anthocyanins from various anthocyanin-rich extracts on the inbition of colon cancer cell growth[J]. J Agric Food Chem, 2008, 56 : 9391–9398. DOI:10.1021/jf8005917 |
| [4] | Woo CW, Man RY, Siow YL, et al. Ganoderma lucidum inhibits inducible nitric oxide synthase expression in macrophages[J]. Mol Cell Biochem, 2005, 275 : 165–171. DOI:10.1007/s11010-005-1352-9 |
| [5] | Zhang WY, Liu HQ, Xie KQ, et al. Procyanidin dimer B2[epicate-chin-(4beta-8)-epicatechin] suppresses the expression of cyclooxygenase-2 in endotoxin-treated monocytic cells[J]. Biochem Biophye Res Commun, 2006, 345 : 508–515. DOI:10.1016/j.bbrc.2006.04.085 |
| [6] | Bubici C, Papa S, Dean K, et al. Mutual cross-talk between reactive oxygen species and nuclear factor-kappa B: molecular basis and biological significance[J]. Oncogene, 2006, 25 : 6731–6748. DOI:10.1038/sj.onc.1209936 |
| [7] | Maines MD. Biliverdin reductase: PKC interaction at the cross-talk of MAPK and PI3K signaling pathways[J]. Antioxid Redox Signal, 2007, 9 : 2187–2195. DOI:10.1089/ars.2007.1805 |
| [8] | Coates PJ. p53 and Mdm 2: not all cells are equal[J]. J Pathol, 2007, 213 : 357–359. DOI:10.1002/(ISSN)1096-9896 |
 2009, Vol. 25
2009, Vol. 25
