2. 福建农林大学动物科学院;
3. 辽宁出入境检验检疫局
霍乱是一种甲类烈性肠道传染病,也是当今3种国际检疫传染病中最严重的一种。霍乱弧菌是引起霍乱暴发流行的病原菌,根据O抗原的特异性可分为O1群、O139群和非O1/非O139群,其中O1群和O139群可引起霍乱流行,而非O1/非O139群的毒性不高,只是偶尔会引起腹泻等疾病,但在进出口食品中不允许被检出。霍乱弧菌胶原酶基因(vcc基因)是霍乱弧菌O1群、O139群和非O1/非O139群共有的,可用来鉴定是否为霍乱弧菌。霍乱弧菌O139群和O1群都含有毒力基因ctxA和tcpA,但O139群和O1群的毒力基因LPSgt存在差异,而非O1/非O139群不含有这些毒力基因〔1, 2〕。本研究分别合成扩增霍乱弧菌3个群的vcc基因、O1群和O139群的毒力基因(ctxA, tcpA基因)以及O139群的毒力基因(LPSgt基因)的特异引物,建立vcc, ctxA, tcpA和LPSgt 4种基因的多重PCR结合变性高效液相色谱(DHPLC)检测方法,在短时间内可对霍乱弧菌可疑纯培养物的鉴定并分型。现报告如下。
1 材料与方法 1.1 材料 1.1.1 菌株、DNAO139群霍乱弧菌(编号为VC29)、O1群霍乱弧菌(编号分别为VC20、VC22)(辽宁出入境检验检疫局); 非O1/非O139群霍乱弧菌(福建出入境检验检疫局技术中心); O139群、O1群霍乱弧菌的DNA (中国疾病预防控制中心传染病预防控制所)。
1.1.2 主要仪器与试剂变性高效液相色谱仪(WAVE4500, 美国Transgenomic公司)脱氧核苷三磷酸(dNTP)、DNA marker Ⅰ、2×Taq PCR MasterMix (厦门泰京公司); 组菌基因组DNA提取试剂盒(天根生化科技有限公司); 5×Buffer (含15 nmol/L MgCl2)、Go Taq DNA聚合酶(5 U/μl,美国Promega公司); Wave DNA sizing control (随DHPLC仪配置); 三乙胺乙酰盐(TEAA,美国Transgenomic公司); 乙腈(美国Fisher公司); 缓冲溶液A (0.1 mol/L TEAA); 缓冲溶液B (0.1 mol/L TEAA含体积浓度为25%的乙腈)。
1.1.3 引物参照文献〔1, 3〕,委托上海生工公司合成以下引物。vcc-F:5′-CCTAATGAGCAACCGACTATCAAAGA-3′, vccR:5′-TGTTCTGAAGCGGTGAGCCATAC-3′,扩增vcc基因,产物大小为155 bp,ctxA-F:5′-ACTCAGACGGGATTTGTTAGGC-3′, ctxA-R:5′-ATCTATCTCTGTAGCCCCTATTAC-3′, 扩增ctx基因,产物大小为304 bp; tepA-F:5′-TTGACCCAAGCACAATGTAAGAC-3′, tcpA-R:5′-CTACTGTGAATGGAGCAGTTCC-3′, 扩增tcpA基因,产物大小为241bp; LPSgt-F:5′-ACATCTGTAGGGATTGTATTGAC-3′,LPSgt-R:5′-ATAACAACTGAGATATCAAGCGTC-3′,扩增LPSgt基因,产物大小为340 bp。引物用TE溶液(10 mmol/L三羟甲基氨基甲烷·盐酸,1 mmol/L乙二胺四乙酸二钠,pH 8.0)稀释至浓度为10 μmol/L,-20 ℃保存备用。
1.2 方法 1.2.1 PCR退火温度的优化PCR反应体系为2×Taq PCR MasterMix 10 μl,引物各0.4 μl,O139群DNA模板50 ng,超纯水(ddH2O)补足至20 μl。PCR反应条件为:94 ℃预变性5 min; 94 ℃变性30 s,50~62 ℃退火30 s,72 ℃延伸30 s,40个循环; 72 ℃延伸5 min。反应结束后,取10 μl PCR产物,经22 mg/mL琼脂糖凝胶电泳分析。
1.2.2 霍乱弧菌多重PCR-DHPLC分型方法参照试剂盒法说明书提取细菌DNA,于核酸蛋白分析仪上测定其质量浓度。PCR反应体系为5×Buffer 6 μl, dNTP 1.2 μl, Go Taq DNA聚合酶0.7 μl,vcc-F, vcc-R各0.5 μl,ctxA-F, ctxA-R各0.6 μl,tcpA-F, tcpA-R各0.8 μl,LPSgt-F, LPSgt-R各1.21 μl,DNA模板50 ng,ddH2O补足至30 μl。反应结束后,取10 μl PCR产物22 mg/mL琼脂糖凝胶电泳分析。另取5 μl PCR产物进行DHPLC检测,洗脱液由缓冲液A (体积比为43.8%)和缓冲液B (体积比为56.2%)组成,以0.9 mL/min的流速在50 ℃下自动洗脱DNA分子,跑样时间为20 min,根据阳性峰出现的位置来判断PCR产物是否正确。
2 结果 2.1 PCR退火温度优化(图 1)
|
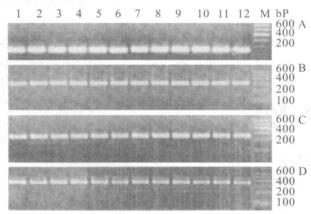
注:A:vcc基因; B:ctxA基因; C:tcpA基因; D:LPSgt基因; 1~12:退火温度分别为50.0,50.3,51.1,52.4,53.8,55.3,56.7,58.1,59.6,60.9,61.7,62 ℃; M:DNA Marker Ⅰ。 图 1 PCR退火温度的优化结果 |
vcc基因、ctxA基因和tcpA基因受退火温度的影响不大,各温度的产量较一致,而LPSgt基因受退火温度影响较大,除前4个温度的产量较高外,其他温度对应的PCR扩增量随着温度的升高而下降。本研究选用53 ℃作为4种基因同时扩增的退火温度。
2.2 霍乱弧菌多重PCR-DHLC分型方法的建立(图 2,3)
|
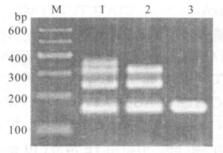
图 2 不同群霍乱弧菌多重PCR产物的电泳结果 |

|
图 3 不同群霍乱弧菌多重PCR产物的DHPLC检测结果 |
凝胶电泳结果表明,O139群扩增到155,240,304和340 bp共4个片段; O1群扩增互155,240和304 bp共3个片段; 而非O1/非O139群仅扩增到155 bp的片段。PCR产物的DHPLC也检测到相同的结果,即O139群出现相应的4个特异峰,O1群出现3个相应的特异峰,非O1/非O139群仅出现霍乱弧菌共有的1个特异峰。
2.3 霍乱弧菌多重PCR-DHLPC分型法的实际应用用建立的霍乱弧菌多重PCR-DHPLC分型方法对辽宁出入境检验检疫局的3个菌株进行了鉴定。编号为VC20、VC22出现了分别与155,240,304 bp片段相吻合的3个峰,可判定为O1群霍乱弧菌; 而编号为VC29的菌株出现了分别与155, 240, 304和340 bp片段相吻合的4个峰,可判定为O139群。多重PCR-DHPLC分型结果与辽宁出入境检验检疫局用传统血清学鉴定结果完全一致。
3 讨论PCR在霍乱弧菌的检测、分型方面的研究已有一些文献报道〔1, 3-9〕,但均采用荧光PCR、PCR或多重PCR-凝胶电泳的方法。本研究针对所选基因,对PCR反应条件进行了优化,并经过多次重复实验优化多重PCR反应体系,使4个基因的扩增产物均能同时达到相近而且较高的扩增效率,应用DHPLC方法来检测多重PCR产物,省去了繁琐的电泳过程,有较好的特异性,检测鉴定结果与预期的完全一致,也与徐晓静等〔1〕报道的结果一致。多重PCR-DHPLC分型方法能在很短的时间内完成对霍乱弧菌可疑纯培养物的鉴定并分型,比常规方法更快速、简便、经济实用,具有较高的应用价值和广泛的应用前景。
| [1] | 徐晓静, 文思远, 陈苏红, 等. 应用多重PCR方法检测霍乱弧菌O139[J]. 黑龙江畜牧兽医, 2006(3) : 74–75. |
| [2] | 毕振强, 赵仲堂. 霍乱弧菌致病因子及调控基因研究进展[J]. 中国公共卫生, 2005, 21(6) : 754–755. |
| [3] | 吕海沧.食品中五种主要的致病性弧菌的PCR检测方法研究[D].福州:福建农林大学, 2007. |
| [4] | Lyon WJ. TaqMan PCR for detection of Vibrio cholerae O1, O139, non-O139, non-O1, and non-O139 in pure cultures, raw oysters, and synthetic seawater[J]. Appl Environ Microbiol, 2001, 67(10) : 4685–4693. DOI:10.1128/AEM.67.10.4685-4693.2001 |
| [5] | Singh DV, Matte MH, Matte GR, et al. Molecular analysis of Vibrio cholerae O1, O139, non-O1, and non-O139 strains:clonal relationships between clinical and environmental isolates[J]. Appl Environ Microbiol, 2001, 67(2) : 910–921. DOI:10.1128/AEM.67.2.910-921.2001 |
| [6] | 芮勇宇, 蔡初的, 俞守义, 等. 3组套式PCR用于检测及区分霍乱弧菌O1群古典型、埃尔托型和O139群[J]. 中国公共卫生, 1999, 15(8) : 733–734. |
| [7] | 井良义, 陈锦英, 王书梅, 等. 多重PCR检测霍乱弧菌的毒素相关基因[J]. 环境与健康杂志, 2003, 20(6) : 361–363. |
| [8] | 黄晓蓉, 吕海沧, 郑晶, 等. 多重PCR方法检测霍乱弧菌的研究[J]. 微生物学杂志, 2006, 26(5) : 15–17. |
| [9] | 石磊, 曾冰冰, 曹以诚, 等. 霍乱弧菌O1群和O139群基因分型方法[J]. 食品与机械, 2007, 23(3) : 132–134. |
 2009, Vol. 25
2009, Vol. 25
