2. 南京军区军事医学研究所
猪链球菌(Streptococcus suis,S.suis)感染可引起猪脑膜炎、关节炎、浆膜炎、心内膜炎、败血症等疾病,长期以来被认为是世界范围内养猪业的重要问题〔1〕。近年来, S.suis感染人并导致严重致病的情况也有发生。尤其是1998年在江苏省和2005年在四川省暴发的猪链球菌2型(S.suis 2)大规模流行感染猪和人的疫情,导致了严重的公共卫生事件〔1, 2〕。迄今为止,能够安全有效地用于预防和治疗猪链球菌感染的疫苗和药物尚未问世。研究发现,肺炎链球菌和化脓链球菌的组氨酸三聚体蛋白(Histidine Triad Protein,HTP)是良好的免疫保护性抗原,可以作为候选的保护性疫苗〔3, 4〕。通过对本实验室保存的S.suis 2型中国强毒株05ZYH33的全基因组序列分析发现该菌株也存在编码HTP的基因,并对其进行了表达纯化,得到纯度较高的重组蛋白,为进一步开发有效的疫苗提供了基础依据。现将结果报告如下。
1 材料与方法 1.1 材料(1)菌株与质粒:菌株05ZYH33,分离自四川省资阳市S.suis 2感染中毒性休克综合征患者(本实验室保存); 表达载体pET28a (美国Novagen公司)及其宿主菌大肠埃希菌(Escherichia coli,E.coli) DH5α和BL21(本实验室保存); 克隆载体pEASY-T1(北京全式金生物技术有限公司)。(2)试剂:PCR扩增试剂盒,DNA胶回收试剂盒,限制性内切酶BamH I和Sal I,T4连接酶(日本TaKaRa公司); DNA Marker和蛋白Marker (立陶宛Fermentas公司); 四甲基联苯胺(TMB)显色液(美国Promega公司); 兔抗05ZYH33抗血清(本实验室制备); 氨苄青霉素(Ampicillin)和卡那霉素(Kanamycin)(上海生物工程有限公司); 其他试剂均为国产分析纯。(3)肉汤培养基(LB培养基),Ampicillin -LB培养基(Ampicillin终浓度100 μg/ml),Kanamycin-LB培养基(Kanamycin终浓度50 μg/ml)。
1.2 方法 1.2.1 05ZYH33全基因序列中htp基因筛选利用Blast软件和ClustalW软件等生物信息学工具筛选本实验室S. suis 2 05ZYH33全基因组序列中可能的HTP编码序列,并将其与已知HTP编码序列进行同源性分析。
1.2.2 PCR扩增htp基因根据筛选所得序列设计合成引物,进行PCR扩增。上游引物为5′-CCCGGATCCGCTGAACAATTAACACCTGA-3′, 划线部分为BamH I酶切位点; 下游引物为5′-CCCGTCGACGATGGTGTATTTGGGTGTAA-3′, 划线部分为Sal I酶切位点。引物由南京赛百胜生物公司合成。PCR程序为95 ℃ 5 min; 95 ℃ 30 s; 60 ℃ 30 s; 72 ℃ 1 min, 共25个循环,最后72 ℃延伸10 min。
1.2.3 目的片段克隆测序PCR产物经1%琼脂糖凝胶电泳,用胶回收试剂盒回收目的片段。将此目的片段与pEASY-T1连接,转化至DH5α感受态细菌,菌液经PCR检测为阳性者用试剂盒提取质粒、酶切并电泳进行鉴定。
1.2.4 重组表达载体pET28a::htp构建和鉴定质粒pEASY-T1::htp和pET28a载体分别用BamH I/Sal I双酶切,并用胶回收试剂盒回收。T4连接酶连接后转化DH5α感受态,菌液经PCR检测为阳性者用试剂盒提取质粒,酶切,电泳鉴定。结果为阳性者由上海英俊生物技术有限公司进行测序,对测定结果进行分析。
1.2.5 HTP的表达及其产物纯化将重组表达载体转化E.coli BL21,经异丙基-β-D-硫代乳糖苷(IPTG)诱导表达4 h,收集菌体超声破碎。离心后取上清进行十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE),明确是否有目的蛋白表达。将重组菌扩大培养并经IPTG诱导表达,超声裂解,离心后的上清用Ni2+亲和层析柱纯化融合蛋白,12% SDS-PAGE电泳鉴定目的蛋白分子量。
1.2.6 HTP免疫原性分析采用电转印法将12%SDS-PAGE电泳后胶上的蛋白转移至硝酸纤维素膜上,5%脱脂奶37 ℃封闭1 h,加兔抗05ZYH33抗血清(1:100稀释),4 ℃孵育过夜,二抗为HRP标记的山羊抗兔IgG (1:1000稀释),37 ℃孵育1 h,之后用3′, 3′, 5′, 5′, -四甲基联苯胺(TMB)显色液显色, 采用蛋白印迹法(Western blot)检验其免疫原性。
2 结果 2.1 05ZYH33全基因组中编码HTP的基因通过与Genbank中已知的蛋白序列进行同源性分析发现,四川分离株05ZYH33全基因组中的开放阅读框CDSSSU0332编码一个HTP近似序列。利用ClustalW软件将05ZYH33的HTP序列与已经被证明为较好的免疫保护性抗原的HTP (肺炎链球菌HTP和化脓链球菌HTP)序列进行同源比对,结果表明,它们的同源性较高,尤其是HxxHxH结构域更为保守。从比对结果可见,不同链球菌中HTP序列N端的同源性要高于C端,而且HxxHxH结构域在N端出现的频率也要高于C端。比对结果表明, 05ZYH33基因组中也存在一个由开放阅读框CDSSSU0332编码的htp基因。
2.2 05ZYH33中HTP的进化树分析通过比对发现,05ZYH33的HTP氨基酸序列与Genbank上的肺炎链球菌HTP (accession no. YP_816370)氨基酸序列相似性为74%,与化脓链球菌HTP的氨基酸序列(accession no. YP_599388)和无乳链球菌HTP的氨基酸序列(accession no. YP_330492)相似性均为57%。而从ClustalW软件生成的进化树中可以看出,S.suis 2 05ZYH33的HTP与化脓链球菌和马链球菌的HTP亲缘关系最近。
2.3 目的基因扩增(图 1)
|
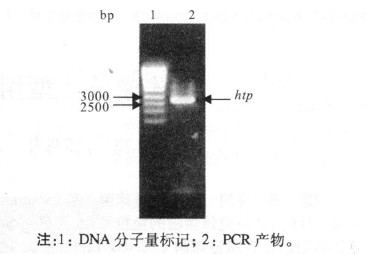
图 1 PCR扩增效果 |
以05ZYH33染色体DNA为模板,对目的基因(htp)进行PCR扩增,产物进行琼脂糖凝胶电泳检测。图 1可见,PCR扩增产物分子量约为2.7 Kb,大小与htp基因的大小(2727 bp)基本相符。
2.4 重组表达载体pET28a::htp鉴定(图 2)
|
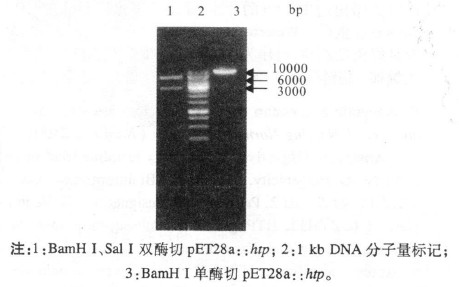
图 2 重组质粒pET28a::htp双酶切鉴定 |
重组表达载体pET28a::htp通过BamH I/Sal I双酶切后,1%琼脂糖电泳显示,05ZYH33中htp片段的长度约2700 bp,序列测定显示该片段全长2727 bp,编码909个氨基酸。
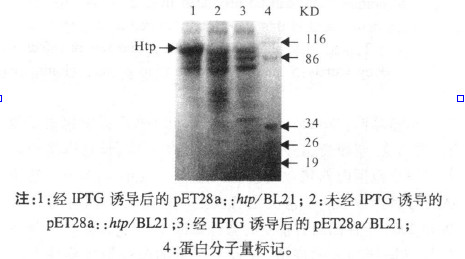
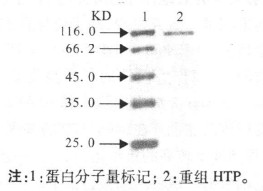
2.5 重组蛋白的表达及纯化含重组表达质粒pET28a::htp的E.coli BL21,经IPTG诱导后,SDS-PAGE分析表明,在约110 KD处有1条明显的新生蛋白条带(图 3),分子量大小与预期一致。利用His-Resin对表达产物进行纯化,纯化后的表达产物只有1条特异的条带(图 4)。
|
图 3 SDS-PAGE检测蛋白表达 |
|
图 4 纯化后的HTP蛋白电泳图谱 |
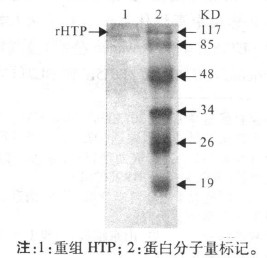
2.6 HTP的免疫原性(图 5)
Wesern blot检测结果显示,HTP蛋白可以与兔抗05ZYH 33全菌抗血清反应, 在特定位置处有明显条带, 表明重组HTP蛋白具有特异性抗原活性。
|
图 5 HTP的Wesern blot检测 |
3 讨论
S.suis 2感染能够导致多种疾病,近年来给养猪业造成了极大的危害,同时也给相关从业人员的身体健康和生命安全带来了严重威胁〔5〕。到目前为止,对S.suis 2型的致病机制及毒力因子调控都取得了重要进展〔6〕,但对S.suis 2型表面蛋白的研究十分有限,这在一定程度上延长了疫苗的研究周期。由于细菌的表面蛋白、分泌蛋白和毒力因子等容易接触宿主的免疫系统,被免疫活性细胞识别,从而刺激免疫应答的产生,因此,被认为是研究保护性疫苗的重要靶点。本课题组对S.suis 2 05ZYH33株全基因组测序和功能注释为S.suis 2疫苗研究提供了基础依据〔7〕。本研究通过对S.suis 2型05ZYH33全基因组进行分析,发现了HTP编码基因。系统进化分析表明,S.suis 2的HTP与一些同样能引起心内膜炎、关节炎、肺炎、败血症以及人链球菌中毒性休克综合征(STSS)细菌的HTP高度同源,提示其在进化中高度保守。本实验成功地表达和纯化了猪链球菌重组HTP,并利用兔抗05ZYH33全菌抗血清证明其具有良好的免疫原性,显示HTP是一种良好的猪链球菌保护性疫苗候选分子。S.suis 2型HTP的成功表达与免疫原性鉴定为猪链球菌感染预防提供了新的手段。
| [1] | Tang J, Wang C, Feng Y, et al. Streptococcal toxic shock syndrome caused by Streptococcus suis serotype 2[J]. PLoS Med, 2006, 3(5) : e151. DOI:10.1371/journal.pmed.0030151 |
| [2] | Lun Z, Wang Q, Chen X, et al. Streptococcus suis:an emerging zoonotic pathogen[J]. Lancet Infect Dis, 2007, 7(3) : 201–209. DOI:10.1016/S1473-3099(07)70001-4 |
| [3] | Adamou JE, Heinrichs JH, Erwin AL, et al. Identification and characterization of a novel family of pneumococcal proteins that are protective against sepsis[J]. Infect Immun, 2001, 69 : 949–958. DOI:10.1128/IAI.69.2.949-958.2001 |
| [4] | Kunitomo EY, Terao S, Okamoto T, et al. Molecular and biological characterization of histidine triad protein in group A streptococci[J]. Microbes Infection, 2008, 10 : 414–423. DOI:10.1016/j.micinf.2008.01.003 |
| [5] | 呼显生, 彭召玲, 李静姬, 等. 1株猪源链球菌的分离鉴定及药敏实验[J]. 中国公共卫生, 2006, 22(10) : 1247–1248. |
| [6] | Pan X, Ge J, Li M, et al. The orphan response regulator CovR:a globally negative modulator of virulence in Streptococcus suis serotype 2[J]. J Bacteriol, 2009. |
| [7] | Chen C, Tang J, Dong W, et al. A Glimpse of streptococcal toxic shock syndrome from comparative genomics of S.suis 2 Chinese isolates[J]. PLoS ONE, 2007, 2(3) : e315. DOI:10.1371/journal.pone.0000315 |
 2009, Vol. 25
2009, Vol. 25

 , 唐家琪2
, 唐家琪2