2. 山东省寄生虫病防治研究所;
3. 美国康乃尔大学
结核病是由结核杆菌感染所致的慢性传染病。现有使用的预防结核的卡介苗保护作用不稳定。所以寻找既可作为抗结核的疫苗, 又可作为抗结核药靶的候选分子是研究的热点。基因组分析发现, 结核杆菌含有磷酸烯醇型丙酮酸羧基酶基因。在很多微生物中, 磷酸烯醇型丙酮酸羧基酶(PEPCK)催化草酰乙酸和磷酸烯醇型丙酮酸之间的可逆性反应。所以, PEPCK在结核致病和诱导机体免疫中可能起重要作用。本研究在大肠埃希菌(E. coli HB 101)中表达了结核杆菌PEP-CK, 并用其免疫小鼠, 观察其刺激小鼠产生的免疫反应, 研究其免疫原性, 为寻找更好的抗结核疫苗成分提供参考依据。
1 材料与方法 1.1 材料带有pckA基因片断的重组质粒pHF /pckA (美国康耐尔大学); 大肠埃希菌HB101 (中国科学院微生物研究所); 18~22 g清洁级纯种BALA /C小鼠(山东大学医学院实验动物中心), 6~8周龄。
1.2 主要试剂及仪器日常型质粒DNA小量快速制备试剂盒(杭州V-gene公司); 镍金属螯合亲和层析(BBST NTA Resin)蛋白质纯化试剂盒(上海博彩生物公司); 还原型谷胱甘肽、氧化型谷胱甘肽等(华美生物工程公司); 弗氏不完全佐剂、卡介苗(BCG)免疫鼠血清均为本实验室配制; 小牛血清(BSA) (上海复旦天呈公司); 碱性磷酸酶(AP)标记的羊抗鼠IgG结合物, 碱性磷酸酶(AP)标记的大鼠抗小鼠γ干扰素(IFN-γ)、白介素12(IL-12)和α肿瘤坏死因子(TNF-α)单抗及兔抗大鼠IgG结合物(美国Sigma公司); 辣根过氧化物酶(HRP)标记的羊抗鼠IgG结合物、4-氯萘酚(北京中山生物技术有限公司); 异硫氰酸荧光素(FITC)标记的小鼠IgG 2a、藻红蛋白(PE)标记的IgG 2a及两者的同型对照(美国BD公司); FC500型流式细胞仪(美国BECKMAN-COULTER公司)。
1.3 实验方法 1.3.1 PEPCK蛋白在大肠埃希菌HB101中的表达将重组质粒pHF /pckA转化大肠埃希菌HB101, 于含氨苄青霉素的固体琼脂培养板上培养, 挑取阳性克隆, 按1: 50的比例接种于含氨苄青霉素的液体琼脂培养基中, 37 ℃摇菌, 加入异丙基-β -D-硫代半乳糖苷(IPTG), 终浓度为1 mm ol/L, 继续摇菌5 h。收集菌液, 8 000 r/min离心5 min, 在沉淀中加入适量的磷酸盐缓冲液(PBS)和等量的3 ×电泳上样缓冲液, 剧烈震荡, 沸水浴, 12 000 r /min离心5 min, 取上清进行聚丙烯酰胺凝胶电泳(SDS-PAGE)分析。
1.3.2 表达产物的纯化和复性收集异丙基-β-D-硫代半乳糖苷(IPTG)诱导表达的转化菌, 按BBST NAT R esin蛋白质纯化试剂盒说明在非变形条件下纯化重组的融合蛋白, 将纯化好的蛋白质装入透析袋, 复性液(含有pH 8.3 20 mmo l Tris-HCL, 1 mmol乙二胺四乙酸, 2 mmol还原型谷胱甘肽, 0.2 mmol氧化型谷胱甘肽)中4 ℃, 24 h, 然后用聚乙二醇(PEG2000)进行浓缩, 用紫外线分光光度仪(UV3000)测定蛋白质含量。
1.3.3 蛋白印迹分析(Western blot)表达产物和从卡介苗中提取的蛋白经SDS-PAGE电泳后转移至硝酸纤维素膜上, 加小牛血清封闭, 室温摇床振摇3 h, 磷酸盐缓冲液漂洗3次, 加入卡介苗免疫的小鼠血清(1: 50), 室温振摇2 h, 冲冼3次, 加入1 : 5 000羊抗鼠抗体, 室温摇2 h, 加入4-氯萘酚, 37 ℃显色。
1.3.4 免疫接种选BALB/c小鼠60只, 雌雄各半, 分为实验组和对照组。实验组每只小鼠腹腔注射表达的重组蛋白PEPCK 10 μg, 加相同体积的弗氏不完全佐剂; 对照组小鼠仅腹腔注射相同量的弗氏不完全佐剂, 隔2周免疫1次, 共免疫3次。
1.3.5 收集、检测T淋巴细胞末次免疫接种2周后, 各组剖杀部分小鼠, 收集血清, 无菌取脾, 制备淋巴细胞悬液。将淋巴细胞悬液浓度调节至5 × 10 6 /ml检测CD4+的单抗为异硫氰酸荧光素(FITC)标记的小鼠IgG 2a, 测CD8+的单抗为藻红蛋白(PE)标记的IgG 2a, 两者配以同型对照, 用流式细胞仪测定。
1.3.6 细胞因子的检测末次免疫2周后杀死部分小鼠, 用收集到的血清作为抗原, 按1 : 64包被ELISA反应板; 抗IFN -γ、IL-12和TNF-α的大鼠抗小鼠单克隆抗体(McAb)(1:3 000)为一抗, 兔抗大鼠IgG-AP结合物(1:2 500)为二抗, 对硝基苯基磷酸钠(pNPP)底物显色, 测吸光度(A 405)值, 实验组A值/阴性对照组A值> 2.1为阳性, 并计算各细胞因子的平均几何滴度。
1.4 统计分析采用SPSS 10.0统计软件进行分析。
2 结果 2.1 PEPCK融合蛋白的表达(图 1)
|
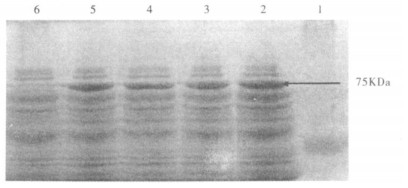
注: 1:标准分子量; 2, 3, 4, 5:表达出的PEPCK重组蛋白; 6:正常大肠埃希菌对照。 图 1 PEPCK融合蛋白表达的SDS-PAGE分析 |
将重组克隆转化大肠埃希菌HB 101, 通过IPTG诱导, 进行SDS-PAGE分析, 发现此克隆表达出72 KDa的蛋白, 与理论预测的PEPCK分子量大小一致, 未转化的大肠埃希菌没有此蛋白的表达。
2.2 重组蛋白的Western blot分析(图 2)
|
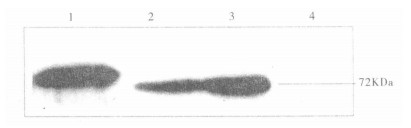
注: 1:表达的重组蛋白; 2, 3:卡介苗中提取的PEPCK蛋白; 4:正常大肠埃希菌对照。 图 2 纯化重组融合PEPCK的Western blot分析 |
纯化的重组蛋白经Western blot分析, 能够被卡介苗免疫的鼠血清识别; 由于组氨酸尾(His Tag Protein)的存在, 表达的重组蛋白略>72 KDa。
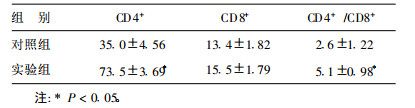
2.3 PEPCK免疫对小鼠脾脏形态的影响(表 1)| 表 1 不同组别小鼠脾脏淋巴细胞检测结果(x±s) |
PEPCK免疫小鼠后, PEPCK实验组小鼠的脾脏胀大, 明显大于对照组小鼠的脾脏, 在剥离时发现粘连也较严重。
2.4 PEPCK对T淋巴细胞的影响用PEPCK免疫小鼠3周后取小鼠脾脏, 用流式细胞仪检测T细胞, PEPCK实验组CD4+ /CD8+比值明显高于对照组(P < 0.05)。PEPCK实验组CD4+细胞明显高于对照组(P < 0.05)。2组CD8+ T细胞差异无统计学意义(P > 0.05)。
2.5 PEPCK对细胞因子产生的影响末次免疫2周后取小鼠血清, ELL SA法检测细胞因子, 单因素方差分析显示, 实验组和对照组的细胞因子差异有统计学意义, 实验组IFN-γ平均几何滴度可达46.0, 而对照组只有7.5(P < 0.05);实验组IL-12平均几何滴度可达36.0, 对照组只有5.0 (P < 0. 05)。实验组TNF-α平均几何滴度可达52.4, 明显高于对照组5.3(P < 0.05)。
3 讨论多种结核杆菌蛋白已经被克隆表达, 对结核杆菌PEPCK的表达报道较少。PEPCK在从原核生物到脊椎动物中都是一个非常关键的酶〔1〕, 催化磷酸烯醇型丙酮酸(PEP)和草酰乙酸(OAA)之间的可逆性反应。本研究在大肠埃希菌HB101中表达了重组蛋白PEPCK。SDS-PAGE检测可见, 表达出一分子量约为72 KDa的条带, 与理论预测的分子量一致, 且表达的蛋白为可溶性, 便于纯化。本实验中, 将表达的PEPCK复性〔2〕, Western blot证明, 复性后的PEPCK能够被小鼠抗卡介苗血清识别, 具有活性。
本实验中用PEPCK免疫小鼠后, 实验组小鼠的CD4+ T细胞、CD4+ /CD8+均明显高于对照组小鼠, 即PEPCK能够刺激CD4+ T细胞增多、活化。CD4+ T细胞是介导细胞免疫反应的主要的细胞, 也被认为是抗结核杆菌感染的主要细胞〔3〕, CD4+ T细胞的增多表明细胞免疫的增强, 对结核杆菌的杀伤作用增强。PEPCK引起机体产生免疫反应的另一个表现是刺激机体产生保护性细胞因子。本研究中实验组小鼠体内产生的IFN-γ、IL-12、TNF-α明显高于对照组。这些细胞因子在抗结核的免疫反应中起重要作用〔4-8〕。实验组小鼠脾脏增大, 明显大于对照组, 而且与周围组织粘连严重。由此可见, PEPCK不仅引起机体产生细胞免疫反应, 也引起体液免疫反应。
实验表明, 结核杆菌PEPCK可以有效的刺激机体产生细胞免疫反应和体液免疫反应, 是很好的抗结核疫苗候选分子之一。
| [1] | Swaninathan S, Gong J, Zhang M, et al. Cytokine production in children with tubercu losis infection and disease[J]. Clin Infect Dis, 1999, 28(6) : 1290–1293. DOI:10.1086/cid.1999.28.issue-6 |
| [2] | De la Barrera S, Aleman M, Musella R, et al. IL-10 down regulate costimulatory molecule on Mycobacterium tuberculos is pulsed m acrophages and impair the lytic activity of CD4 and CD8 CTLin tuberculos is patients[J]. Clin Exp Immunol, 2004, 138(1) : 128–138. DOI:10.1111/cei.2004.138.issue-1 |
| [3] | Collins D M. New tuberculosis vaccines basesd on attenuated strains of the Mycobacteriumtubercu losis complex[J]. Immunol Cell Biol, 2000, 78(4) : 342–348. DOI:10.1046/j.1440-1711.2000.00937.x |
| [4] | Chen J, Dong D, Yang Y. The effect of interleukin-12 on the production of Th1(1) and Th (2) cytokines by peripheral blood mononuclear cells from patierts with tuberculosis[J]. Zhonghua Jie He Hu Xi Za Zhi, 2002, 25(5) : 292–295. |
| [5] | Hwang SA, Kruzel ML, Actor JK. Lactoferrin augements BCG vaccine efficacy to generate Thelper response and subsequent protection against challenge with virulent Mycobacteriumtubercu losis[J]. Int Immunopharmacol, 2005, 5(3) : 591–599. DOI:10.1016/j.intimp.2004.11.006 |
| [6] | Feng CG, Jankovic D, Kullberg M. Maintenance of pumlonary Th1 effector function in chronic tub erculos is requires persistent IL-12 production[J]. JmImunol, 2005, 174(7) : 4185–4192. DOI:10.4049/jimmunol.174.7.4185 |
| [7] | Lasco TM, Yamamoto T, Yoshmiura T. Effect of Mycobacteriumbovis BCG vaccination on Mycobacteriumspecific celluar proliferation and tumor necros is factor alpha production from distinct guinea pig leukocyte population[J]. Infect Immun, 2003, 71(12) : 7035–7042. DOI:10.1128/IAI.71.12.7035-7042.2003 |
| [8] | Saunders BM, Briscoe H, BrittonW J. T cell derived tumour necrodid factor is essential, but not sufficient, for protection against Mycobacterium tuberculosis infection[J]. Clin Exp Immunol, 2004, 137(2) : 279–287. DOI:10.1111/cei.2004.137.issue-2 |
 2009, Vol. 25
2009, Vol. 25