虾类食品营养丰富, 但同时也是高致敏性食物之一,可引起各种速发型超敏反应症状, 如荨麻疹、风疹、喉痉挛、哮喘等甚至可能危及生命〔1〕。口虾蛄(squilla oratoria)是我国南北沿海常见的水产品,喜栖于浅水泥沙或礁石裂缝内。研究表明,口虾蛄是我国常见的食物性致敏原之一, 其主要变应原为原肌球蛋白(tropomyosin)〔2〕。为了探讨口虾蛄过敏原诊断和抗原标准化,本研究对其原肌球蛋白(tropomyosin)基因进行了克隆表达及变应原性鉴定。结果报告如下。
1 材料与方法 1.1 材料口虾蛄(深圳市南山市场); 质粒菌株:pMD 18-T载体(大连TaKaRa公司),pET-28 a (+)载体(美国Novagen公司); 大肠埃希菌E.coli Top10、E.coliBL21(DE3)(本实验室保存); 大肠埃希菌使用脂质双层(LB)培养基,37℃振荡培养; 核酸电泳DNA Marker、T4 DNA连接酶、NdeI和HindⅢ内切酶(大连TaKaRa公司); RNase A、溶菌酶(上海生工公司); Taq DNA聚合酶、蛋白电泳Protein Marker和预染Protein Marker (美国MBI Fermentas公司); RNA提取试剂盒(德国Qiagen公司); AMV First Strand cDNA Synthesis Kit (美国BBI公司); OMEGA Plasmid Mini kitⅠ(100)、OMEGA Gel Extraction kit (50)(美国OMEGA公司); 其他试剂均为分析纯为本实验室配置。
1.2 方法 1.2.1 简并引物设计从SWISS-PROT和TrEMBL (www.expasy.org)以及NCBI (www.ncbi.nlm.nih.gov)的数据库下载到15个动物性过敏原原肌球蛋白核酸序列。利用ClustalW程序确定其保守区域。根据这些保守区域的序列,设计简并引物, 并由上海生工公司合成:Trop5a:5′-ATG GA (C/G) GC (C/A) ATC AAG AAG AAG ATG C-3′; Trop3b:5′-TTA (G/A) TA GCC AG (T/A)(C/A) A GTT CGC-3′。
1.2.2 原肌球蛋白泛变应原基因RT-PCR扩增、克隆与序列分析取新鲜口虾蛄肉少许液氮研磨后用Qiagen公司试剂盒进行总RNA的提取。RT-PCR的逆转录反应采用上述简并引物Trop5a和Trop3b,后继PCR反应通过特异性PCR引物并引入NdeI和HindⅢ酶切位点,引物序列如下:lnxs1:5′-GAACATATGATGGAGGCCATCAAGAAGA-3′(含NdeⅠ位点); lnxx2:5′-GAAAAGCTTTTAGTAGCCAGACAGTTCGC-3′(含HindⅢ位点和终止密码),PCR反应程序为:95 ℃ 3 min后用降落(Touchdown) PCR方式进行扩增,第1个循环为94 ℃ 30 s,65 ℃ 30s,72 ℃ 5 min,此后每个循环退火温度下降1 ℃,当退火温度下降到57 ℃时,则以94 ℃ 30 s,57 ℃ 30 s,72 ℃ 5 min运行30个循环,再于72 ℃延伸10 min结束。电泳检测PCR产物,并切胶回收克隆到pMD-18T载体,挑取阳性菌落进行DNA测序。将测序所得序列通过美国国立生物技术信息中心(NCBI)中的局部对比基本检索工具(BLAST)进行序列比对,分析其序列同源性。
1.2.3 构建重组表达质粒将测序后的tropomyosin目的基因与原核表达载体pET-28a分别用NdeⅠ和HindⅢ酶切后相互连接,具体反应条件参照产品说明书。通过含氨苄青霉素(Amp)的LB平板进行抗氨苄筛选, 挑取单菌落LB/Amp培养, 碱裂解法提取质粒,并用NdeⅠ和HindⅢ酶切鉴定。测定该重组质粒DNA序列由上海生工生物工程有限公司完成。
1.2.4 pET-28-Tropomyosin/E.coli BL21(DE3)诱导表达将含有目的基因的重组子转化感受态大肠埃希菌E.coli BL21(DE3)中,待细菌生长处于对数生长期(A600nm=0.6~0.8)时, 加入终浓度为1 mmol/L的异丙基-B-D-硫代乳糖苷(IPTG), 诱导蛋白表达。5 h后取1 ml菌液,4 ℃下离心弃去上清液, 沉淀重悬于50 μl 1×PBS,取10 μl与等量2×十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)上样缓冲液混合,煮沸5 min,取8 μl上样进行电泳检测目的基因表达情况。在上述表达产物中,加入溶菌酶至终浓度为0.5 mg/ml,室温放置30 min并反复冻融数次后, 加DNaseI至终浓度为20 g/ml, 室温放置30 min, 离心后分别取上清液与沉淀进行SDS-PAGE分析。
1.2.5 原肌球蛋白的分离纯化大肠埃希菌中表达的原肌球蛋白以包涵体形式存在于细胞中,将分离的包涵体进行洗涤、纯化和复性,参照文献〔3〕操作。
1.2.6 原肌球蛋白变应原活性测定将纯化复性后的原肌球蛋白进行SDS-PAGE,再转移到硝酸纤维膜上,转移条件为350 mA,70 min,用对虾过敏的患者血清做一抗,同时用无过敏史的健康人血清做阴性对照,参照文献〔4〕方法进行免疫印迹(Western-blot)检测。
2 结果 2.1 原肌球蛋白基因的克隆与测序(图 1)
|
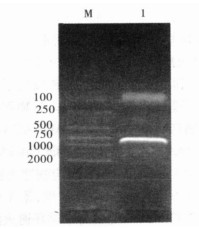
注:M:DNA分子量标准; 1:Tropomyosin基因RT-PCR扩增产物。 图 1 RT-PCR扩增结果 |
扩增的原肌球蛋白基因片段电泳显示约850bp的电泳条带。回收RT-PCR产物并于pMD-18T载体连接后转化E.coli Top 10。挑取4个阳性菌落进行测序,其中4个测序结果完全相同,表明LA-Taq进行PCR扩增时有一定校正能力。该序列已登录GenBank (登录号为EF 584510)。通过与GenBank数据库比对,该序列与GenBank登录号MEU08008(刀额新对虾)、AF034954(缅因龙虾)、AY827100(草虾)、DQ151457(褐美对虾)报道的序列同源性达到95%左右。
2.2 表达质粒构建pET-28-Tropomyosin重组质粒用NdeI和HindⅢ双酶切后,电泳显示出约850 bp的条带,表明目的基因成功地亚克隆到表达载体pET-28a (+)。再经DNA测序表明,亚克隆序列正确。
2.3 原肌球蛋白表达与纯化(图 2)
|
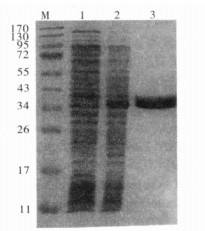
注:M:蛋白质分子量标准; 1:诱导前; 2:诱导后; 3:Ni2+亲和层析纯化后。 图 2 口虾蛄tropomyosin重组蛋白在大肠埃希菌中的诱导表达及纯化 |
工程菌经1 mmol/L IPTG诱导, 进行SDS-PAGE电泳,可见36 kDa左右的诱导条带明显。经鉴定tropomyosin基因以包涵体形式表达。重组蛋白经过Ni2+亲和层析纯化时检测280nm蛋白紫外吸收峰,洗脱时可观察到一尖锐的峰型出现,收集此峰进行SDS-PAGE电泳检测,可见单一的36kDa蛋白条带,说明目的蛋白主要集中在此峰。
2.4 原肌球蛋白变应原活性测定(图 3)
|
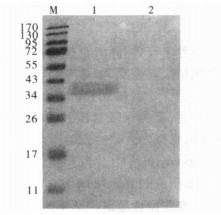
注:M:蛋白质分子量标准; 1:重组原肌球蛋白与过敏患者血清反应; 2:重组原肌球蛋白与健康人血清反应。 图 3 免疫印迹分析重组原肌球蛋白变应原活性 |
Western-blotting检测结果显示,在阳性血清反应条带上约36 kDa处有一明显的识别条带,同时阴性血清无对应的识别条带。表明本研究制备的tropomyosin能与对虾过敏的患者血清IgE结合,具有良好的变应原活性。
3 讨论大肠埃希菌原核表达系统遗传背景清楚、转化和表达效率高, 易发酵且易于操作,可以快速大量生产重组蛋白。本研究选用的pET28a (+)是一种高效原核表达系统,N端含有6个组氨酸标鉴(6×HiS tag),使重组蛋白的纯化可采用金属螯合Ni2+亲和层析的方法〔5, 6〕,从而使纯化蛋白操作简便。
本研究利用生物信息学方法对多种动物性食物和虾泛变应原tropomyosin基因进行同源性分析,利用其高度保守区域设计并合成简并引物,从中国南北沿海常见口虾蛄中成功克隆出一个新的口虾蛄tropomyosin基因,该基因由855个碱基组成(含终止子),编码284个氨基酸,并登录了GeneBank数据库(登录号为EF584510)。通过对其编码氨基酸序列的同源性分析发现与其他报道的虾tropomyosin具有较高的同源性(约95%),提示不同地区的同一种变应原基因具有一定的区域特色,这可能是由于该物种在区域驯化或人为改良等选择进化的长期过程中形成的。基因差异导致其编码的蛋白质变应原性也可能存在一定的差异,故在临床上应尽可能使用本地化的变应原进行临床免疫诊断和治疗。此外,本研究获得的重组tropomyosin能和对虾过敏病人血清中的IgE结合,表明重组变应原具有良好的变应原性,将为口虾蛄变态反应性疾病的特异性诊断研究奠定基础。
| [1] | Arlian LG. Arthropod allergens and human health[J]. Annu Rev Entomol, 2002, 47 : 395–433. DOI:10.1146/annurev.ento.47.091201.145224 |
| [2] | Reese G, Ayuso R, Lehrer SB. Tropomyosin:an invertebrate pan-allergen[J]. Int Arch Allergy Immunol, 1999, 119(4) : 247–258. DOI:10.1159/000024201 |
| [3] | 朱健琦, 刘志刚, 高波, 等. 粉尘螨Ⅰ类变应原(Der fⅠ)的克隆表达、纯化及免疫学特性[J]. 昆虫学报, 2006, 49(2) : 213–218. |
| [4] | 杨慧, 刘志刚, 韩庆国, 等. 艾蒿、青蒿花粉变应原组分的研究[J]. 免疫学杂志, 2004, 20(2) : 120–123. |
| [5] | 安广宇, 董宁征, 阮长耿. 抗血小板膜糖蛋白单克隆抗体SZ 21基因克隆及单链抗体的构建和表达[J]. 免疫学杂志, 2001, 17(3) : 200–203. |
| [6] | Jiang Z, Huang AL, Tao XH. Construction and characterization of bivalent vaccine candidate expressing HspA and M (r)18000 OMP from Helicobacter pylori[J]. World J Gastroenterol, 2003, 9(8) : 1756–1761. DOI:10.3748/wjg.v9.i8.1756 |
 2009, Vol. 25
2009, Vol. 25

 , 吉坤美
, 吉坤美