血管内皮的炎性反应是引发心血管疾病的重要早期事件。细胞间粘附分子-1(intercellular adhesion molecule-1,ICAM-1)和血管细胞粘附分子-1(vascular cell adhesion molecule,VCAM-1)参与血管内皮的炎性反应〔1, 2〕。莱菔硫烷是主要存在于十字花科蔬菜(尤其是绿菜花)中的异硫氰酸盐类植物化学物(isothiocyanates,ITCs),流行病学调查提示,莱菔硫烷可能具有预防心血管疾病的作用〔3〕。为了解莱菔硫烷对上述2类重要的血管内皮细胞粘附因子表达的影响,为莱菔硫烷在防治心血管疾病中的应用提供理论基础,本研究以体外培养的人脐静脉内皮细胞(ECV304)为研究模型,以脂多糖(LPS)作为炎性刺激物,从转录水平上观察了莱菔硫烷对ICAM-1和VCAM-1的影响及分子机制。结果报告如下。
1 材料与方法 1.1 材料(1)细胞:人血管内皮细胞选择人脐静脉内皮细胞(ECV304);中科院上海生命科学研究院细胞库)。(2)试剂:莱菔硫烷(美国LKT有限公司);脂多糖(LPS;美国Sigma公司);兔抗人核转录因子(NF-κB)抗体、异硫氰基荧光素(FITC)标记的兔二抗(美国Santa Cruz有限公司);mRNA提取试剂(TRIZOL;美国Invitrogen公司);其他试剂(美国ABI公司);逆转录试剂盒primescriptTM RT Reagent Kit (大连宝生物公司);Real-time PCR所用探针、引物由美国Sigma公司合成。ICAM-1和VCAM-1引物及探针序列如下:ICAM-1(NM_000201):正向引物5′-TCAGTCAGATACAACAGCATTTG-3′;反向引物5′-CTCATCAGGCTAGACTTTAACATC-3′;探针5′-TCTTGCTCCTTCCTCTTGGCTTAGTCAT-3′。VCAM-1(NM_001078):正向引物5′-GCTGAGAGGCAGACTTCC-3′;反向引物5′-GGCAGTTACTGTTCTTCAGG-3′;探针5′-AAGAAATGCCCATCTATGTCCCTTGCTG-3′。18S (X03205):正向引物5′-GGCTCATTAAATCAGTTATGGTTCCT-3′;反向引物5′-GTATTAGCTCTAGAA TTACCACAGTTATCCA-3′;探针5′-TGGTCGCTCGCTCCTC TCCCAC-3′。
1.2 方法 1.2.1 总RNA提取ECV304细胞在含10%胎牛血清的RPMI-1640培养液进行常规培养。取生长状态良好的ECV304细胞接种于20 ml的培养瓶中。贴壁过夜,待细胞呈现单层融合状态时,先用低血清浓度的培养液(5%胎牛血清)预处理2 h,随后用不同剂量的莱菔硫烷预作用4 h,最后除对照组外各组再加入100 ng/ml的脂多糖刺激1 h。用冷磷酸盐缓冲液(PBS)冲洗细胞后,用TRIZOL试剂盒按照说明书操作。提取后的总RNA用紫外分光光度计测定含量,并进行RNA纯度及完整性鉴定,将符合实验要求的总RNA于-80 ℃保存备用。
1.2.2 逆转录和实时定量PCR逆转录采用primescriptTM RT Reagent Kit进行。总转录体积为10 μl,反应条件为37 ℃ 15 min,85 ℃ 5 s。将逆转录后的cDNA进行定量PCR (real-time PCR)反应。采用25 μl体系,其中包括50 ng样品、100 nmol/L引物和200 nmol/L探针以及10 μl的Tag酶的复合体系,不足体积用无RNA酶的焦磷酸二(diethl pyrocarbonate,DEPC)水补充。反应条件如下:50 ℃ 2 min;95 ℃ 10 min;95 ℃ 15 s;60 ℃,1 min 40个循环。数据结果采用2△△Ct法〔4〕计算(其中[△△Ct=(Ct,目标-Ct,18 S)处理-(Ct,目标-Ct, 18 S)对照])。
1.2.3 免疫荧光杂交反应取生长状态良好的ECV304细胞接种于6孔板中爬片,每孔浓度为5×104个细胞。过夜后,待细胞完全贴上盖玻片后,进行分组,对照组采用含5%胎牛血清的低浓度培养液培养2 h;脂多糖单独刺激组采用含5%胎牛血清的低浓度培养液培养2 h后再用脂多糖作用30 min;莱菔硫烷作用组采用含5%胎牛血清的低浓度培养液培养2 h后,分别用5,10,20 μmol/L的莱菔硫烷作用4 h,然后再用脂多糖作用30 min。处理后的细胞用丙酮在-20 ℃固定20 min,洗涤后在室温下杂交抗NF-κB抗体(1:50)2 h,然后避光杂交FITC标记的兔二抗(1:100)1 h,在激光共聚焦显微镜下观察结果并拍照。
1.3 统计分析采用SPSS 16.0软件进行方差分析,差异有统计学意义用SNK (Student-Newman-Keuls)分析,检验水平α=0.05。
2 结果 2.1 莱菔硫烷下调ICAM-1 mRNA表达(图 1)
|
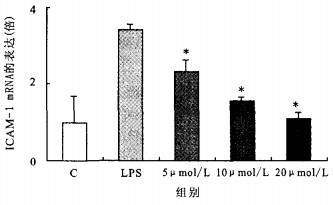
注:与LPS组比较,* P < 0.05。 图 1 莱菔硫烷对LPS诱导的ICA M -1 mRNA表达的抑制作用 |
图 1可见,ECV304细胞受到脂多糖(100 ng/ml)刺激后,ICAM-1 mRNA表达量明显上升,是对照组的3.4倍;用5,10,20 μmol/L莱菔硫烷作用后,细胞中ICAM-1mRNA表达量分别下降为对照组的2.3,1.5和1.1倍,呈一定剂量-效应关系,与脂多糖组比较,差异均有统计学意义(均P < 0.05)。其中20 μmol/L的莱菔硫烷组ICAM-1的mRNA表达水平已接近对照组水平。表明莱菔硫烷能明显抑制脂多糖诱导的ECV304细胞中ICAM-1的mRNA表达。
2.2 莱菔硫烷下调VCAM-1 mRNA表达(图 2)
|
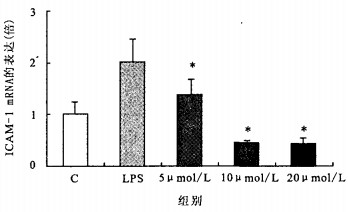
注:与LPS组比较,* P < 0.05。 图 2 莱菔硫烷对LPS诱导的VCAM-1 mRNA表达的抑制作用 |
图 2可见,脂多糖(100 ng/ml)作用ECV304细胞后,能明显诱导VCAM-1 mRNA的表达,比对照组上升2倍(P < 0.05)。莱菔硫烷可明显抑制脂多糖诱导的VCAM-1 mRNA表达。其中5 μmol/L莱菔硫烷能使脂多糖诱导的VCAM-1 mRNA表达降低为1.4倍,10,20 μmol/L莱菔硫烷则完全抵消了脂多糖对VCAM-1 mRNA的诱导,2组VCAM-1 mRNA的表达均降低为对照组的0.4倍,与脂多糖组比较,差异均有统计学意义(均P < 0.05)。表明莱菔硫烷能明显抑制脂多糖诱导的ECV304细胞中VCAM-1 mRNA的表达。
2.3 莱菔硫烷阻断NF-κB向核内转位(图 3)
|
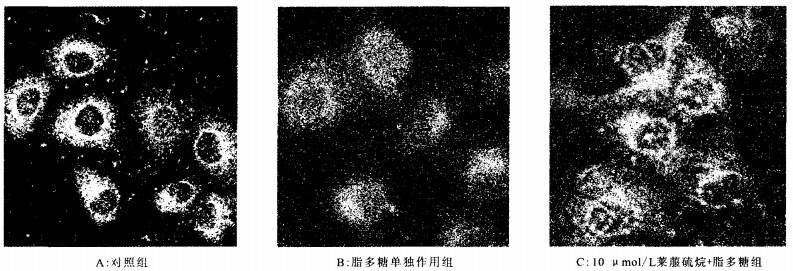
图 3 莱菔硫烷对ECV304细胞内NF-κB的核转录的影响 |
采用免疫荧光杂交反应,并用激光扫描共聚焦显微镜观察NF-κB由细胞浆向细胞核内转位情况。图 3可见,细胞在静息状态下,细胞浆内呈现强烈的绿色荧光,表明NF-κB主要存在于静息细胞的胞浆内(图 3A);脂多糖(100 ng/ml)作用ECV304细胞30 min后,细胞浆内强烈绿色荧光减弱而胞核呈现强烈的绿色荧光,提示脂多糖能明显诱导NF-κB由细胞浆向细胞核内转位(图 3B);10 μmol/L莱菔硫烷作用后再用脂多糖处理细胞,细胞核中的绿色荧光明显弱于脂多糖单独处理组,提示莱菔硫烷能明显抑制脂多糖诱导的NF-κB向核内的转位(图 3C)。
3 讨论莱菔硫烷是一种异硫氰酸盐(isothiocyanates,ITCs)类的植物化学物,其多种作用机制特别是作为癌症化学预防剂的机制已经被实验证实〔5, 6〕。近年来研究提示,莱菔硫烷也可能参与了炎症调节过程〔7, 8〕。本文观察结果显示,用100 ng/ml的脂多糖作用ECV304细胞1 h后,ICAM-1和VCAM-1 mRNA的表达水平明显上升,表明在本实验条件下,成功建立了粘附分子高表达的实验模型。5~20 μmol/L莱菔硫烷能在不同程度上抑制脂多糖诱导的ICAM-1和VCAM-1 mRNA表达,而且莱菔硫烷对VCAM-1的抑制作用强于ICAM-1。
NF-κB是LPS诱导的前炎症反应的主要转录因子和调节因子〔6〕,是存在于ICAM-1和VCAM-1基因上的NF-κB特异结合位点,在ICAM-1和VCAM-1表达中特别是在调节炎性刺激引起的表达上发挥关键作用〔9〕。本文结果显示,10 μmol/L的莱菔硫烷可明显阻断LPS诱导的NF-κB核转位,但莱菔硫烷通过何种机制来调控NF-κB的核转位尚需进一步研究。
本文结果在血管内皮细胞水平上证实了莱菔硫烷对细胞粘附的抑制作用,为莱菔硫烷的抗炎作用提供了实验依据。研究表明,莱菔硫烷在5~20 μmol/L剂量范围内的有效作用可能更具有实际意义,该剂量范围只需要每天摄入约200 g绿菜花即可达到〔10〕。提示莱菔硫烷在较低剂量水平表现出的抗血管粘附作用可应用于心血管疾病防治。
| [1] | 张刚, 程锦泉, 彭绩. 细胞间粘附分子-1与心血管疾病相关性[J]. 中国公共卫生, 2006, 22(11) : 1404–1406. |
| [2] | Galkina E, Ley K. Vascular adhesion molecules in atherosclerosis[J]. Arterioscler Thromb Vasc Biol, 2007, 27 : 2292–2301. DOI:10.1161/ATVBAHA.107.149179 |
| [3] | Wu L, Noyan Ashraf MH, Facci M, et al. Dietary approach to attenuate oxidative stress, hypertension, and inflammation in the cardiovascular system[J]. Proc Natl Acad Sci USA, 2004, 101(18) : 7094–7099. DOI:10.1073/pnas.0402004101 |
| [4] | Suzuki N, Yoshida A, Nakano Y. Quantitative analysis of multi-species oral biofilms by TaqMan real-Time PCR[J]. Clinical Medicine & Research, 2005, 3(3) : 176–185. |
| [5] | Zhang Y, Tang L. Discovery and development of sulforaphane as a cancer chemopreventive phytochemical[J]. Acta Pharmacol Sin, 2007, 28(9) : 1343–1354. DOI:10.1111/aphs.2007.28.issue-9 |
| [6] | Jugea N, Mithena RF, Traka M. Molecular basis for chemoprevention by sulforaphane:a comprehensive review[J]. Cell Mol Life Sci, 2007, 64 : 1105–1127. DOI:10.1007/s00018-007-6484-5 |
| [7] | Thejass P, Kuttan G. Modulation of cell-mediated immune response in B16F-10 melanoma-induced metastatic tumor-bearing C57BL/6 mice by sulforaphane[J]. Immunopharmacol Immunotoxicol, 2007, 29(2) : 173–186. DOI:10.1080/08923970701511728 |
| [8] | Bertl E, Bartsch H, Gerhäuser C. Inhibition of angiogenesis and endothelial cell functions are novel sulforaphane-mediated mechanisms in chemoprevention[J]. Mol Cancer Ther, 2006, 5(3) : 575–585. DOI:10.1158/1535-7163.MCT-05-0324 |
| [9] | Heiss E, Herhaus C, Klimo K, et al. Nuclear factor kappa B is a molecular target for sulforaphane-mediated anti-inflammatory mechanisms[J]. Biol Chem, 2001, 276 : 32008–32015. DOI:10.1074/jbc.M104794200 |
| [10] | Conaway CC, Getahun SM, Liebes LL, et al. Disposition of glucosinolates and sulforaphane in humans after ingestion of steamed and fresh broccoli[J]. Nutr Cancer, 2000, 38 : 168–178. DOI:10.1207/S15327914NC382_5 |
 2009, Vol. 25
2009, Vol. 25

