2. 江苏大学医学院;
3. 江苏大学机械工程学院
国内外对稳恒磁场生物效应的研究较多。实验证明,弱磁场会引起显著的生物学效应,改变细胞增殖,抑制细胞凋亡以及改变基因转录。研究显示,工频磁场对成纤维细胞F-action骨架形态可产生影响〔1〕。但不同强度的稳恒磁场对生物体产生的生物效应尚不明确,由于各试验室的衡量标准不同,有些研究结果相差甚远。当生物体完全暴露于稳恒磁场中,磁场将可能对生物体的生长代谢产生影响〔2-5〕。本文通过稳恒磁场对新生小鼠肾上皮细胞作用,观测其对细胞分化、增殖、蛋白质以及脂质过氧化的影响,探索稳恒磁场对新生小鼠肾上皮细胞增殖和分化的影响。
1 材料与方法 1.1 试剂与仪器稳恒磁场(镇江金港磁性元件有限公司);RPMI1640培养基(美国Sigma公司);胎牛血清(美国GIBCO公司);胰蛋白酶(1:250)进口分装(美国Sigma公司);CO2培养箱(美国NAPCO公司);马血清(浙江三利生物制品厂)。二甲基亚砜(美国GIBCO公司)。
1.2 大鼠新生小鼠肾上皮细胞制备采用文献〔6〕方法进行培养,活细胞率为92%,再用含10%胎牛血清的RPMI 1640培养基将细胞密度调整至4×105个细胞/ml的细胞悬液,于CO2培养箱中(37 ℃,5% CO2,95%空气,100%湿度)孵育。
1.3 新生小鼠肾上皮细胞培养调整细胞密度为4×105个细胞/ml加入96孔培养板,每孔加20 μl,置CO2培养箱中(37 ℃,5% CO2,95%空气,100%湿度)培养,分对照组(二甲基亚砜)和稳恒磁场强度剂量组,强度分别按5,10,20,30,40,50和60 mT;每组4孔,第3 d更换1次新鲜培养基,第10 d后吸掉每孔中的培养液,用等渗2.5%戊二醛固定,然后用苏木精染色,放入37 ℃培养箱内孵育过夜,次晨用磷酸盐缓冲液(PBS)冲洗2次,在倒置显微镜下观察染成蓝色的肾上皮细胞和集落形态,计算出集落形成率,以正常对照组集落数为100%,确定肾上皮细胞分化抑制结果。
1.4 新生小鼠肾上皮细胞蛋白质含量测定〔7〕上皮细胞悬液(4×105个细胞/ml)加入24孔培养板培养10 d后,用0.1%胰蛋白酶消化,离心,吸取沉淀物。采用考马斯亮蓝G-250方法测定小鼠肾上皮细胞内的蛋白质相对含量,以正常对照组为100%,以蛋白质的相对含量来反映不同强度的稳恒磁场对上皮细胞作用,即蛋白质相对含量的变化可反映细胞毒性作用。
1.5 新生小鼠肾上皮细胞内丙二醛(MDA)含量测定〔9〕以上述同样方法收集各组细胞,调整细胞密度为4×105个细胞/ml,制成单细胞悬液,pH 7.4的磷酸盐缓冲液制备成匀浆,低温状态下离心4 000 r/min后,取出上清液待测。采用改进的硫代巴比妥酸法测定丙二醛含量。
1.6 新生小鼠肾上皮细胞内超氧化物歧化酶(SOD)活性测定〔8〕作用10 d后用0.25%胰蛋白酶消化收集细胞,再用磷酸盐缓冲液(PBS)漂洗3次,调整细胞密度为4×105个/ml制成单细胞悬液,低温超声粉碎细胞,采用改良的连苯三酚自氧化法测定超氧化物歧化酶(SOD)的活性。
1.7 统计分析采用Stata 7.0统计软件进行t检验。
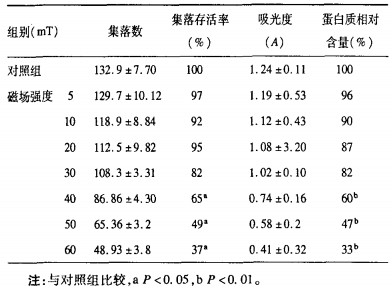
2 结果 2.1 稳恒磁场对新生小鼠肾上皮细胞存活率及蛋白质含量影响(表 1)| 表 1 不同稳恒磁场强度对新生小鼠肾上皮细胞集落存活率和蛋白质含量影响(x±s, n=10) |
正常对照组新生小鼠肾上皮细胞培养,初期呈圆形分散分布,胞体呈圆形或菱形,部分细胞开始长出突起。随着时间延长,胞体增大,细胞之间有相连接现象,突起也逐渐发育生长,10 d后形成明显的集落,当稳恒磁场强度为40,50,60 mT时,集落形成率比对照组明显降低(P < 0.01),而且出现细胞脱落、漂浮、细胞明显崩解、细胞碎片等现象。当稳恒磁场的磁感应的磁感应的磁感应强度为40,50,60 mT时相对蛋白质含量比对照组明显降低(P < 0.05)。
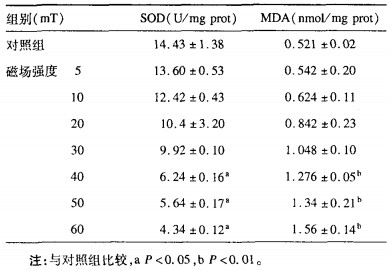
2.2 稳恒磁场对新生小鼠肾上皮细胞MDA、SOD的影响(表 2)| 表 2 不同稳恒磁场强度对新生小鼠肾上皮细胞SOD活性和MDA含量影响(x±s, n=10) |
表 2显示,不同强度的稳恒磁场染毒新生小鼠肾上皮细胞后,细胞中MDA含量与对照组比较,当稳恒磁场的磁感应强度为40,50,60 mT时MDA的含量均增高,呈明显的剂量-效应关系,差异均有统计学意义(P < 0.01)。与对照组比较,当稳恒磁场的磁感应强度为40,50,60 mT时SOD活性逐渐降低,且呈明显的剂量-效应关系(P < 0.05)。
3 讨论在有些工作和生活环境中,人们会受到不同强度的磁场作用;在磁疗和磁性保健用品的使用中,均存在着稳恒磁场暴露对人体健康影响的安全限量问题〔10, 11〕。国外对稳恒磁场生物效应的研究多侧重于实验观察和职业暴露,而国内对稳恒磁场生物效应的研究则以磁疗和磁保健用品作用为主〔10〕。本实验研究发现,一定强度的稳恒磁场对细胞有损伤作用。表现细胞内的自由基活性、蛋白质含量及对肾上皮细胞集落形成均有抑制作用。机体代谢过程中产生的活性氧自由基若不被及时消除,就会对自身造成氧化危害,抗氧化系统能有效阻止自由基在体内的积累。稳恒磁场对运动的带电粒子有洛沦兹力作用,影响细胞膜的离子通透性和膜两侧的电位,从而使信号的跨膜传导发生改变。本实验结果显示,当稳恒磁场强度为40,50,60 mT时,新生小鼠肾上皮细胞集落形成率明显降低,而且出现细胞脱落、漂浮、细胞明显崩解、细胞碎片及死亡现象。稳恒磁场强度为40,50,60 mT时,蛋白质相对含量、SOD活性及MDA含量同时受到不同程度的影响。结果提示,在一定强度的磁场作用下,既可抑制新生小鼠肾上皮细胞的增殖、分化;又使蛋白质含量降低和脂质过氧化平衡失调。
| [1] | 储克平, 菜知音, 张玉, 等. 0.4 mT工频磁场对CHL细胞微丝装配的影响[J]. 中国辐射卫生, 2007, 16(3) : 259–261. |
| [2] | High WB, Sikora J, Ugurbil K, et al. Subchronic in vivo effects of a high static magnetic field (9.4 T) in rats[J]. Journal of Magnetic Resonance Imaging, 2005, 12(1) : 122–139. |
| [3] | Wiskirchen J, Groenewaeller EF, Kehlbach R, et al. Long-term effects of repetitive exposure to a static magnetic field (1.5 T) on proliferation of human fetal lung fibroblasts[J]. Magnetic Resonance in Medicine, 1999, 41(3) : 464–468. DOI:10.1002/(ISSN)1522-2594 |
| [4] | Kelleher MO, Al-Abri RK, Lenihan DV, et al. Use of a static magnetic field to promote recovery after peripheral nerve injury[J]. J Neurosurg, 2006, 105(4) : 610–615. DOI:10.3171/jns.2006.105.4.610 |
| [5] | Onodera H, Jin Z, Chida S, et al. Effects of 10-T static magnetic field on human peripheral blood immune cells[J]. Radiat Res, 2003, 159 : 775–779. DOI:10.1667/0033-7587(2003)159[0775:EOTSMF]2.0.CO;2 |
| [6] | 吴全义, 端礼荣. 氦氖激光对大鼠胚胎脊髓神经细胞影响[J]. 中国公共卫生, 2004, 20(11) : 1322–1323. |
| [7] | 司徒镇强, 吴军正. 细胞培养[M]. 北京: 世界图书出版社, 1996: 181-183. |
| [8] | 赵云斌, 刘敏, 余忠谊. 邻苯三酚自氧化法测定血中超氧化物歧化酶的活性[J]. 中国卫生检验杂志, 2001, 11(4) : 387–388. |
| [9] | 向荣, 王鼎年. 过氧化脂质硫代巴比妥酸分光光度法的改进[J]. 生物化学与生物物理进展, 1990, 17(3) : 241–242. |
| [10] | 郭润霞. 稳恒磁场生物效应与暴露安全限量[J]. 环境与健康杂志, 2003, 20(1) : 50–52. |
| [11] | 张莹, 李伯勤, 董娟, 等. 工频磁场对胎鼠大脑皮质神经元影响[J]. 中国公共卫生, 2008, 24(4) : 503–504. |
 2009, Vol. 25
2009, Vol. 25