2. 华南理工大学轻工与食品学院生物技术与基因工程中心
沙门菌是食源性致病菌中一个主要的属,在各类细菌性食物中毒事件中,沙门菌造成的食物中毒位居前列〔1, 2〕。常规的沙门菌检测方法费时费力,已经不能满足食品生产质量控制的要求〔3〕。因此,需要开发一种灵敏度高并且反应迅速的方法。Notomi等开发出一种新的恒温核酸扩增法-环介导恒温核酸扩增法(loop-mediated isothermal amplification of DNA,LAMP)〔4, 5〕。本研究利用DNA环介导恒温核酸扩增法对市售不同生肉来源的沙门菌进行快速检测,并且着重在灵敏度和特异性方面对此方法进行验证,以建立的LAMP反应条件能够对今后病原微生物的检测研究工作提供参考依据。
1 材料与方法 1.1 菌株猪霍乱沙门菌猪霍乱亚种ATCC13312(S.ATCC13312)(广东省微生物研究所);其余5株沙门菌HB009,HB371,HB069,HB215,HB143分别分离自市售的生猪肉、海产品、生牛肉、生羊肉和鸡肉。其他属菌株共14株保藏于本实验室,作为沙门菌环介导恒温核酸扩增反应特异性试验中的对照菌株。所有菌株均保存在质脂双层(LB)培养基中。
1.2 仪器及试剂恒温金属浴锅(Thermocell, 杭州博日科技有限公司);PCR扩增仪ABI2700(美国ABI公司);凝胶成像系统(BIO-RAD Gel Doc EQ凝胶成像系统)。Bst大片段DNA聚合酶(爱尔兰Biolabs公司);甜菜碱(分析纯,美国Sigma公司);琼脂糖以及引物合成(大连TaKaRa生物公司)。
1.3 方法 1.3.1 LAMP反应引物设计以沙门菌的属特异性基因invA〔6, 7〕为靶基因,选择位于8 091~331之间的DNA序列作为LAMP扩增区域。将待扩增的DNA分为6个独立的区域,根据这6个区域分别设计LAMP反应所需2对引物(内引物FIP和BIP、外引物F3和B3)。FIP由F2和F1C两部分组成,BIP由B2和B1C两部分组成,其2个部分都能分别识别靶DNA正义链和反义链独立区域。外引物F3和B3分别识别靶DNA上F2和B2的外侧的独立区域,F3序列是5′-gcaacagctacgtgatga-3′;B3序列是5′-ctctattgccggcatcatta-3′。2对引物识别靶DNA上6个独立区域。FIP由22个碱基F1C和20个碱基F2,以及中间连接的TTTT组成,序列是5′-cttagatccccgcattgttggttttccgccacatattatcgcgat-3′;BIP由21个碱基B1C和20个碱基B2,以及中间连接的TTTT组成,序列是5′-gaccatcatgaatggtcagcattttattggcggtatttcggtcta-3′(引物由大连宝生物公司合成)。
1.3.2 LAMP反应(1) DNA模板制备:DNA提取参照文献〔8〕。(2) LAMP反应体系:25μl反应混合物包括各1.6 μmol/L的FIP和BIP,各0.2 mol/L的F3和B3,1×恒温缓冲液,1 mol/L的甜菜碱,6 mmol/L的MgSO4,1.6 mmol/L的dNTP,8 U/μl的大片断DNA聚合酶,1 μlDNA。(3)反应过程:除了大片断DNA聚合酶,将其余的试剂混合物于95℃反应5 min,使DNA变性。然后迅速于冰上冷却,并加入Bst聚合酶,将反应物混匀,置于65℃恒温金属浴中反应60 min,最后在80℃条件下反应5 min结束反应。(4) LAMP产物检测:肉眼观察反应物的外观变化并在2%琼脂糖凝胶上100 V电泳分离25 min,加样量7 μl/上样孔。凝胶置于EB中染色10 min,水洗10 min,在BIO-RAD Gel Doc EQ凝胶成像系统下照像检测。
1.3.3 PCR反应50 μl反应总体积的组成:1 μl模板,各30 pmol外引物,1.25U Taq DNA聚合酶,10 mmol/L dNTP 2 μl,5μl 10×Buffer。扩增循环条件为:94 ℃预变性5 min,之后94 ℃变性30 s;52 ℃退火30 s;72 ℃延伸1 min,共30个循环,最后延伸7 min。取PCR产物5 μl,在1%琼脂糖凝胶电泳上100 V电泳20 min,EB染色后在BIO-RAD Gel Doc EQ凝胶成像系统下照像检测。
2 结果 2.1 S.ATCC13312的LAMP反应条件试验为了确立LAMP反应的条件,选择S.ATCC13312菌株的DNA作为扩增目标。结果从凝胶上230 bp大小的位置一直到上样孔处,出现了梯状的多条带,表明是发生特异性扩增反应。阴性对照没有添加扩增目标的模板DNA。
2.1.1 LAMP反应时间测试LAMP反应在60~65 ℃都可以进行,并且在60 min内就可以完成。试验发现,反应温度在60~65 ℃之间结果区别不明显,只是65 ℃的时候生成产物量稍微多一些。所以,将LAMP反应的温度初步定在65 ℃。在65 ℃条件下,检测最快的反应时间,分别将反应时间设为15,30,45,60 min。每个时间对应的LAMP反应的S.ATCC13312 DNA的量均是10 ng。随着反应时间的延长,靶DNA的数量在不断增长,在45 min时,有迹象表明发生特异性扩增,时间延长到60 min时,产物大量生成。
2.1.2 LAMP反应引物试验LAMP反应体系中,S.ATCCl3312 DNA的量均定为10 ng,设立每个体系分别缺失1条或2条引物,分别在65 ℃下反应60 min,反应结束后用2%的琼脂糖凝胶电泳分离、成像。只有当4条引物全部同时存在时反应才能进行。表明缺失任何一条引物都不能进行LAMP反应过程中链置换反应,不能形成哑铃状的DNA结构,从而使反应停滞。
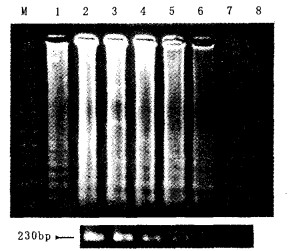
2.2 S.ATCC13312的LAMP和PCR反应灵敏度比较试验(图 1)
|
注:M: DGL2000; 1:阳性对照; 2~7: S. ATCC13312 DNA的量分别为每管1 ng, 100, 10, 1 pg, 100, 10 fg; 8:阴性对照。 图 1 LAMP和PCR反应灵敏度比较 |
将S.ATCCl3312的DNA依次进行10倍的稀释,最终使得DNA浓度分别为1 ng/μl,100,10,1 pg/μl,10,1 fg/μl。将稀释过的DNA分别取1μl于LAMP应中和PCR反应,检测这2种方法的灵敏度。结果可见,LAMP反应可以在60 min内,最低检测到100 fg DNA/管。PCR反应最低检测到1 pgDNA/管。
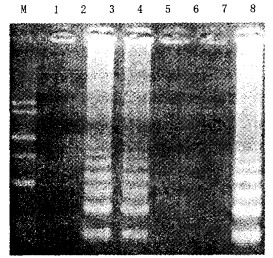
2.3 S.ATCC13312的LAMP反应特异性试验(图 2)
|
注:M:DGL2000; 1:阴性对照(无靶DNA存在); 2: LAMP反应体系中1 pg靶DNA混合100 ng大肠埃希菌O157: H7基因组DNA; 3: LAMP反应体系中1 pg靶DNA混合100 ng铜绿假单胞菌P81基因组DNA; 4: 100 ng大肠埃希菌O157: H7基因组DNA; 5: 100 ng铜绿假单胞菌P81基因组DNA; 6:阳性对照(1 pg S. ATCC13312基因组DNA)。 图 2 LAMP反应特异性试验(1) |
为了检测LAMP反应的特异性,分别在25 μl反应体系中,将100 ng的非沙门菌属的DNA与1 pg S.ATCC13312 DNA混合作为LAMP反应的扩增目标,65℃下反应60 min。观察LAMP反应是否受外源DNA的影响。结果可见,本试验设计的LAMP反应对S.ATCC13312是非常特异的。
2.4 LAMP反应检测不同食物来源沙门菌特异性试验(图 3)

|
注:M: DGL2000; 1: 1 pg S. ATCC13312 DNA; 2: 1 pg沙门菌HB009 DNA; 3: 1 pg沙门菌HB371DNA; 4: 1 pg沙门菌HB069 DNA; 5: 1 pg沙门氏菌HB215 DNA; 6: 1 pg沙门菌HB143 DNA; 7: 10 ng屎肠球菌41 DNA; 8: 10 ng金黄色葡萄球菌200 DNA; 9: 10 ng嗜麦寡养单胞菌112 DNA; 10: 10 ng奇异变形杆菌70 DNA; 11: 10 ng鲍氏不动杆菌74 DNA; 12: 10 ng凝固酶阴性葡萄球菌80 DNA; 13: 10 ng克氏肺炎菌55 DNA; 14: 10 ng弗氏柠檬酸杆菌46 DNA; 15: 10 ng大肠埃希菌240 DNA; 16: 10 ng铜绿假单胞菌P24 DNA; 17:阴性对照。 图 3 LAMP反应特异性试验(2) |
利用已经建立的LAMP试验条件分别检测市售不同生肉来源的沙门菌(1 pg/μ1),并且同时也利用相同的条件扩增其他属的细菌(10 ng/μl),确认LAMP反应可以特异性地检测到沙门菌,反应条件同1.3.2。结果可见,本试验针对沙门菌特异性基因invA设计的LAMP反应,只对不同生肉来源的沙门菌是特异性的,在60 min内就能利用此反应快速地检测到。但是同样条件下,对非沙门菌检测均阴性。
3 讨论本实验结果表明,根据沙门菌特异性invA基因设计的LAMP反应对于沙门菌的检测是非常快速有效的,它可以在恒温65 ℃条件下60 min内检测到目标菌的靶基因,凝胶上出现的梯状电泳条带表明特异性反应发生。同一反应体系中,检测靶基因的过程不会受到大量存在的非靶基因的影响,特异性很强。LAMP反应可以最少检测到100 fg的靶DNA,其检测灵敏度是PCR反应的10倍,这样,在利用LAMP方法进行检测时就会大大减少假阳性或者假阴性存在的可能。
LAMP方法是一种简便、快速、高效的基因扩增法,与PCR反应相比,LAMP反应最明显的优势是,在一般恒温条件下进行,所用设备简单、花费少,普通水浴锅或其他有稳定热源的装置就可以采用,不需要PCR所必需的精密温度循环装置,同时它的检测灵敏度和特异性又能满足快速鉴定病原微生物的需要,可以节约成本。所以,它可以作为常规检测工具,能够建立起总成本低廉的检测体系,在公共卫生安全检测、临床快速诊断以及环境监测等领域有实际应用意义。
| [1] | Tirado C, Schmidt K. WHO surveillance programme for control of foodborne infections and intoxications:results and trends across greater Europe[J]. J Infect, 2001, 43 : 80–84. DOI:10.1016/S0163-4453(01)90861-8 |
| [2] | Wallace DJ, Van Gilder T, Shallow S, et al.Incidence of foodborne illnesses reported by the foodborne diseases active surveillance network[FoodNet]-1997.FoodNet Working Group[J].J Food Prot, 2000, 63:807-809. |
| [3] | 何晓青. 沙门氏菌检验技术进展[J]. 中国公共卫生, 2003, 19(10) : 1260–1262. |
| [4] | Notomi T, Okayama H, Masubuchi H, et al. Loop-mediated isothermal amplification of DNA[J]. Nucleic Acids Res, 2000, 28(12) : e63. DOI:10.1093/nar/28.12.e63 |
| [5] | 王丽, 石磊, 李琳. DNA环介导的恒温扩增法在快速鉴定病原微生物中的应用[J]. 生命的化学, 2006, 26(5) : 462–464. |
| [6] | Chen S, Yee A, Griffiths M, et al. The evaluation of a fluorogenic polymerase chain reaction assay for the detection of Salmonella species in food commodities international[J]. J Food Microbiol, 1997, 35 : 239–250. DOI:10.1016/S0168-1605(97)01241-5 |
| [7] | Ohtsuka K, Yanagawa K, Takatori K, et al. Detection of Salmonella enteria in naturally contaminated liquid eggs by loop-mediated isothermal amplification, and characterization of Salmonella isolates[J]. Appl Environ Microbiol, 2005, 71 : 6730–6735. DOI:10.1128/AEM.71.11.6730-6735.2005 |
| [8] | Sambrook J, Frishch EF, Maniatis T. Molecular cloning:A laboratory manual[M].2th ed.New York: Cold Spring Harbor Laboratory press, 1989: 439. |
 2009, Vol. 25
2009, Vol. 25

