2. 中国农业科学院农产加工研究所, 北京 100094
近年来,伴随饲料工业的发展,为满足畜禽快速生长需要,我国畜牧业生产过程中存在盲目向饲料中添加过多微量元素的现象,导致饲料中铅超标的情况时有发生,对畜禽健康和食品安全造成潜在的危害〔1〕。有研究表明,长期低剂量铅暴露可以抑制T淋巴细胞的增殖和分化〔2, 3〕,并导致血清中免疫球蛋白IgM,IgG含量降低〔4〕。本研究观察饲料中添加不同剂量铅对猪免疫机能的影响,找出饲料中铅含量与猪免疫毒性的剂量-效应关系,为国家制定饲料中铅含量限量标准提供理论依据。
1 材料与方法 1.1 材料与仪器健康商品仔猪24头,雌雄各半(陕西杨陵上河猪场),体重14~17 kg;醋酸铅(纯西安化学试剂厂);胎牛血清培养液(DMEM)(美国Gibco公司);植物凝集素(PPHA-P)(美国Sigma公司);二甲基亚砜(DMSO,美国Sigma公司);猪淋巴细胞分离液(天津灏洋生物制品科技责任公司);标准胎牛血清(天津灏洋生物制品科技责任公司);XD811L生化分析仪(上海迅达医疗仪器有限公司);CA500三分类血液分析仪(日本埃尔玛公司);CKX41倒置显微镜(日本Olympus公司);MCO-15AC二氧化碳培养箱(日本Sanyo公司);DG5030多孔酶标测定仪(国营华东电子管厂)。
1.2 分组与染毒24头猪随机分为4组,每组6头,分别为对照组和低、中、高剂量组(饲料中分别添加铅5.0,15.0,45.0 mg/kg)。正常饲料适应性饲养10 d后,攻毒饲养持续90 d。
1.3 血液中白细胞数量分析采用乙二胺四乙酸钠(EDTA-Na)真空采采取猪血管抗凝血,血液分析仪测定全血中白细胞数量。
1.4 T淋巴细胞活力测定采用T淋巴细胞转化试验测定T淋巴细胞转化率。于猪前腔静脉采取无菌抗凝血,经猪淋巴细胞分离液分离出淋巴细胞,显微镜下稀释至5×106个/ml,加入含PHA-P的DMEM培养藏100 μl (PHA-P终浓度为9 μg/ml),CO2培养箱孵育68 h,之后加入四甲基偶氮噻唑蓝(MTT 5 mg/ml)10 μl,继续孵育4 h,加入100 μl DMSO,轻微振荡10 min,利用酶标仪在490 nm波长下测定其吸光度(A)值。用加PHA-P孔的吸光度值减去不加PHA-P孔的吸光度值代表淋巴细胞的活力。
1.5 免疫球蛋白(IgM,IgG,lgA)和补体(C3,C4)测定采用免疫比浊法,按照试剂盒说明操作。试剂盒(上海玉兰生物技术有限公司)。
1.6 统计分析采用SPSS 13.0软件进行方差分析和Duncan多重比较分析。
2 结果 2.1 铅对猪血液中白细胞数量及T淋巴细胞活力的影响(表 1)| 表 1 铅暴露对猪白细胞数量和T淋巴细胞活力影响(x±s) |
低中剂量组血液中白细胞数量较对照组略有降低,差异无统计学意义(P > 0.05);高剂量组血液中白细胞数量显著低于对照组(P < 0.05)。3个剂量组T淋巴细胞活力与对照组比较差异均有统计学意义(P < 0.05),且中剂量组T淋巴细胞活力较低剂量组略有上升, 但3个攻毒组血液内T淋巴细胞活力差异无统计学意义(P > 0.05)。
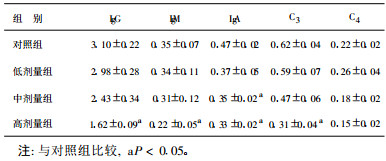
2.2 铅对猪血清中免疫球蛋白及补体含量的影响(表 2)| 表 2 铅暴露对猪血清中免疫球蛋白和补体含量影响(x±s, g/L) |
随着饲料中铅含量的增高,血清中免疫球蛋白数量呈下降趋势。结果显示,高剂量组体内IgG、IgA含量均显著低于对照组(P < 0.05);中剂量组体内IgA含量显著低于对照组P < 0.05);低剂量组各类免疫球蛋白含量与对照组比较差异均无统计学意(P < 0.05)。随着饲料中铅含量的增加,C3含量呈逐步降低趋势,且高剂量组血清中C3含量与对照组比较差异有统计学意义(P < 0.05),而中、低剂量组血清中C3含量与对照组之间比较差异无统计学意义(P > 0.05)。C4含量低剂量组与高剂量组比较差异有统计学意义(P < 0.05)。
3 讨论T淋巴细胞转化试验是目前测定机体细胞免疫功能状态的一种较好的方法,而测定血清中的IgM、IgG、IgA、C3、C4含量则能较好地反映出机体体液免疫能力的强弱。
研究发现,饲喂含铅饲料可导致猪体内白细胞含量降低,T淋巴细胞活力下降,免疫球蛋白与补体含量下降。说明食用含铅饲料可以使猪免疫力降低,证明铅具有免疫毒性,与相关报道一致〔5-8〕但也有报道表明, 铅可以促进T淋巴细胞的增殖和分化,低浓度的铅在体外可以激活小鼠淋巴细胞,使其DNA合成增加〔9〕。本实验发现, 中剂量组T淋巴细胞活力略高于低剂量组,但远低于对照组。提示,铅含量在一定范围内或许可以小幅度提高T淋巴细胞活力,但具体作用机制还有待于进一步研究。
实验结果表明,低剂量组T淋巴细胞活力测定结果与对照组比较差异有统计学意义,(P < 0.05),说明饲料中含铅5 mg/kg对试验猪免疫能力的损伤已经在少数指标上开始体现。高剂量组的试验猪各免疫指标与对照组相比急剧降低,其中WBC、IgG、IgA、C3与对照组比较差异有统计学意义(P < 0.01),说明饲料中铅含量达到45 mg/kg己经对猪免疫力造成极严重影响,与成军〔10〕等研究结果部分相似。
| [1] | 何进, 黄逸红. 饲料中铅、镉含量超标的危害与对策[J]. 饲料博览, 2006(5) : 45–47. |
| [2] | Mishra KP, Singh VK, Rani R, et al. Effect of lead exposure on the immune response of some occupationally exposed individuals[J]. Toxicology, 2003, 188(2-3) : 251–259. DOI:10.1016/S0300-483X(03)00091-X |
| [3] | 赵剑, 蔡原, 谭成森, 等. 铅和乙醇对雄性小鼠细胞免疫功能影响[J]. 中国公共卫生, 2006, 22(1) : 52–53. |
| [4] | Sarasua SM, Vogt RF, Henderson LO, et al. Serum immunoglobulins and lymphocyte subset distributions in children and adults living in communities assessed for lead and cadmium exposure[J]. Journal of Toxicoloy and Environmental Health, 2000, 60(1) : 1–15. DOI:10.1080/009841000156556 |
| [5] | Koller LD, Kovacic S. Decreased antibody formation in mice exposed to lead[J]. Nature, 1974, 250(462) : 148–150. |
| [6] | Lee JE, Naqi SA, Kao E, et al. Embryonic exposure to lead: comparison of immune and cellular responses in unchallenged and virally stressed chickens[J]. Arch Toxicol, 2002, 75(11-12) : 717–724. DOI:10.1007/s00204-001-0283-9 |
| [7] | Lee JE, Chen S, Karen A, et al. Developmental windows of differential lead-induced immunotoxicity in chickens[J]. Toxicology, 2001, 156(2-3) : 161–170. DOI:10.1016/S0300-483X(00)00350-4 |
| [8] | 钟振伟, 王净. 小鼠喂养低铅饲料对细胞免疫功能的影响[J]. 中国公共卫生, 2002, 18(12) : 1429–1430. |
| [9] | Krocova Z, Macela A, Kroca M, et al. The immunomodulatory effect (s) of lead and cadmium on the cells of immune system in vitro[J]. Toxicol in Vitro, 2000, 14(1) : 33–40. DOI:10.1016/S0887-2333(99)00089-2 |
| [10] | 成军, 高丰, 金天明, 等. 仔猪实验性铅中毒的血液学变化[J]. 内蒙古民族大学学报:自然科学版, 2004, 19(2) : 190–192. |
 2009, Vol. 25
2009, Vol. 25

 , 郭波莉2, 潘家荣2, 杨鸣琦1, 文一2
, 郭波莉2, 潘家荣2, 杨鸣琦1, 文一2