研究表明,线粒体功能改变与细胞凋亡密切相关。线粒体膜通透性转运孔(mitochondrial permeability transition pore,MPTP)在细胞凋亡(cell apoptosis) 中的作用非常关键[1, 2]。MPTP的开放可导致线粒体膜通透性转变,引起促凋亡因子释放、活性氧过度生成、能量产生障碍、胞浆内钙稳态失衡等一系列凋亡事件的发生。实验表明,镉能够引起细胞凋亡,并且线粒体受损是镉毒性的首要位点[3]。本实验室研究已发现:镉能够诱导人胚胎肾细胞(HEK 293) 细胞凋亡,并且其凋亡依赖于线粒体凋亡途径[4, 5],但是其机制尚不十分清楚。本实验对离体的HEK 293细胞的线粒体进行CdCl2染毒,研究CdCl2诱导MPTP的开放、线粒体膜电位(mitochondrial membrane potential,MMP)、氧化应激(oxidative stress)损伤和一系列线粒体酶活性的变化,进一步阐明线粒体结构和功能损伤在镉致HEK293细胞凋亡中的作用。
1 材料与方法 1.1 材料人正常肾细胞系HEK 293(本实验室制备)。胎牛血清培养液(DMEM)(美国GIBCO公司);小牛血清(杭州四季青生物技术有限公司);线粒体提取试剂盒(美国PIERCE公司);环孢素A (cyclosporin A,Cs A)、2,7-二氯荧光素二乙酸酯 (DCFH-DA) (美国Sigma公司);罗丹明123 (rhodamine 123,Rh-123) (南京凯基公司);ATP酶、乳酸脱氢酶(LDH)、超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)和丙二醛(MDA)生化试剂盒(南京建成生物工程研究所);其他常规化学试剂均为国产分析纯。主要仪器包括:分光光度计(日本Shimadazu公司);透射电镜(日本JEOL公司);荧光分光光度计(日本岛津公司)。
1.2 线粒体提取HEK 293细胞贴壁培养于含10%小牛血清,青、链霉素各100 U/L的DMEM中,置于37℃,5%CO2的饱和湿度培养箱中培养。取处于对数生长期的HEK 293细胞,细胞量约2×107。按线粒体提取试剂盒说明书从细胞中提取线粒体。提取线粒体的所有步骤均在冰上操作。
1.3 分光光度法测定MPTPMPTP的变化表现线粒体膨胀产生的吸光度下降[6, 7]。参照文献[8],配制线粒体膨胀测定介质(250 mmol/L蔗糖,0.5 mmol/L KH2PO4,4.2 mmol/L丁二酸钾,2 mmol/LTris,pH 7.4)。用线粒体膨胀测定介质将线粒体稀释至蛋白浓度为0.5 mg/ml。将不同浓度(1,5,10 μmol/L)的CdCl2和10 μmol/L CdCl2加1 μmol/L Cs A与线粒体悬液共同孵育2 min,对照组加入等体积生理盐水。在UV-2101PC紫外分光光度仪上检测吸光度A 520 nm处的变化,持续观察10 min。
1.4 线粒体超微结构的观察不同浓度(1,5,10 μmol/L)的CdCl2与线粒体25℃共同孵育2 min,对照组加入等体积生理盐水。然后经2.5%的戊二醛固定,再用1%的锇酸固定,丙酮脱水,环氧树脂包埋。聚合后经超薄切片,醋酸铀、柠檬酸铅双重染色,JEM-1230透射电镜下观察线粒体的超微结构。
1.5 Rh-123检测线粒体膜电位的变化上述各组线粒体悬液加入Rh-123使其终浓度为5 mg/L,37℃避光孵育20 min,再用磷酸盐缓冲液(PBS)洗3遍,荧光分光光度计检测荧光强度,激发光波长为505 nm,发射光波长为534 nm。
1.6 活性氧(reactive oxygen species,ROS)含量的测定参照文献[9],利用荧光探针2,7-二氯荧光素二乙酸酯(DCFH-DA)进行ROS含量测定。配制N-2羟乙基哌嗪-N′-2-乙磺酸(HEPES)缓冲液(120 mmol/L NaCl,2.5 mmol/L KCl,1.2 mmol/L NaH2PO4,0.1 mmol/L MgCl2,5.0 mmol/L NaHCO3,6.0 mmol/L葡萄糖,1.0 mmol/L CaCl2,10 mmol/L HEPES,pH 7.4)。线粒体用HEPES缓冲液重悬,用5 μmol/L DCFH-DA(终浓度)对活性氧进行标记,荧光分光光度计检测荧光强度,激发光波长为488 nm,发射光波长为530 nm。
1.7 与呼吸作用相关的酶活力检测测定了Na+-K+-ATP酶、Ca2+-Mg2+-ATP酶和LDH的活力,以试剂盒和分光光度计进行测定,重复3次。
1.8 与氧化应激相关指标的检测SOD、GSH-Px的活力和MDA的含量以试剂盒和分光光度计进行测定,重复3次。
1.9 统计分析采用SPSS 8.0软件进行统计分析。组间差异采用t检验。
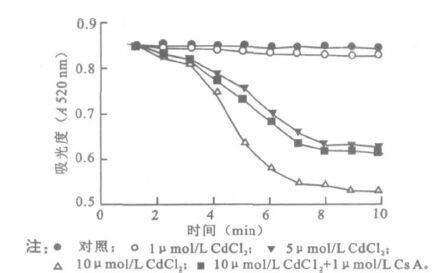
2 结果 2.1 CdCl2对MPTP的影响(图 1)不同浓度CdCl2均使吸光度下降,且呈一定的浓度-效应依存关系,其中5,10μmol/L CdCl2处理组与对照组比较,A值有明显的下降。MPTP抑制剂CsA和10 μmol/L CdCl2共孵育组与10 μmol/L CdCl2单独处理组比较,线粒体吸光度值减小,表明镉引起的MPTP的开放能够被CsA所抑制。
|
图 1 不同浓度CdCl2对MPTP开放的影响 |
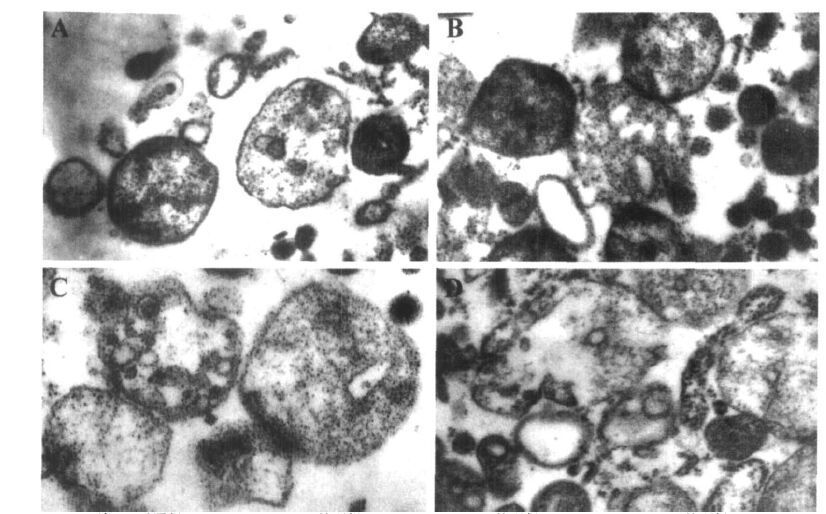
2.2 CdCl2引起线粒体形态的改变(图 2)
|
注: A: 对照组; B: 1 Lmol /L CdCl2 处理组; C: 5 Lmol/ L CdCl2 处理组; D: 10 Lmol/L CdCl2 处理组。 图 2 线粒体形态改变的电镜观察(×12000) |
2.3 CdCl2对线粒体膜电位的影响
CdCl2处理组线粒体膜电位明显低于对照组,其中5 μmol/L CdCl2处理组和10 μmol/L CdCl2处理组与对照组比较,差异有统计学意义(P<0.05)。
2.4 CdCl2对线粒体内ROS含量的影响1,5,10 μmol/L的CdCl2均能够促进ROS的生成,随着CdCl2浓度增大荧光强度逐渐增大,其中5 μmol/L CdCl2处理组(50.40±1.32)与对照组(26.10±4.10)比较,差异有统计学意义(P<0.05),10 μmol/L CdCl2处理组(60.77&llusmn;3.72) 与对照组比较,差异有统计学意义(P<0.01)。
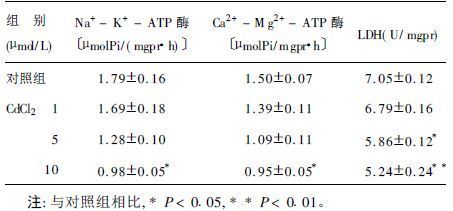
2.5 CdCl2对线粒体内呼吸作用相关酶活力影响(表 1)实验结果表明,1 μmol/L的CdCl2即可影响Na+-K+-ATP酶、Ca2+-Mg2+-ATP酶和LDH的活性,其酶活力值低于对照组,并且随着CdCl2剂量的加大,酶活性呈逐渐降低的趋势。和对照组比较,10 μmol/L CdCl2处理组的Na+-K+-ATP酶、Ca2+-Mg2+-ATP酶和LDH活性均明显降低,差异有统计学意义(P<0.05或P<0.01)。
| 表 1 CdCl2对线粒体内ATP酶和LDH活性的抑制作用( x±s, n=3) |
2.6 CdCl2对氧化应激的影响(表 2)
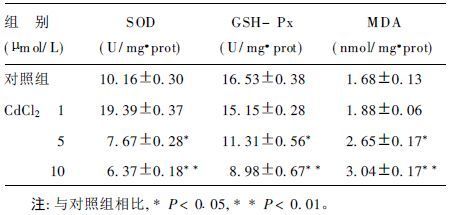
随着CdCl2浓度的增大,SOD和GSH-Px的活性逐渐降低,MDA的含量趋于升高,呈一定的剂量-反应关系,其中5和10 μmol/L CdCl2处理组与对照组比较,差异均有统计学意义(P<0.05或P<0.01)。
| 表 2 CdCl2对氧化应激的影响( x±s, n=3) |
3 讨论
MPTP是跨越线粒体内外膜的通道,是由蛋白质组成的复合体。多种凋亡信号,如促凋亡蛋白Bax、Bad、Bid和Ca2+、活性氧类等可以诱导MPTP开放,引发线粒体肿胀,线粒体跨膜电位降低[7]。本研究发现,CdCl2能引起MPTP的开放并使线粒体膜电位下降。
同时镉处理后线粒体的ROS含量呈逐渐增加的趋势,并且SOD、GSH-Px的活性有明显的下降,而MDA的含量却大幅度的增加,高浓度处理组与对照组比较,差异有统计学意义(P<0.01)。SOD能清除超氧阴离子自由基(O2-),保护细胞免受损伤;GSH-Px是催化过氧化氢(H2O2)分解的酶。因此,这些酶活力的高低间接反映了机体清除氧自由基能力的大小。当机体处于氧化应激状态时,体内组织细胞ROS量相对升高,超过机体的清除能力,可导致机体组织脂质过氧化水平升高。MDA是脂质过氧化物的主要产物之一,其在生物体内的含量间接反映细胞的损伤。本研究发现,HEK 293细胞线粒体中MDA的含量随着染镉浓度的增大呈上升趋势,说明HEK 293细胞线粒体的膜系统遭受到越来越严重的损伤。
以上结果证实镉可诱导HEK 293细胞线粒体的结构和功能损伤。镉可以引起MPTP的开放、线粒体膨胀、线粒体膜电位下降、ROS含量的增加以及和氧化应激相关的酶活性降低等一系列与细胞凋亡相关事件的发生,说明线粒体在镉诱导的HEK293细胞凋亡中发挥着重要作用。
| [1] | Takeyama N, Miki S, H irakaw a A, et al. Role of mit ochondrial permeabilit y tansit ion and cyt och rome C release in hydrogen peroxide induced apopt osis[J]. Exp Cell Res, 2002, 274(1) : 16–24. DOI:10.1006/excr.2001.5447 |
| [2] | Hirakaw a A, T akeyama N, Nakatani T, et al. M it ochon drial permeability transit ion and cyt ochrome C release in isch emia-reperfusion injury of th e rat liver[J]. J S urg Res, 2003, 111(2) : 240–247. DOI:10.1016/S0022-4804(03)00091-X |
| [3] | Hamada T, Sasaguri T, Tanimoto A, et al. Apoptosis of human kidney 293 cells is promot ed by polymerized cadm ium-metallothionein[J]. Biochem Biophys Res Commun, 1996, 219(3) : 829–834. DOI:10.1006/bbrc.1996.0318 |
| [4] | 田婷, 毛伟平, 张超, 等. 镉致HEK293细胞凋亡中氧化应激作用[J]. 中国公共卫生, 2007, 23(10) : 1192–1193. |
| [5] | Mao WP, Ye JL, Guan ZB, et al. Cadmium induces apoptosis in human embryonic kidney (HEK) 293 cells by caspase-dependent and-independent pathw ays acting on mitochondria[J]. Toxicology In Vit ro, 2007, 21 : 343–354. DOI:10.1016/j.tiv.2006.09.004 |
| [6] | Clarke SJ, McStay GP, Halest rap AP. Sanglif ehrin A acts as a potent inhibit or of the mit ochondrial permeability transition and reperfusion injury of the heart by binding to cyclophilin-D at a diff erent sit e f rom cyclosporin A[J]. J Biol Chem, 2002, 277 : 34793–34799. DOI:10.1074/jbc.M202191200 |
| [7] | DiL isa F, M enabo R, Cant on M, et al. Opening of the mitochondrial permeabil it y transit ion pore causes depletion of mit ochondrial and cyt osolic NAD+ and is a causat ive event in the death of myocyt es in postischemic reperfusion of the heart[J]. J Biol Chem, 2001, 276 : 2571–2572. DOI:10.1074/jbc.M006825200 |
| [8] | Hunt er DR, Haworth RA. The Ca2+-induced membran e trans-i tion in mit ochondria[J]. Arch Biochem Biophys, 1979, 195 : 453–459. DOI:10.1016/0003-9861(79)90371-0 |
| [9] | Hamai D, Campbell A, Bondy SC. Modulat ion of oxidat ive event s by mult ivalent manganese complexes in brain tissue[J]. Free Rad Biol Med, 2001, 31 : 763–768. DOI:10.1016/S0891-5849(01)00639-6 |
 2008, Vol. 24
2008, Vol. 24