自20世纪80年代,中国大陆、孟加拉等因饮用高砷水暴发大面积砷(As)中毒以来,慢性砷中毒已引起全世界的重视[1]。流行病学调查显示[2-4],长期砷暴露可降低儿童的智力和记忆能力。但是,目前砷暴露致记忆障碍的分子机制尚不清楚。海马是学习记忆的重要部位。N-甲基-D-天冬氨酸受体(NMDAR)是兴奋型氨基酸特异性受体的一种,近年来被认为是学习记忆中的关键物质。本文对砷暴露大鼠海马神经元超微结构和NMSAR亚基mRNA表达进行检测,以探讨砷暴露致学习记忆障碍的分子机制。
1 材料与方法 1.1 试剂NaAsO2(德国Merck公司);As标准溶液(GBW08611国家标准物质研究中心)。
1.2 仪器微波消解仪(奥地利Anton Paar公司);原子荧光光度计(北京海光公司);透射电子显微镜(荷兰飞利浦公司);MyCycler梯度PCR仪(美国Bio-rad公司)。
1.3 方法 1.3.1 动物染毒健康断乳Sprague-Dawley雄性大鼠48只,体重40~50 g,(第三军医大学实验动物中心)。在标准SPF级动物房内饲养,人工控制昼夜变化。实验时随机分为4组:对照组、低剂量组、中剂量组和高剂量组,每组12只。对照组饮用消毒自来水,染毒组分别饮用2.72,13.6,68 mg/L亚砷酸钠水溶液并每2 d换1次,连续染毒3个月。实验终期,大鼠经10%水合氯醛腹腔麻醉,心脏采血后,断头分离脑组织,将脑组织在冰冷生理盐水中漂洗,用滤纸吸干,置于-70度冰箱保存。
1.3.2 脑砷的测定取脑组织0.2 g于聚四氟乙烯管,经微波消解后,用原子荧光光度计测定砷含量。
1.3.3 透射电子显微镜标本制作实验终期,大鼠经腹腔麻醉后,断头,在冰上快速分离海马,切取1 mm×1 mm×1 mm海马CA1区组织块,2.5%的戊二醛溶液4℃固定24 h。0.1 mo/L磷酸盐缓冲液漂洗,1%锇酸后固定,丙酮梯度脱水,环氧树脂-618包埋。半薄切片(片厚1μm)定位,超薄切片,饱和醋酸铀电子染色,TECNAI-10电子显微镜观察,照相。
1.3.4 NMDAR亚基基因表达的检测引物序列如下:内参β-actin上游:5′-TAA AGA CCT CTA TGC CAA CAC AGT-3′,下游:5′CAC GAT GGA GGG GCC GGA CTC ATC-3′,产物长度250 bp。NR1亚基上游:5′AGC GGG TAAACAACA GCA ACAAAA -3′,下游5′-GAA TCG GCC AAA GGG ACT GAA-3′,产物长度305 bp。NR2A亚基上游:5′-ATA CCG GCA GAA CTC CAC AC-3′,下游:5′-CCT CCA GTA GCC GTT CTC TG-3′,产物长度387 bp。NR2B亚基上游:5′GGC CTT CTT TGC TGT CAT TTT-3′,下游5′-AGT TCT TCC ATC TCC CCA TCT C-3,产物长度471 bp。每组随机选5只大鼠海马进行RT-PCR。按试剂盒说明书步骤提取总RNA,按常规方法制备cDNA,以cDNA为模板进行PCR扩增。PCR产物经1.7%的琼脂糖凝胶电泳,BIO-RAD凝胶成像分析系统进行灰度扫描。目的条带表达量的计算为目的条带灰度值/β-actin条带灰度值。
1.4 统计分析应用SPSS 10.0统计软件进行单因素方差(One-Way-ANOVA)分析。
2 结果 2.1 大鼠脑砷值3个砷暴露组的大鼠脑砷均高于对照组,且脑砷值随饮水砷浓度的增高而增加;13.6和68 mg/L组脑砷值[(3.75+0.68) 和(4.33+0.64) μg/g],与对照和2.72 mg/L组脑砷值[0和(0.44+0.09) μg/g]比较,差异有统计学意义(P<0.05)。
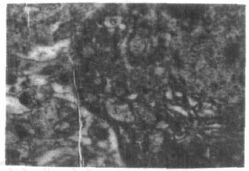
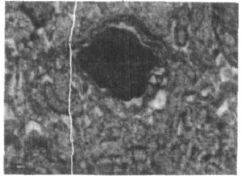
2.2 透射电镜观察结果(1) 神经细胞变化:对照组神经元细胞核形态规则,核膜光滑,染色质分布均匀;细胞器丰富,粗面内质网分布规则,网腔均匀一致,表面附有较多核糖体颗粒。实验组能见到许多神经元,胞体变小,胞浆浓缩,基质染色变深;细胞器肿胀、空化,线粒体肿胀,脊减少或无脊,粗面内质网扩张(图 1)。(2) 毛细血管变化:对照组毛细血管,周围结构正常,内皮细胞的胞核、细胞器及其外周的基膜清晰可见。实验组毛细血管内皮细胞中部分粗面内质网、高尔基复合体、线粒体可见明显的扩张(图 2)。
|
图 1 染砷组海马神经元 |
|
图 2 染砷组海马毛细血管 |
2.3 NMDA受体亚基mRNA表达(图 3~图 5)
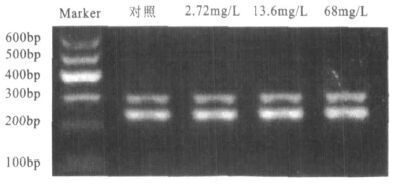
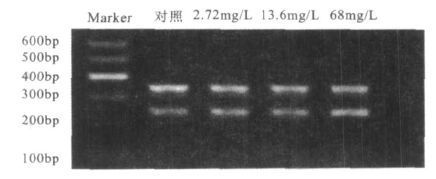
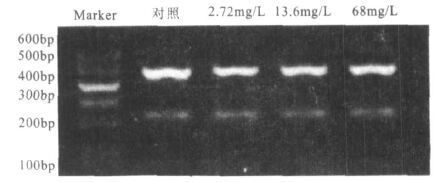
图 3可见,NR1亚基RT-PCR扩增产物长度为305 bp,内参β-actin 250 bp,与预期目的片断相同。大鼠海马组织NR1 mRNA在砷暴露后,各处理组与对照组相比差异无统计学意义(P>0.05)。图 4可见,NR2A亚基RT-PCR扩增产物长度为387 bp,与预期目的片断相同。大鼠海马组织NR2A mRNA在砷暴露后,各处理组与对照组相比均明显降低(P<0.05)。2.72,13.6,68 mg/L组分别为对照组的79%,80%和71%。图 5可见,NR2B亚基RT-PCR扩增产物长度为471 bp,与预期目的片断相同。大鼠海马组织NR2B mRNA在砷暴露后,各处理组与对照组比较差异无统计学意义(P>0.05)。
|
图 3 NR1亚基mRNA RT-PCR扩增产物 |
|
图 4 NR2A亚基mRNA RT-PCR扩增产物 |
|
图 5 NR2B亚基mRNA RT-PCR扩增产物 |
3 讨论
砷是一种神经毒物,长期暴露于高砷环境,可引起失眠健忘等高级神经功能紊乱[6]。动物实验表明,砷暴露可降低大鼠学习记忆能力[5, 6]。透射电镜观察发现,染砷组大鼠海马神经细胞发生一系列病变。砷是一种原浆毒物,能抑制多种酶活性,影响细胞代谢。砷与脂质过氧化也有关,能抑制线粒体的生物氧化和三磷酸腺苷(ATP)的形成[7],从而使细胞超微结构发生变化,甚至细胞变性。毛细血管内皮细胞损伤,可导致血管通透性增加,降低血脑屏障对毒物的屏蔽作用。
NMDAR被认为是学习记忆的关键物质。NR1是其功能亚基,与学习记忆关系密切;NR2是其调节亚基,共4种亚型,完整的NMDAR至少含有1个NR2亚基。不同的NR2亚基组成的NMDAR对学习记忆功能的贡献也不同[8]。特异性阻断NR2A亚基能消除突触的长时程增强(LTP),特异性阻断NR2A亚基则消除突触的长时程减弱(LTD),LTP与LTD的正常产生是维持良好学习记忆功能的基础[9]。肖俊等发现,慢性砷中毒可抑制LTP的诱导与维持[6]。本实验发现,砷暴露对NR1和NR2B的mRNA表达无影响,但明显地降低了NR2A的mRNA表达量,这将影响LTP诱导与维持。提示NR2A mRNA表达水平的降低,在砷致学习记忆功能障碍中起重要作用。
综上所述,慢性的饮水砷暴露可引起大鼠海马超微结构改变,降低NMDAR亚基mRNA表达,可能进而影响学习记忆功能。
| [1] | 孙贵范. 深入研究慢性砷中毒的分子作用机制[J]. 中国地方病学杂志, 2004, 23(1) : 1–2. |
| [2] | Calderon J, Navarro M E, Jimenez-Capdeville ME, et al. Exposure to arsenic and lead and neuropsychological development in Mexican children[J]. Environmental Research Section A, 2001, 85 : 69–76. DOI:10.1006/enrs.2000.4106 |
| [3] | Song Y T, Hung Y C, Hee W T, et al. The effects of chronic arsenic exposure from drinking water on the neurobehavioral development in adolescence[J]. Neuro Toxicology, 2003, 24 : 747–753. |
| [4] | Wasserman GA, Liu XH, Parvez F, et al. Water arsenic exposure and children’s intellectual function in Araihazar, Bangladesh[J]. Environmental Health Perspectices, 2004, 112(13) : 1329–1333. DOI:10.1289/ehp.6964 |
| [5] | 席淑华, 孙贵范, 孙文绢, 等. 砷对仔代大鼠神经行为和学习记忆功能影响[J]. 中国公共卫生, 2006, 22(5) : 559–560. |
| [6] | 肖俊, 张敏, 潘娅, 等. 慢性染砷对大鼠学习记忆功能的影响[J]. 中国医学物理学杂志, 2006, 23(2) : 114–117. |
| [7] | 吴顺华, 王国荃, 刘开泰. 砷对健康影响的研究进展[J]. 国外医学医学地理分册, 2002, 23(4) : 145–160. |
| [8] | Paoletti P, Neyton J. NMDA receptor subunits:function and phar2 macology[J]. Cur Opin Pharmacol, 2006, 4 : 39–47. |
| [9] | Liu LD, Tak PW, Mario FP, et al. Role of NNMDA receptor sub2 types in governing the direction of hippocampal synaptic plasticity[J]. Science, 2004, 304 : 1021–1023. DOI:10.1126/science.1096615 |
 2008, Vol. 24
2008, Vol. 24

 , 张勇燕, 付文娟
, 张勇燕, 付文娟