引用本文

杨晓红, 赵华明, 汤兆强, 范雪梅, 宋丽云, 殷国荣, 张志华, 段希玲. 肌幼虫可溶性抗原免疫小鼠抗旋毛虫感染作用[J]. 中国公共卫生, 2008, 24(12): 1481-1482.

YANG Xiao-hong, ZHAO Hua-ming, TANG Zhao-qiang, et al. Effect of intranasal immunization with muscle larvae soluble antigen of Trichinella spiralis on the protection of mice against T. spiralis infection[J]. Chinese Journal of Public Health, 2008, 24(12): 1481-1482.

肌幼虫可溶性抗原免疫小鼠抗旋毛虫感染作用
杨晓红
1, 赵华明
2, 汤兆强
2, 范雪梅
2, 宋丽云
2, 殷国荣
3
, 张志华
1, 段希玲
1
1. 山西职工医学院寄生虫学教研室, 太原 030012;
2. 山西医科大学第二临床医学院;
3. 山西医科大学寄生虫学教研室
收稿日期: 2008-04-21
基金项目: 山西省高校科技研究开发项目(200613052)
作者简介: 杨晓红(1961-), 女, 山西太原人, 副教授, 本科, 研究方向:寄生虫感染与免疫。
通讯作者: 殷国荣
摘要:
目的
观察不同剂量旋毛虫肌幼虫可溶性抗原(muscle larvae soluble antigen, MLSAg)滴鼻免疫小鼠诱导的抗旋毛虫感染作用, 确定MLSAg滴鼻免疫适宜剂量.
方法
C57BL/6J小鼠50只, 随机分为5组, 分别用5, 10, 20, 30μg MLSAg溶于20μl生理盐水滴鼻免疫小鼠2次, 间隔2周;对照组用0.9%NaCl20μl滴鼻.末次免疫后7d, 用旋毛虫肌幼虫150条/只灌胃攻击全部小鼠, 观察健康状况, 记录体重.攻击后28d, 检测血清和肠液IgG、IgA.计数舌肌、咬肌、膈肌及后肢肌肉的虫荷.
结果
攻击后对照组小鼠体重逐渐减轻, 而4个免疫组小鼠体重仍呈增高趋势.5, 10, 20和30μg组小鼠血清IgG水平分别为1.255, 1.281, 1.394和1.441;血清IgA水平分别为1.108, 1.282, 1.262和1.326, 均高于对照组(1.158, 1.035).肠液IgA水平分别为1.974, 2.026, 2.057和2.015明显高于对照组(1.785);10, 20和30μg组小鼠肌肉虫荷均明显低于对照组及5μg组(P<0.05).
结论
不同剂量MLSAg滴鼻免疫小鼠均可诱导抗旋毛虫感染, 滴鼻免疫剂量以20μg为佳.
关键词:
旋毛形线虫
肌幼虫可溶性抗原
滴鼻免疫,黏膜免疫
Effect of intranasal immunization with muscle larvae soluble antigen of Trichinella spiralis on the protection of mice against T. spiralis infection
YANG Xiao-hong, ZHAO Hua-ming, TANG Zhao-qiang, et al
Department of Parasitology, Shanxi Medical College of Health Personnel Taiyuan 030012, China
Abstract:
Objective
To investigate the effect of intranasal immunization with different doses of the muscle larvae soluble antigen(MLSAg)of Trichinella spiralis on the protection of mice against T.spiralis infection.
Methods
Fifty adult C57BL/6J mice were randomly divided into five groups and were immunized intranasally with 5, 10, 20 or 30μg of MLSAg per mouse twice at interval of 2 weeks, and the mice receiving PBS were used as controls.On the 7th day after last immunization, all mice were infected with 150 T.spiralis larvae by gastric gavage.The health conditions of the infected mice were observed, and the body weight of mice was recorded every day after challenges.The infected mice were killed on the 28th day after challenges, and the levels of serum Ig G, IgA and Ig G, IgA in small intestinal juice were detected by ELISA.Meanwhile, the larvae in the tongue, masseter, diaphragma and the muscles of posterior limb were counted.
Results
The results showed that the body weight of the control mice gradually decreased after challenges, while those of mice immunized with different doses of MLSAg of T.spi ralis remained steadily growing.The levels of Ig G, IgA in intestinal juice and serum in all the immunized mice were higher than that of the control, especially in the 20μg dose immunized groups.In comparisison with the mice of 5μg dose immunized groups and the control group, the larvae loads in the muscles of tongue, masseter, diaphragma and posterior limb in the 10μg, 20μg and 30μg dose immunized groups were significantly decreased.
Conclusion
It is evident that the intranasal immunization with different doses of MLSAg of T.spiralis can induce protective immune responses against the parasite, in which the protective effect induced with 20μg of soluble antigen were most significant.
Key words:
Trichinella spi ralis
musele larvae soluble antigen
intranasal immunization
mucosal immunity
旋毛形线虫(Trichinella spiralis,旋毛虫)呈世界性分布,可感染人和150多种动物,引起食源性寄生虫病。我国人群中男、女血清平均阳性率分别为3.43%和3.19%[1],最高达50.2%。对旋毛虫病的防治至今尚无疫苗。因此,研制安全、有效、价廉的旋毛虫疫苗乃当务之急。近年来,对黏膜免疫及黏膜免疫接种疫苗的研究很多[2],但有关黏膜免疫在抗旋毛虫感染中作用研究较少[3]。黏膜免疫,备受关注的滴鼻免疫是安全、有效的最佳黏膜免疫途径。与胃肠黏膜免疫相比,鼻黏膜免疫无胃酸及消化酶的作用,只需较少抗原即可诱导有效免疫应答。滴鼻免疫不仅能诱导鼻相关淋巴组织(nasal-associated lymphoid tissue,NALT)免疫应答,而且能诱导全身黏膜相关淋巴组织及系统的免疫应答。本研究采用MLSAg滴鼻免疫小鼠诱导的抗旋毛虫感染作用,为疫苗的制作提供基础依据。
1 材料与方法
1.1 实验动物和旋毛虫 C57BL/6J小鼠(中国医学科学院实验动物研究所,微生物级别为二级);旋毛虫(T.spiralis,T1) (首都医科大学),用于肌幼虫可溶性抗原制备和感染小鼠。
1.2 主要试剂 考马斯亮蓝蛋白测定试剂盒(南京建成生物工程研究所);辣根过氧化物酶标记山羊抗小鼠IgA(美国Sigma公司);辣根过氧化物酶标记山羊抗小鼠IgG(北京中杉金桥生物技术有限公司)。
1.3 MLSAg制备 按文献[4]方法分离并纯化旋毛虫肌幼虫。纯化后的肌幼虫-20℃冻融5次,冰浴中超声粉碎(150W×15s×20次,间隔20s),-20℃冻融3次,4℃,12000r/min离心30min,上清液即为MLSAg。Bradford法测定MLSAg蛋白含量,-20℃保存,用于滴鼻免疫ELISA检测旋毛虫抗体包被酶标板。
1.4 动物分组与处理 6~7周C57BL/6J小鼠50只,雌雄各半,随机分为5组,每组10只。用MLSAg 5,10,20,30μg,溶于20μl 0.9% NaCl,滴鼻免疫2次,间隔2周。对照组用0.9% NaCl 20μl滴鼻。末次免疫后第7d,每只小鼠用150条旋毛虫肌幼虫灌胃攻击。逐日观察小鼠健康状况,记录体重。攻击后28d采血分离血清,颈椎脱臼处死小鼠,剪取全部肠,收集肠冲洗液,取舌肌、咬肌、膈肌及后肢肌肉。
1.5 特异性抗体测定 按文献[5]方法,剪取幽门至回盲部小肠段,置于平皿内,用3ml磷酸盐缓冲液(PBS)冲洗肠腔3次,收集小肠冲洗液,2500r/min离心10min,取上清,-20℃保存备用。ELISA法测定小肠液和血清IgG、IgA吸光度(A492)。
1.6 组织内肌幼虫分离计数 取小鼠舌肌、咬肌、膈肌及后肢肌肉,用1%胃蛋白酶-1%盐酸消化液(15ml/g肌肉),37℃消化18~20h。完全消化后,计数肌肉组织中的旋毛虫幼虫并计算减虫率。减虫率=(对照组每克肌肉幼虫数-实验组每克肌肉幼虫数)/对照组每克肌肉幼虫数×100%。
1.7 统计分析 采用SPSS 11.5统计软件进行分析,组间存活率比较采用χ2检验,其他指标比较采用单因素方差分析。
2 结果
2.1 小鼠健康状况及体重变化 攻击后第7~13d,对照组小鼠出现倦怠、活动减少、饮水及采食减少等异常表现,第14d上述症状减轻、逐渐恢复正常,免疫组小鼠则无明显异常表现。攻击后对照组小鼠体重呈下降趋势,5,10,20,30μg组小鼠体重仍呈增高趋势,差异有统计学意义(P<0.05)。实验过程中小鼠无死亡。
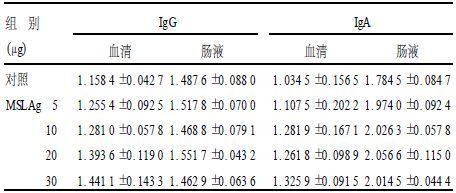
2.2 血清和肠液IgG、IgA水平(表 1) 攻击后第28d,免疫组小鼠血清IgG、IgA和肠液IgA抗体均略高于对照组,但组间差异无统计学意义,小鼠肠液IgG无明显规律性改变。
表 1

表 1 不同组别小鼠血清和肠液IgG、IgA水平(A492 ,
x±s)
|
表 1 不同组别小鼠血清和肠液IgG、IgA水平(A492 ,
x±s)
|
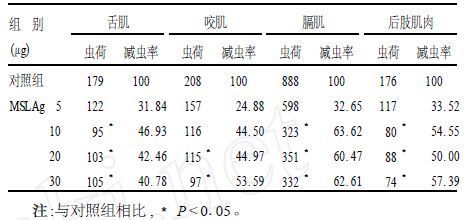
2.3 肌肉虫荷(表 2) 攻击后第28d处死全部小鼠,计数小鼠舌肌、咬肌、隔肌及后肢肌肉平均虫荷和减虫率。10,20,30μg组比较,差异均有统计学意义(P<0.05)。舌肌平均虫荷显著低于对照组;20和30μg组(P<0.05) 咬肌平均虫荷显著低于对照组;10(P<0.001),20(P<0.005) 和30μg组(P<0.005) 膈肌平均虫荷显著低于对照组;10(P<0.05),20(P<0.01) 和30μg组(P<0.001) 后肢肌肉平均虫荷显著低于对照组。
表 2

表 2 不同组别小鼠肌肉平均虫荷(条/g)和减虫率(%)
|
表 2 不同组别小鼠肌肉平均虫荷(条/g)和减虫率(%)
|
3 讨论 本研究表明,该抗原通过黏膜免疫途径能诱导小鼠产生抗旋虫的保护性免疫,免疫组小鼠肠黏液特异性sIgA抗体水平明显升高,且以20μg组为最高,肌幼虫减虫率可达42.46%~60.47%,进一步证实黏膜IgA的水平是其免疫保护的重要环节,而小鼠肠液IgG无明显规律性改变。在本研究中,免疫组小鼠血清IgG和血清IgA均高于对照组,说明在动物体内产生有效的免疫保护。
本试验采用旋毛虫肌幼虫可溶性抗原滴鼻免疫小鼠。实验中发现,攻击后对照组小鼠体重明显降低,免疫组仍呈增高趋势,10,20和30μg组增高明显(P<0.05);10,20和30μg实验组虫荷均明显低于对照组,其他各组肌幼虫减虫率可达62.61%(P<0.05)。目前多数学者采用经口、皮下、皮内、腹腔、肌肉等免疫接种途径,需要大剂量的抗原或使用佐剂,才能发挥较好的免疫效果。本研究中采用经鼻腔内免疫小鼠,较小剂量的抗原,在无佐剂的条件下,也能诱导较强的免疫保护性。
本实验结果表明,不同剂量MLSAg滴鼻免疫小鼠均能诱导抗旋毛虫感染作用,幼虫可溶性抗原作为抗寄生虫病疫苗的候选抗原分子,可通过黏膜免疫途径发挥抗旋毛虫感染的作用。从血清和肠液中抗体的水平及小鼠肌肉的减虫率来看,20μg为旋毛虫肌幼虫可溶性粗抗原滴鼻免疫的最佳剂量。
参考文献
| [1] |
全国人体重要寄生虫病现状调查办公室.
全国人体重要寄生虫病现状调查报告[J]. 中国寄生虫学与寄生虫病杂志, 2005, 23(B10) : 332–340.
|
| [2] |
石蓉, 殷国荣, 孟晓丽, 等.
CpG ODN联合STAg滴鼻免疫BALB/c小鼠诱导的黏膜IgA免疫应答动态变化[J]. 中国公共卫生, 2008, 24(10) : 1197–1199.
|
| [3] |
Picherot M, Oswald IP, Cote M, et al.
Swine infection with Trichinella spi ralis:Comparative analysis of the mucosal intestinal and systemic immune responses[J]. Vet Parasitol, 2007, 143(3) : 122–130.
|
| [4] |
王中全, 崔晶.
旋毛虫幼虫收集方法的探讨[J]. 河南预防医学杂志, 1993, 4(1) : 32–34.
|
| [5] |
殷国荣, 元海军, 杨亚波, 等.
TSo联合IFN-γ鼻内免疫小鼠诱导的弓形虫IgA抗体特异性免疫应答[J]. 热带医学杂志, 2004, 4(6) : 670–673.
|
 2008, Vol. 24
2008, Vol. 24

 , 张志华1, 段希玲1
, 张志华1, 段希玲1