2. 贵阳医学院寄生虫学教研室;
3. 中山大学中山医学院寄生虫学教研室
近30年来,在东南亚、中国大陆和台湾地区发现牛带绦虫,其形态与传统牛带绦虫相似但却以猪作为中间宿主,多数学者称为亚洲牛带绦虫或牛带绦虫亚洲亚种(Taenia saginata asiatica)[1-3]。为了进一步了解亚洲牛带绦虫在分类、分子诊断和基因疫苗等方面情况,于2006年对亚洲牛带绦虫的功能基因组学进行研究[4]。本研究从亚洲牛带绦虫cDNA质粒文库中筛选出WD40基因,通过构建pET-28a(+)-WD40原核表达载体,并对其原核表达产物进行了纯化和免疫学分析。
1 材料与方法 1.1 材料 1.1.1 血清来源感染亚洲牛带绦虫猪血清(贵阳医学院寄生虫学教研室)。患者血清来自贵州省都匀市米秀乡驱出成虫病人;健康人血清(中山医学院病原生物学实验室)。
1.1.2 文库、质粒、菌株虫体标本采自亚洲牛带绦虫流行区贵州省都匀市米秀乡,亚洲牛带绦虫成虫全长cDNA质粒文库的构建和EST测序及Unigene分析与上海联合基因有限公司合作完成。原核表达质粒pET-28a(+)和大肠埃希菌BL-21/DE3由中山医学院病原生物学实验室保存。
1.1.3 主要试剂和工具酶Ex Taq酶(含dNTP)、BamHⅠ、XhoⅠ、T4 DNA连接酶、DNA标准(DL 2000)(大连宝生物工程公司);异丙硫代-β-D半乳糖苷(IPTG)(美国Promega公司);Ni-IDA Agarose(cat No:69670)(美国Novagen公司);蛋白分子量标准(立陶宛MBI公司);DNA凝胶回收试剂盒、质粒纯化试剂盒(北京赛百盛基因公司);辣根过氧化物酶标记的山羊抗猪、抗人IgG二抗、3,3二氨基联苯胺(DAB)显色试剂盒(武汉博士德有限公司);聚偏二氟乙烯膜(PVDF)(美国Millipore公司);十二烷基磺酸钠( SDS)、丙烯酰胺、亚甲叉双丙烯酰胺、过硫酸胺等试剂(上海申友生物科技公司)。
1.1.4 引物合成和DNA测序基因扩增引物和重组质粒DNA测序由Introvigen上海生物技术有限公司合成。
1.2 方法 1.2.1 WD40基因的识别将获得的亚洲牛带绦虫unigene进行Blastx分析,获得编码亚洲牛带绦虫WD40基因文库质粒编号为HC20-D3,GenBank登录号为EF201938。
1.2.2 WD40基因的扩增根据已获得的WD40编码序列,利用DNAClub和PCRdesign设计引物。上游引物:ATCGGATCCATGAAGTTGACCGTATCAGAGGTG带BamHⅠ酶切位点;下游引物:GCGCTCGAGTCACTCAGCATTGATGTTAGGTAAC带XhoⅠ酶切位点。以亚洲牛带绦虫成虫cDNA文库中WD40基因的克隆质粒为模版,94℃预变性5 min后,热循环参数为94℃ 1 min,62℃ 1 min,72℃ 1 min,共32个循环,最后72℃延伸10 min。PCR产物1%琼脂糖凝胶电泳回收。
1.2.3 重组原核表达质粒(pET-28a (+)-WD40)的构建及鉴定将PCR产物和原核表达质粒pET-28a(+) 经BamHiv、XXhoiv双酶切后回收,连接,转化大肠埃希菌BL-21/DE3感受态细胞,卡那霉素筛选阳性克隆;对阳性克隆提取质粒进行PCR、双酶切和测序鉴定。
1.2.4 重组蛋白的表达将确定能表达重组蛋白的单菌落接种于5ml LB培养基中,过夜培养后1:100转接到1 000 ml培养基中,培养至A600约为0.6时加入异丙硫代-β-D半乳糖苷(IPTG)至终浓度为1 mmol/L,28℃、250 r/min进行诱导。诱导4h后离心收菌,用十二烷基磺酸钠(SDS)聚丙烯酰胺凝胶电泳(PAGE)检测蛋白质的表达。
1.2.5 菌体的裂解、重组蛋白可溶性判断及待纯化融合蛋白上清的制备取单菌落接种于1 000 ml含卡那霉素的LB培养基中,37℃震荡培养至A600为0.6,加入IPTG使其终浓度为1 mmol/L,28℃震荡培养4 h。6000 g×10 min 4℃离心,收集细菌,按文献[5]方法进行。
1.2.6 尿素变性纯化重组蛋白在得到的包涵体(超声后沉淀)中加入A液10ml重悬,4℃,12 000 r/min离心15 min,弃上清,重复2次;再用B液洗涤1次,4℃,6 000 r/min离心15 min。将洗涤后的包涵体沉淀加入8 mmol尿素(溶于基础液)18 ml,放置1 h左右,沉淀完全溶解,溶液清亮透明。采用透析法,逐步降低尿素浓度。
1.2.7 免疫印渍法(Western Blotting)检测重组蛋白的免疫性将纯化的蛋白进行SDS-PAGE(12%)电泳,使用电转移仪于100 V冰浴转印1.5 h,将蛋白转移至聚偏二氟乙烯(PVDF)膜上。将含蛋白Marker条带剪下,PVDF膜转入上述感染亚洲牛带绦虫的猪血清(1:100稀释),室温孵育2 h,磷酸盐缓冲液(PBS)洗涤3次,每次5 min。然后于辣根过氧化物酶标记的羊抗猪IgG(1:2000稀释),室温孵育1 h,PBS洗涤3次,每次5 min。DAB显色至出现目的条带,超纯水终止反应[6]。
2 结果 2.1 生物信息学分析该基因与GenBank中日本血吸虫同源基因(登录号为:AAW26164)一致性达74%,相似性达85%。全长1208bp,编码区为81~1056bp,编码324个氨基酸,理论分子质量和等电点分别为35942.4和6.44。
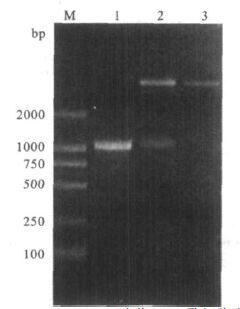
2.2 原核重组质粒的鉴定(图 1)
|
注: M: 为Marker (2000bp); 1: PCR产物; 2:双酶切鉴定结果; 3:重组质粒pET-28a(+)-WD40。 图 1 重组质粒的PCR 及双酶切鉴定图 |
将重组质粒进行PCR和双酶切鉴定,产物进行1%琼脂糖凝胶电泳,在1 000 bp左右有一清晰的条带,与目的基因的大小(975 bp)基本相符,证明重组质粒构建成功。
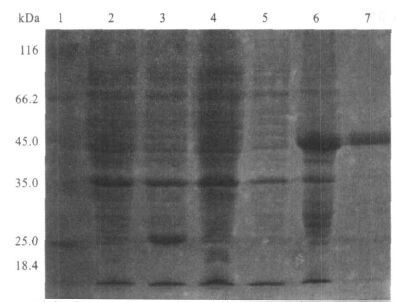
2.2 蛋白表达纯化结果(图 2)
|
注: 1: 蛋白标准; 2: pET-28a(+) 质粒用IPTG 诱导; 3: pET-28a(+) 质粒未用IPT G 诱导; 4: pET-28a(+)-WD40 重组质粒用IPTG 诱导; 5: pET-28a(+)-WD40 重组质粒未用IPT G 诱导; 6:pET-28a(+)-WD40 重组质粒诱导后菌液沉淀; 7: 破包涵体后得到的纯化蛋白。 图 2 重组质粒pET-28a(+)-WD40 在大肠埃希菌BL-21/ DE3 的表达产物的12%SDS-PAGE 电泳分析 |
将构建好的重组质粒转化到E.coli BL-21/DE3中表达,SDS-PAGE电泳分析结果显示,在第6、7泳道大约在42kD左右处出现表达条带,与目的蛋白分子量基本相符。注:1:蛋白标准;2:pET-28a(+)质粒用IPTG诱导;3:pET-28a(+)质粒未用IPTG诱导;4:pET-28a(+)-WD40重组质粒用IPTG诱导;5:pET-28a(+)-WD40重组质粒未用IPTG诱导;6:pET-28a(+)-WD40重组质粒诱导后菌液沉淀;7:破包涵体后得到的纯化蛋白。
2.3 Western Blotting鉴定用感染亚洲牛带绦虫猪血清和患者血清识别重组蛋白均显示出相应的条带。
3 讨论WD40结构域又称为WD基元或Trp-ASP,是一个重要的结构域,存在于很多具有调控功能的蛋白质中,介导蛋白质之间的相互作用,参与多种细胞功能的调节,在信号转导、蛋白运输、染色体修饰、转录或RNA加工、细胞凋亡等过程中具有重要作用[7, 8]。WD40重复序列蛋白是一类结构保守、功能复杂的蛋白,有关此类蛋白和细胞内信号传导途径的研究显示,该家族成员很可能通过调控胞内信号转导而影响细胞基本生命活动,在信号转导、mRNA前体的加工、细胞骨架的装配方面起着极其重要的作用,是一类重要的调节蛋白。
本实验成功构建了亚洲带绦虫成虫重组质粒pET-28a(+)-WD40,并将其转化入大肠埃希菌BL21(DE3),IPTG诱导表达结果显示该蛋白是以包涵体的形式表达,通过尿素变性纯化重组蛋白,得到条带很浓的纯化蛋白。用纯化后的重组抗原做免疫印渍实验,结果能识别感染亚洲牛带绦虫的猪血清和患者血清,证实重组蛋白在纯化后具有免疫反应性。本研究为进一步研究亚洲牛带绦虫WD40基因的生物学功能奠定了基础。
| [1] | 黄艳, 黄江, 胡旭初, 等. 亚洲带绦虫磷脂酰肌醇转运蛋白A序列分析[J]. 中国公共卫生(增刊2007):23:1-3. |
| [2] | 莫兴泽, 包怀恩, 黄江, 等. 亚洲带绦虫与从江牛带绦虫实验感染牛和猪的比较研究[J]. 中国寄生虫病防治杂志, 2005, 18(2) : 120–123. |
| [3] | 包怀恩. 我国亚洲牛带绦虫研究的现状和展望[J]. 热带医学杂志, 2002, 2(3) : 215–219. |
| [4] | 黄江, 胡旭初, 包怀恩, 等. 亚洲带绦虫成虫全长cDNA质粒文库的构建及EST测序[J]. 热带医学杂志, 2007, 7(2) : 116–118. |
| [5] | J萨姆布鲁克, EF弗里奇, T曼尼阿蒂斯. 分子克隆实验指南[M].北京: 科学出版社, 2002: 37-39. |
| [6] | Harlow E, Lane D. 抗体技术实验指南[M].2002: 161-184. |
| [7] | 朱海青, 陈竺, 王振义, 等. 细胞蛋白质相互作用的结构基础[J]. 生命的化学, 2001, 21(2) : 93–95. |
| [8] | 段红英, 丁笑生, 孙富丛. WD-重复蛋白[J]. 中国生物化学与分子生物学报, 2007, 23(2) : 102–105. |
 2008, Vol. 24
2008, Vol. 24

 , 吴璇2, 胡旭初3, 余新炳3, 王虎1
, 吴璇2, 胡旭初3, 余新炳3, 王虎1