2. 浙江省宁波市北仑区疾病预防控制中心;
3. 浙江省医学科学院病毒病研究所
浙江省宁波市地处东南沿海,历史上是甲型肝炎(甲肝)高发区,常见甲肝周期性流行。2000 年宁波市将甲肝疫苗接种纳入计划免疫管理,推广满2周岁儿童接种甲肝疫苗的免疫策略。新型冻干甲肝减毒活疫苗(H2株)是本地区推广接种的疫苗之一。该疫苗是在规范化液体甲肝疫苗(H2株)基础上研制的一种新剂型甲肝减毒活疫苗[1, 2]。它在稳定性、有效期及保证疫苗滴度方面比液体剂型有明显提高[3, 4]。为了进一步考核在甲肝流行区接种该疫苗的血清流行病学效果,验证现有免疫策略的合理性,2002~2006年在宁波市北仑区进行了冻干甲肝疫苗免疫原性及免疫持久性观察。结果报告如下。
1 对象与方法 1.1 对象在宁波市北仑区各接种门诊筛选满2周岁、免疫前血清抗甲肝病毒(HAV)-IgG阴性、无肝炎史和肝病症状的甲肝易感儿童119名,并获得监护人知情同意,接种1剂冻干甲肝减毒活疫苗。冻干甲肝减毒活疫苗(H2株,浙江省普康生物技术有限公司),批号20020606A,滴度为106.5半数感染剂量(TCID50)。以无菌注射用水1.0 ml稀释疫苗后皮下接种。
1.2 方法免疫前采集119名易感儿童指血,采用酶联免疫(ELISA)方法检测抗-HAV-IgG抗体;免疫后2个月采集119名儿童指血,42个月时采集其中94名儿童静脉血(因迁居外地失访25名),分离血清,用酶联免疫竞争抑制法测定抗-HAV抗体(试剂盒浙江省医学科学院提供);同时以WHO甲肝免疫球蛋白标准品(含100mU)进行标定。将待测血清倍比稀释及等比稀释后标准品测得的吸光度(A)值代入回归方程,计算血清中抗-HAV-IgG抗体含量(mU/ml)和几何平均滴度(GMT)。
1.3 统计分析采用SAS软件进行统计分析。
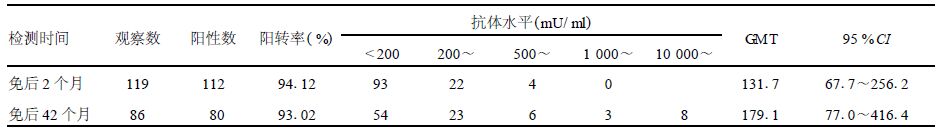
2 结 果 2.1 免疫后抗体水平(表 1)| 表 1 冻干甲型肝炎减毒活疫苗接种42个月血清学效果 |
2.1.1 免疫后2个月抗-HAV IgG抗体水平
119名2周岁儿童接种冻干甲型肝炎减毒活疫苗后2个月,抗-HAV IgG抗体阳转率为94.12%,抗体GMT为131.7(67.7~256.2)mU/ml。
2.1.2 免疫后42个月抗-HAVIgG抗体水平 共有94名儿童观察至免疫后42个月,其中抗-HAV IgG抗体水平大于10 000 mU/ml者8名,推测可能是隐性自然感染后的再次免疫回忆反应,因此,未纳入统计分析。其余86名儿童免疫后42个月的抗体阳性率为93.20%,抗体GMT为179.11 (77.0~416.4)mU/ml。
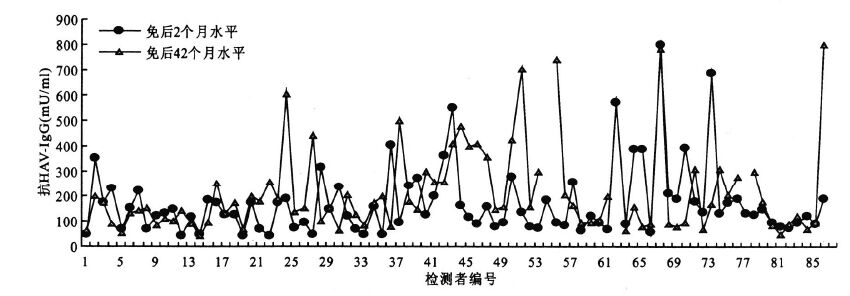
2.2 抗体水平变化(图 1)图 1可见,免疫后42周的抗体GMT高于免疫后2个月(t=2.728,P=0.008)。其中4.7%的个体抗体水平呈4~8倍下降,32.6%的个体抗体呈1~4倍下降,48.8%的个体抗体呈1~4倍升高,13.9%的个体抗体呈4倍以上升高。表明接种冻干甲肝减毒活疫苗后观察42个月,其血清抗体水平没有下降。
|
注:免后42个月抗-HAV IgG水平检测者编号55#:1 536 mU/ml; 63#:2 836 mU/ml; 78#:3 040 mU/ml。 图 1 免疫后2 个月与42 个月抗- HAV IgG抗体水平比较 |
3 讨 论
疫苗对甲型肝炎控制的有效期限取决于疫苗提供的保护期限,而后者与疫苗刺激产生的抗体水平及抗体持久性密切相关。我国科学家自发研制的甲型肝炎减毒活疫苗(H2株)经大规模人群使用其安全性已得到证实[5-8]。“八五”期间使用的疫苗由于滴度(105.0~5.5 TCID50)较低,免疫后抗体阳转率(30%~40%)及几何平均滴度(GMT)均不高,保护率在70%~78%[6]。“九五”期间提高了规范化H2甲肝疫苗的滴度(107.0 TCID50),考核证实,单剂接种后2个月抗体阳转率可达95%,GMT=131mU/ml,3年后抗体阳转率下降至75%,4年后降至60%,但疫苗保护效果可维持在95%以上[5, 6, 9, 10]。
冻干甲肝减毒活疫苗是在规范化液体甲肝疫苗(H2株)基础上研制的一种新剂型甲肝减毒活疫苗。本文结果显示,2周岁儿童接种冻干甲肝减毒活疫苗后,抗体阳转率未随免疫年延长而改变,42个月后GMT水平更高。这可能与下列2种因素有关,一是活疫苗接种后,既能诱导体液免疫产生保护性IgG抗体,又能诱导细胞免疫,使接种对象再次接触相同的抗原时,诱导细胞介导的免疫反应,再次产生抗体升高[11-13]。二是免疫后2个月采指血检测,免后42个月采静脉血检测的程序中,可能受到指血采集时体液的影响或由于血清量不足影响,免后2个月抗体水平偏低。
本文结果提示,在甲肝流行区推广满2周岁儿童接种单剂冻干甲肝减毒活疫苗,短期内无需加强免疫。是否需要加强免疫以及加强免疫的时机需进一步的长期观察和研究[14, 15]。
| [1] | 国家知识产权局.冷冻干燥甲型肝炎减毒活疫苗及制备方法[P].2001-10-31. |
| [2] | The Committee for Standardization of Biologics of the P R China.Rrequirements for Biologics of the People's Republic of China[S].Beijing:Chemical Industry Press,2000:83-86. |
| [3] | Mao JS, Chai SA, Xie RY, et al. Further evaluation of the safety and protective efficacy of live attenuated hepatitis A vaccine (H2 strain) in humans[J]. Vaccine, 1997, 15 : 944–947. DOI:10.1016/S0264-410X(96)00304-0 |
| [4] | 庄成, 柴少爱, 陈念良, 等. 冻干甲型肝炎减毒活疫苗H2株的安全性和免疫原性研究[J]. 中国计划免疫, 2003, 9(6) : 337–339. |
| [5] | 徐志一, 汪萱怡, 李荣成, 等. 甲型肝炎减毒活疫苗免疫原性与保护效果的研究[J]. 中华医学杂志, 2002, 82(10) : 678–681. |
| [6] | 江世平, 黄全诚, 陈俊民, 等. 柳州市大规模人群甲型肝炎减毒活疫苗流行病学效果考核[J]. 中华流行病学杂志, 1995, 16(3) : 140–142. |
| [7] | 吴婉贞, 徐志一, 复家骠, 等. 甲型肝炎减毒活疫苗现场效果考核[J]. 中国公共卫生, 1996, 12(12) : 535–536. |
| [8] | 张勇, 马景臣, 韩常全, 等. 甲肝减毒活疫苗流行病学效果初步研究[J]. 中国公共卫生学报, 1994, 13(6) : 341–343. |
| [9] | 汪萱怡, 马景臣, 张勇, 等. 不同剂量甲型肝炎减毒活疫苗免疫原性与免疫持久性观察[J]. 中华流行病学杂志, 2001, 22(2) : 111–113. |
| [10] | Xu ZY, Wang XY, Li RC, et al. Preliminary results of a randomized and controlled trail of live attenuated hepatitis A vaccine[J]. Chin Med Sci J, 1999, 14(S) : 8–10. |
| [11] | Dienstage JL, Poper H, Purcell RH. The pathology of viral hepatitis A and B in chimpanzees[J]. Am J Pathol, 1976, 83 : 131–148. |
| [12] | Wang XY, Xu ZY, Yao X, et al. Immune responses of anti-HAV in children vaccinated with live attenuated and inactive hepatitis A vaccine[J]. Vaccine, 2004, 22 : 1941–1945. DOI:10.1016/j.vaccine.2003.11.007 |
| [13] | 忻亚娟, 庄成, 钱汶, 等. H2株冻干甲肝减毒活疫苗接种后血中T淋巴细胞亚群的变化[J]. 中国卫生检验杂志, 2003, 13(5) : 566–567. |
| [14] | Wang X Y, Xu Z Y, Ma J C, et al. Long-term immunogencity after single and booster dose of a live attenuated hepatitis A vaccine:Results from 8-year follow-up[J]. Vaccine, 2007, 25 : 446–449. DOI:10.1016/j.vaccine.2006.08.004 |
| [15] | Zhuang FC, Qian W, Mao ZA, et al. Persistent efficacy of live attenuated hepatitis A vaccine (H2 strain) after a mass vaccination program[J]. Chinese Medical Journal, 2005, 118(22) : 1851–1856. |
 2008, Vol. 24
2008, Vol. 24