在雄激素的作用下,胎鼠在孕13~14 d时,整个尿道板由背侧向腹侧开始融合形成完整的尿道,在此过程中涉及尿道板正常的沟渠化作用和尿生殖褶的融合,它们共同形成有管的尿道[1]。雄激素及其受体在调节基因转录过程中起重要作用[2]。在氟他胺(Flu)作用下,尿道生殖褶不能向阴茎腹侧中线融合,尿道生殖结节显示有敞开的、连续的尿道生殖沟;且上皮缝存在,显示尿生殖褶没有融合,两者共同导致尿道开口的位置异常,从而引起尿道下裂的发生。为探讨氟他胺诱导尿道下裂形成过程中相关凋亡基因的表达水平,研究其导致尿道下裂的作用机制进行了本项研究。现报道如下。
1 材料与方法 1.1 材料 1.1.1 实验动物及分组清洁(SPF)级SD大鼠60只,约8周龄,雌性40只,雄性20只,体重230~250 g(四川大学华西实验动物中心)。受孕雌鼠40只随机分为2组:对照组和Ful染毒组各20只。
1.1.2 试剂I抗:表皮生长因子(EGF)兔抗大鼠BA0250,表皮生长因子受体(EGFR)兔抗大鼠BA0820及Caspase-3兔抗大鼠BA2142(武汉博士德公司);II抗SP9000生物素化羊抗兔IgG(北京中杉金桥生物工程公司);辣根过氧化酶(DAB)显色剂,ZLI9032(北京中杉金桥生物工程公司);氟他胺、氯仿、异丙醇、75%乙醇、焦碳酸乙二(二乙)脂(DEPC)水和生理盐水均为国产试剂。样本组织mRNA提取和纯化试剂盒(美国Clontech公司)。探针标记杂交试剂盒(美国Clontech公司)。激光共聚焦Agilent扫描仪。
1.1.3 仪器OLYMPUS显微镜、Mias-200图像分析仪及Leitz-1515轮转式手摇切片机(西德Heraeus公司);Rat 12KcDNA基因表达谱芯片(上海生物芯片有限公司)。
1.2 方法 1.2.1 染毒方法清洁级SD大鼠(四川大学华西实验动物中心)60只按雌雄2:1比例配对,当日18:00合笼,次日8:00观察阴栓,观察到阴栓为孕第0 d。染毒组孕鼠在第12~17 d连续6 d,每天8:00腹部皮下注射用生理盐水配置的Flu(6.0546 mg/kg),对照组为等量生理盐水。
1.2.2 样本采集于怀孕第20 d解剖孕鼠,迅速取出染毒组和对照组雄性仔鼠双侧睾丸,将之放在装有RNA保存液的冻存管中,液氮冻存。染毒组和对照组样本mRNA提取质量鉴定各项指标符合实验要求,同时取出雄性仔鼠生殖结节,做免疫组化指标检测。
1.2.3 基因表达谱芯片检测将对照组和染毒组mRNA分别用Cy3和Cy5逆转录标记。与Rat 12KcDNA表达谱芯片杂交,筛选标准以Flu染毒组/对照组(Cy5/Cy3) 荧光强度比值>2判定为基因表达上调,<0.5为基因表达下调。
1.2.4 检测指标用免疫组化检测尿道生殖结节中表皮生长因子(EGF)、表皮生长因子受体(EGFR)及半胱氨酸天冬氨酸蛋白酶3(caspase-3) 的表达情况,用基因芯片技术检测睾丸中相关凋亡基因的表达。
1.3 统计分析应用SPSS统计软件进行t检验。
2 结果 2.1 动物染毒结果雄性子代表现出性分化和性发育异常,如尿道下裂、隐睾等。对照组尿道下裂的发生率依次为0,单侧隐睾发生率0;染毒组(6.0546 mg/kg)尿道下裂的发生率100%,单侧隐睾发生率15.56%[3]。
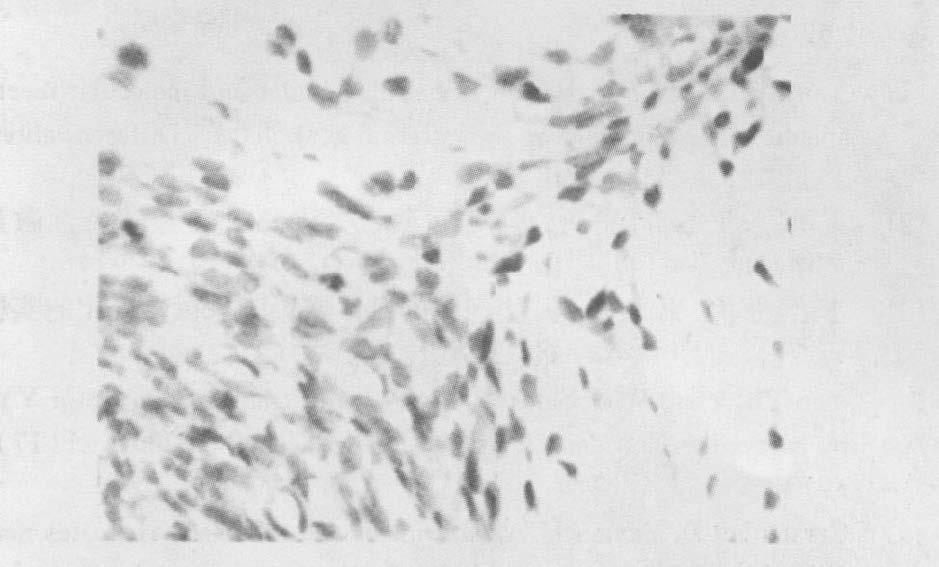
2.2 免疫组化指标检测 2.2.1 GD 20 EGF在生殖结节间充质细胞和尿道细胞中的表达(图 1~4)由图 1~4可见,在胚胎20 d,与对照组比较,染毒组EGFR在间充质细胞和尿道细胞中表达减弱。在间充质细胞和尿道细胞中EGF的表达,对照组灰度值分别为(93.74±2.0594) 和(100.184±0.66) ;染毒组依次为(110.533±2.679) 和(111.201±3.169 9) ;进行2样本均数的比较,差异有统计学意义(P<0.05) 。
|
图 1 对照组EGF 在间充质细胞中的阳性表达 |
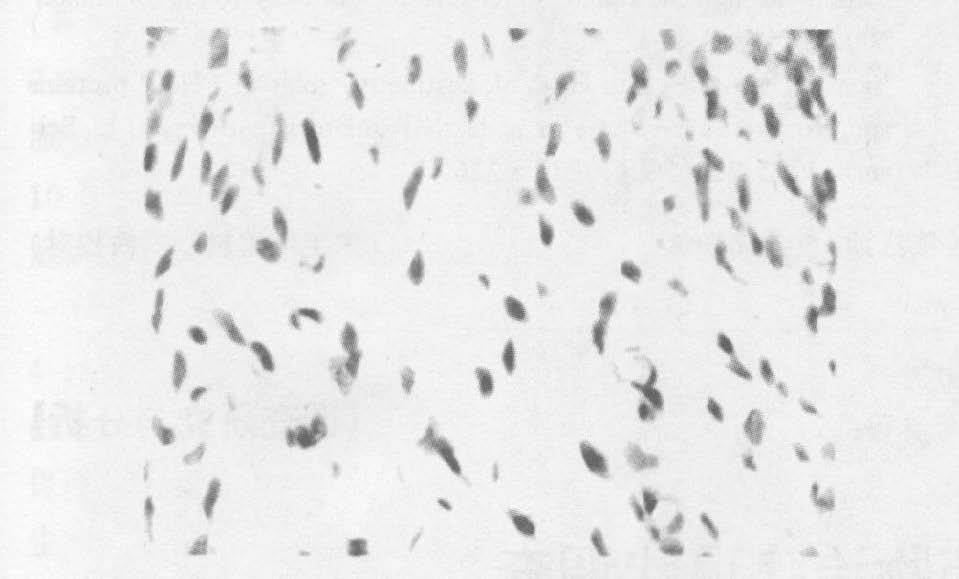
|
图 2 染毒组EGF 在间充质细胞中的阴性表达 |
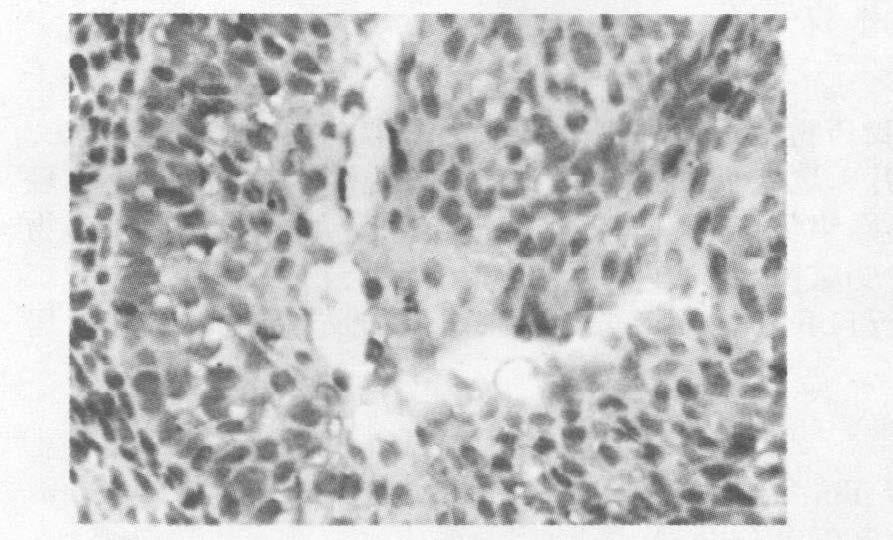
|
图 3 对照组EGF 在尿道细胞中的阳性表达 |
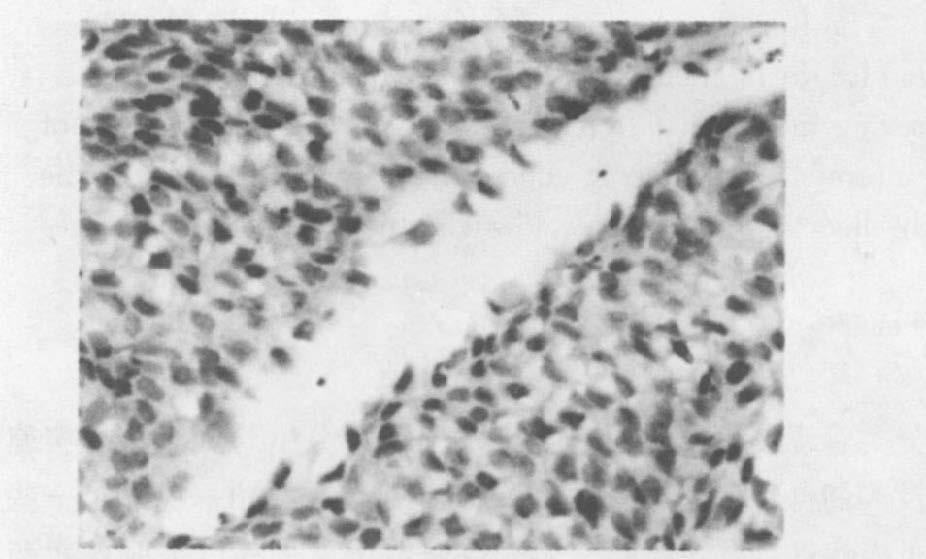
|
图 4 染毒组EGF 在尿道细胞中的阴性表达 |
2.2.2 胚胎20 d EGFR在生殖结节、间充质细胞和尿道细胞中的表达
在胚胎20 d与对照组比较,染毒组EGF在生殖结节、间充质细胞和尿道细胞中表达减弱。在生殖结节细胞、间充质细胞和尿道细胞中EGFR的表达,对照组灰度值分别为(102.922±0.805 6) ,(93.74±2.059 4) 和(94.317±0.774 8) ;染毒组依次为(113.646±0.657 5) ,(110.533±2.679 4) 和(106.952±0.952 0) ,进行2样本均数的比较,差异有统计学意义(P<0.05) 。
2.2.3 胚胎20 d caspase-3在生殖结节、间充质细胞和尿道细胞中的表达在胚胎20 d,与对照组比较,染毒组caspase-3在生殖结节、间充质细胞和尿道细胞中表达增强。在生殖结节细胞、间充质细胞和尿道细胞中Caspase-3的表达 ,对照组灰度值分别为(105.115±0.672 7) ,(97.447±3.664 4) 和(105.292±0.623 2) ;Flu染毒组依次为(90.167±1.081 7) ,(78.657±4.718 8) 和(90.167±1.081 7) ,进行2样本均数的比较,差异有统计学意义(P<0.05) .
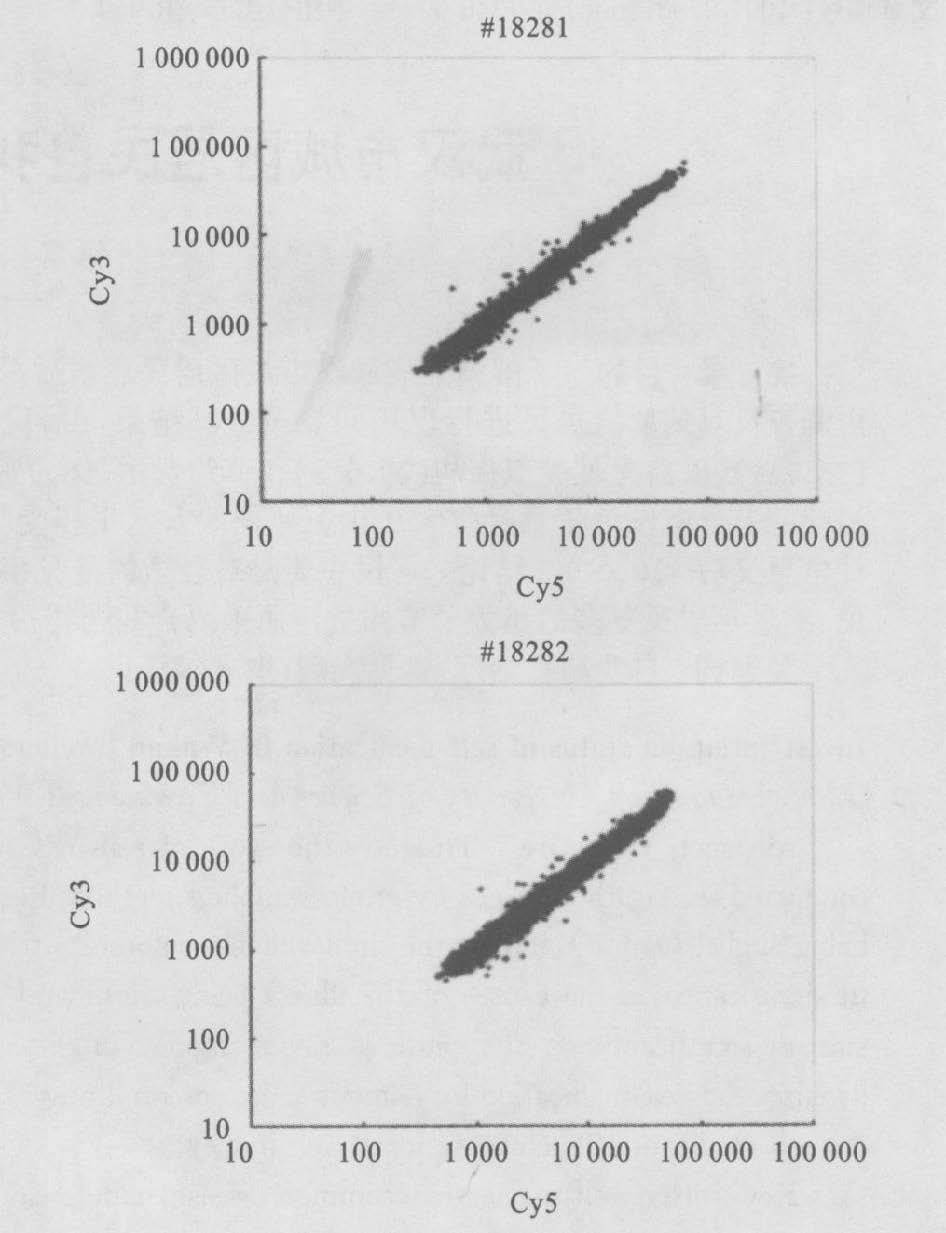
2.3 Flu染毒组与信号强度数据散点图(图 5)图中X轴、Y轴分别代表Cy3和Cy5的荧光强度值,每一个数据点代表芯片上1个基因点的杂交信号。大多数的点在Y值与X值的比值在0.5~2范围之内,只有少量的散点分布在比值范围之外,表明这些散点基因在2组可能存在差异表达。
|
图 5 杂交信号强度散点图 |
2.4 已知功能的差异表达凋亡基因
与对照组比较,染毒组有2条相关凋亡基因表达下调(即Cy5/Cy3<0.5) ,有1条相关凋亡基因表达上调(即Cy5/Cy3>2.0) 。用基因库ID(Genbank_ID)表达:AK007561 Ras相关的C3肉毒毒素底物2(RAS-related C3 botulinum substrate 2) 基因、AW521361 YY1转录因子(YY1 transcription factor)、NM_021740a前胸腺素(prothymosin alpha);其比率(Ratio)分别为0.377,0.479,4.282。
3 讨论EGF、EGFR对胚胎向雄性方向发展及雄性生殖器官的分化、发育起着促进作用。本次实验结果表明,与对照组比较,EGF、EGFR在生殖结节、间充质细胞和尿道细胞胞浆(主)或胞膜中表达减弱;导致胎儿前尿道发育不全而使尿道异位开口于阴茎腹侧或会阴部。
实验表明,caspase-3为caspase家族中的凋亡执行因子,是导致细胞凋亡的最强大的最终效应因子。本次实验结果表明,与对照组比较,caspase-3在生殖结节、间充质细胞和尿道细胞胞浆中表达增强;使这些正常部位的细胞发生凋亡,阻碍了尿道板正常的沟渠化作用和尿道生殖褶的融合。
Yao YL等[4]实验证明,正常表达的YY1能够抑制细胞内c-Fos、Fas、p53和c-myc等凋亡基因的表达。Carstanjen等[5]研究证实,Rac2可以抑制超氧化物产生,保护细胞不被过氧化物所损伤。Jiang等[6]发现,在细胞凋亡形成后能够提高caspase-9的活性,而Ptma参与抑制细胞凋亡的形成,对caspase-9的活性进行负性调控。本次实验结果提示,Flu不但使睾丸生殖细胞受到超氧化物的袭击,而且促进了睾丸生殖细胞发生凋亡。
实验表明,Flu染毒能够在性发育期干扰子代雄鼠尿生殖结节和睾丸组织中相关凋亡基因的表达水平,导致子代雄性大鼠尿道下裂的发生,从而为进一步研究尿道下裂发病的分子机制提供了重要的实验依据。
| [1] | Yamada G, Satoh Y, Baskin LS, et al. Cellular and molecular mechanisms of development of the external genitalia[J]. Differentiation, 2003, 71(8) : 445–460. DOI:10.1046/j.1432-0436.2003.7108001.x |
| [2] | 王洪军, 王继群, 田庚, 等. 雄性激素受体mRNA表达及性激素与增龄的关系[J]. 中国公共卫生, 2003, 19(8) : 938–939. |
| [3] | 李岩, 张浩, 王文冬, 等. 小剂量的氟他胺影响大鼠性分化的实验研究[J]. 四川大学学报: 医学版, 2006, 37(2) : 258–261. |
| [4] | Yao YL, Yang WM, Seto E. Regulation of transcription factor YY1 by acetylation and deacetylation[J]. Mol Cell Biol, 2001, 21(17) : 5979–5991. DOI:10.1128/MCB.21.17.5979-5991.2001 |
| [5] | Carstanjen D, Yamauchi A, Koornneef A, et al. Racregulates neutrophil chemotaxis,superoxide production,and myeloid colony formation through multiple distinct effector pathways[J]. J Immunol, 2005, 174(8) : 4613–4620. DOI:10.4049/jimmunol.174.8.4613 |
| [6] | Jiang X, Kim HE, Shu H, et al. Distinctive roles of PHAP proteins and prothymosin-alpha in a death regulatory pathway[J]. Science, 2003, 299(5604) : 223–226. DOI:10.1126/science.1076807 |
 2008, Vol. 24
2008, Vol. 24

