2. 辽宁大学生命科学院生物化学教研室;
3. 沈阳农业大学食品学院;
4. 沈阳国家新药安全评价中心;
5. 沈阳三生制药有限公司
随着农药的种类和用量逐年增加,释放于环境中的农药不仅带来了环境污染和生态平衡问题,而且也对人类健康造成潜在危害。流行病学资料显示,肿瘤发生率的增长与使用农药的农产品密切相关[1]。因此,研究农药的遗传毒性具有重要意义。粉唑醇具有内吸性,在植物体内传导,对病害有保护和治疗作用。可防治禾谷类作物白粉病、长蠕孢属、柄锈菌属、壳针菌属病原菌等,对谷物白粉病有特效。本文通过慧星试验、Ames试验、小鼠骨髓嗜多染红细胞微核试验研究粉唑醇的遗传毒性,为评价粉唑醇对生态系统的影响及其合理安全使用提供科学依据。
1 材料与方法 1.1 主要试剂粉唑醇,化学名称为α-(2-氟苯基)(4-氟苯基)-1氢-1,2,4-三唑-1-乙醇(兴农股份有限公司提供,纯度95%)。二甲基亚砜(DMSO),二氨基芴(2-AF),甲基磺酸甲酯(MMS),TritonX-100, 溴化乙锭(EB)(美国Sigma公司)。环磷酰胺(CP),丝裂霉素C (上海华联制药有限公司)。小牛血清(上海普飞生物有限公司)。
1.2 实验菌株和培养基实验菌株为组氨酸营养缺陷型鼠伤寒沙门菌TA97、TA98、TA100和TA102菌株(沈阳国家新药安全评价中心遗传毒理实验室),经鉴定各项遗传特性均符合实验要求,菌株增菌、基因型鉴定及各种试验用培养基均按标准操作[2]。
1.3 实验动物健康ICR小鼠100只,雌、雄各半,体重(25±2) g (中国科学院上海实验动物中心),常规喂养,观察1周后使用。
1.4 实验方法(1) Ames试验:采用标准平皿掺入法[2],依照文献[3]方法。(2) 小鼠骨髓嗜多染红细胞(PCE) 微核试验:依照文献[3]方法。取ICR小鼠5mg/kg 3个受试农药剂量组,1个阳性对照组(环磷酰胺,剂量为50 mg/kg),1个阴性对照组(DMSO)。(3) 慧星试验:动物分组、染毒依照文献[3]方法。取材依照文献[4]方法。慧星试验依照文献[5]方法并略加改进[4]。荧光显微镜下用515~560 nm的激发光观察,在200×下每只动物计数100个慧星图像,用CASP (Comet Assay Software Project) 图像分析软件测定尾长、尾部面积、尾部DNA含量、尾矩(TM)。
1.5 统计分析应用SPSS 11.5软件进行统计分析。
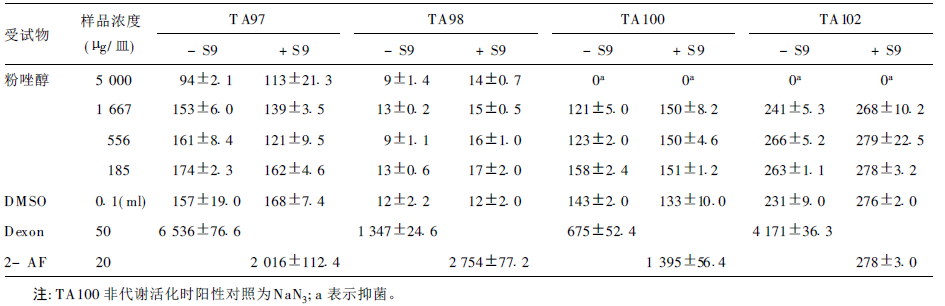
2 结果 2.1 Ames试验结果(表 1)从表 1可见,粉唑醇Ames试验,各菌株在5 000 μg/皿剂量组出现抑菌,各剂量组无论是否代谢活化,细菌回变数小于阴性对照组细菌回变数的2倍。且无剂量-效应关系,皆为阴性试验结果。结果表明,在本试验条件下,粉唑醇无诱导微生物基因突变的能力。
| 表 1 粉唑醇对鼠伤寒沙门菌体外回复突变试验结果(x±s) |
2.2 小鼠嗜多染红细胞微核试验结果
粉唑醇小鼠嗜多染红细胞微核试验中,雄性小鼠80,40,20 mg/kg 3个受试农药剂量组诱导的微核发生率分别为(1.4±0.53) ‰,(1.6±0.88) ‰,(2.0±0.71) ‰,与阴性对照组诱导的微核发生率(1.4±0.54) ‰比较,差异均无统计学意义(P>0.05)。阳性对照组的微核发生率为(14.8±3.10) ‰,与阴性对照组比较,差异有统计学意义(P<0.01)。雌性小鼠80,40,20 mg/kg 3个受试农药剂量组诱导的微核发生率分别为(1.8±0.46) ‰,(1.8±0.83‰),(1.6±0.88) ‰,与阴性对照组诱导的微核发生率(1.8±0.43) ‰比较,差异均无统计学意义(P>0.05)。阳性对照组的微核发生率为(17.2±2.87) ‰,与阴性对照组比较,差异有统计学意义(P<0.01)。同时各试验组PCE/正染红细胞(NCE) 的比值均在正常值范围内(正常比值范围:0.60~1.20),试验结果为阴性。表明在本试验条件下,粉唑醇对ICR小鼠无诱发PCE微核率增高作用,即粉唑醇无诱导染色体损伤的能力。
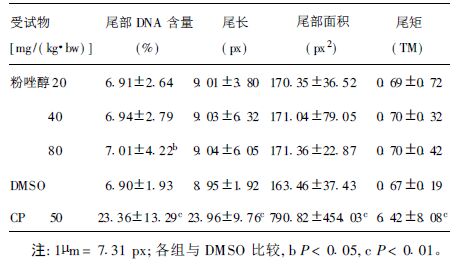
2.3 慧星试验结果(表 2)从表 2可见,粉唑醇慧星试验,随着粉唑醇浓度的升高,小鼠骨髓细胞慧星尾长、尾部DNA含量、尾部面积和尾矩都呈现增加趋势,其中剂量80mg/(kg·bw) 时,尾部DNA含量与阳性对照组比较,差异有统计学意义(P<0.05),而其他评价指标与阳性对照组比较,差异无统计学意义。试验结果总的趋势是随着粉唑醇浓度的升高,细胞受损度增高,但无明显的阳性反应,得出粉唑醇在试验剂量范围内不能引起小鼠骨髓细胞的DNA损伤。使用台盼兰进行细胞存活率测定时,试验前细胞存活率均在95%以上,染毒后的细胞存活率也在90%以上,说明DNA损伤为受试物作用所致,而非细胞毒性。
| 表 2 粉唑醇慧星试验结果(x±s) |
3 讨论
农药注册要求对化合物潜在遗传毒性进行综合评价,但单一试验尚不能检测所有的遗传毒性化合物,因此,常用的方法是进行一组遗传毒性体外和体内试验,这些试验相互补充而不是代表不同的等级水平。在本次试验中,选用Ames试验、小鼠骨髓嗜多染红细胞微核试验、慧星试验这一组遗传毒理学试验,从不同的遗传学终点角度,对粉唑醇的遗传毒性进行分析。3项试验结果均为阴性,表明在本次实验条件下,该受试物未显示有遗传毒性作用,为该农药的遗传毒性评价提供了相关依据。但长期低剂量反复接触是否有蓄积作用及远期效应,需要进一步研究。
| [1] | 李小燕, 陈贤均. 三种常用农药的遗传毒性和细胞毒性研究现状[J]. 中国预防医学杂志, 2004, 5(2) : 157–159. |
| [2] | 毛德寿, 周宗灿, 王志远. 环境生化毒理学[M]. 沈阳: 辽宁大学出版社, 1986: 307-319. |
| [3] | 付保荣, 曹向宇, 惠秀娟, 等. 杀虫剂杀螟丹遗传毒性检测[J]. 中国公共卫生, 2007, 23(7) : 809–810. |
| [4] | 曹向宇, 惠秀娟, 马汐平, 等. 激素类除草剂二氯喹啉酸遗传毒性比较[J]. 中国公共卫生, 2006, 22(3) : 333–334. |
| [5] | A Hartmann, E Agurll, C Beevers, et al. Recommendations for conducting the in vivo alkaline comet assay[J]. Mutagenesis, 2003, 18(1) : 45–51. DOI:10.1093/mutage/18.1.45 |
 2008, Vol. 24
2008, Vol. 24