近年来,幽门螺杆菌(Helicobacter pylori,Hp)疫苗的研究主要集中在尿素酶(Ure)、细胞相关毒素(CagA)、热休克蛋白60(HSP60)等抗原上,但由于保护率和安全性上存在一定缺陷,目前尚无可应用于临床的Hp疫苗[1] 。Hp是胃肠道感染细菌,黏膜免疫在抗Hp感染上发挥着核心作用,黏附素在Hp定植过程中不可或缺,已成为具有广阔应用前景的疫苗候选抗原。从Hp的多种黏附素中筛选保护性抗原,通过激发黏膜免疫,阻断Hp的黏附和定植,是未来Hp疫苗研究的主要方向。hp0410属于幽门螺杆菌主要黏附素hpaA基因家族同系成员,编码产物可能为N-乙酰神经氨酰乳糖结合原纤维血凝素(N-acetylneuraminyl-lactose-binding haemagglutinin,NLBH)的亚单位[2],NLBH在Hp的黏附和定植过程中发挥重要作用,抗NLBH抗体能抑制Hp的黏附[3]。HP0410是Hp的特有蛋白,保守性高,与其他物种的同源性很低,有望作为幽门螺杆菌候选疫苗。本研究在克隆表达HP0410的基础上,利用抗HP0410单抗E018和12肽噬菌体展示技术[4, 5],获得HP0410的模拟表位,为构建Hp嵌合表位口服疫苗提供了基础依据。现将结果报告如下。
1 材料与方法 1.1 材料(1)菌株与培养基:大肠埃希菌ER2738来自12肽噬菌体展示库试剂盒;重组大肠埃希菌采用脂质双层(LB)培养基。(2)实验试剂:辣根过氧化物酶(HRP)-羊抗鼠IgG(武汉博士德公司),一管式PCR反应体系和四甲基联苯胺(TMB)可溶性单组分底物(北京天为时代公司);12肽噬菌体展示库试剂盒(新英格兰BioLabs公司);异丙基-B-D-硫代乳糖苷(IPTG)、X-gal、氨苄青霉素和四环素(广州威佳公司);谷胱苷肽-S-转移酶(GST)纯化试剂盒(上海生工公司);限制性内切酶BamHI和EcoRI(日本TaKaRa公司)。
1.2 方法 1.2.1 hp0410扩增与克隆设计用于扩增hp0410(GenBank NO.AAD07478.1)的引物,由日本TaKaRa公司合成,引物序列如下:R:5′-CGCTAAAAAAACTCACATCGG;F:5′- CATTACCTCTAAACCACCCAGGAACG。利用以上引物和一管式PCR反应体系,从Hp NCTC11639基因组DNA中扩增出hp0410。
1.2.2 酶切鉴定扩增产物纯化后,连入T载体pMD-18T,转入大肠埃希菌TOP10感受态细胞中,37℃在含有X-gal的平板上培养14h,利用Amp抗性和蓝白斑筛选出白色重组菌落,微量PCR鉴定及双酶切鉴定并送交TaKaRa进行重组质粒测序鉴定。从重组pMD18-T中双酶切下hp0410,克隆入表达载体pGEX-4T-1中,转化入大肠杆菌BL21感受态细胞中,Amp抗性平板培养基上筛选阳性克隆,进行PCR以及BamH I和EcoR I双酶切鉴定。
1.2.3 HP0410表达与纯化按优化诱导条件,150 r/min 30℃下0.05 mmol/L IPTG诱导4h,大量诱导表达HP0410,GST柱纯化重组蛋白,并进行SDS-PAGE鉴定。
1.2.4 抗HP0410单克隆抗体的筛查4℃下100mg/ml HP0410包被,10%牛血清白蛋白(BSA)的碳酸盐缓冲液(CBS),37℃封闭,用0.5%聚丁二酸丁二醇酯(PBST)冲洗6次,拍干残液,加入待筛查单克隆抗体1:100稀释液,37℃结合1h,0.5%PBST 冲洗6次,拍干残液,加入1:10000稀释HRP-羊抗鼠37℃结合1h,0.5%PBST冲洗6次,拍干,加入TMB底物显色10min,2 mol/L硫酸终止反应,450nm下酶标仪读数。
1.2.5 噬菌体展示库筛选与扩增利用筛查到的1株小鼠单抗IgG1(E018) 100μg/ml浓度,筛查12肽的M13噬菌体。获得的噬菌体用浓度为10和1 μg/ml的E018继续进行2轮筛选。从第3次筛选滴定的X-gal-IPTG平板上,随机挑取40个蓝色噬斑,大量扩增并提纯单克隆噬菌体。
1.2.6 噬菌体的ELISA鉴定每孔10μg/ml E018,100μl作为包被液,并每孔设空白对照,阴性对照为ER2738菌。4℃潮湿环境孵育过夜。加入封闭液4℃1h,0.1%三羟甲基氨基甲烷缓冲液(TBST)洗板6次,拍干。加入用TBS1:2稀释的单克隆噬菌体扩增产物,每孔100μl,室温振荡1h,0.3%TBST洗板6次,拍干。加入1:5000稀释的HRP标记噬菌体抗体100μl,室温振荡1~2h,0.5%TBST洗板6次,拍干。加入100μl可溶性TMP底物,37℃避光反应10min,用2 mol/L硫酸终止反应,450nm处读取吸光度(A)值。
1.2.7 单克隆M13噬菌体单链DNA提取和测序分别提取各株单克隆噬菌体的DNA并由美国Invetrogen公司测序。
1.2.8 竞争抑制实验每孔100μl的10μg/ml E018共6孔,4℃包被过夜,加入封闭液4℃1h,0.1%TBST洗板6次,拍干。每孔加入100μl展示候选表位的噬菌体扩增液,并按顺序分别加入0,20,40,60,80,100μl浓度为100μg/ml的HP0410,混匀,室温振荡1h,0.3%TBST洗板6次,拍干。每孔加入1:5000稀释的HRP标记噬菌体抗体100μl,室温振荡1~2h,0.5%TBST洗板6次,拍干。加入100μl可溶性TMP底物,37℃避光反应10min,用2 mol/L硫酸终止反应,450nm处读取吸光度(A)值。
1.3 生物信息学分析利用www.Ncbi.nlm.nih.gov网站上的BLAST工具对hp0410进行同源性搜索和分析。利用harvard大学在线抗原性预测软件对HP0410进行抗原表位预测(http://bio.dfci.harvard.edu/Tools/antigenic.html),利用在线软件Rankpep (http://bio.dfci.harvard.edu/Tools/rankpep.html)预测HP0410可与人HLAⅡ类分子紧密结合的结构域。
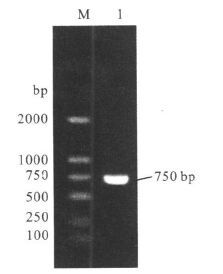
2 结果 2.1 hp0410的扩增和克隆从幽门螺杆菌NCTC11639基因组中扩增出hp0410,PCR产物经0.7%琼脂糖凝胶电泳鉴定,片段大小为750bp,与预测相符(图 1)。PCR产物连入pMD18-T中测序,与基因库(GenBank)上的Hp标准株22695和J99对应序列比对,DNA序列同源性分别为95.07%和94.96%,氨基酸序列同源性则分别为94%和96%。克隆入pGEX-4T-1后,重组质粒经双酶切鉴定获得2个DNA条带,片段大小与预期相符(图 2)。
|
注:M:DL2000 DNA marker;1:Hp0410。 图 1 hp0410PCR扩增 |
|
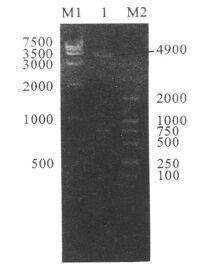
注:M1:DL7500DNA marker;1:BamH I和EcoR I双酶切重组pGEX-4T-1;M2:DL2000 DNA marker。 图 2 重组pGEX-4T-1双酶切鉴定 |
2.2 HP0410的表达和纯化
诱导表达HP0410,菌体裂解上清液SDS-PAGE鉴定(图 3)。结果表明,HP0410主要以可溶性形式表达,上清液中蛋白水平较高。GST柱纯化重组蛋白,对未纯化的裂解上清液、洗脱液、GST糖珠分别进行SDS-PAGE,鉴定纯化效果(图 4)。
|
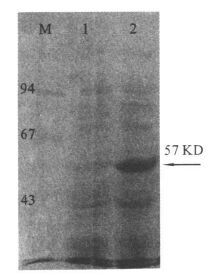
注:M:Low MW protein marker;1:诱导前HP0410;2:重组HP0410。 图 3 上清液SDS-PAGE鉴定 |
|
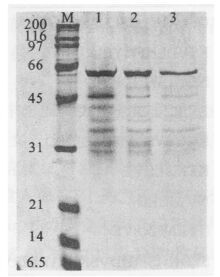
注:M:Low MW protein marker; 1:上清液;2: GST糖珠;3:洗脱液。 图 4 HP0410纯化 |
2.3 噬菌体富集分析
3次筛选的噬菌体投入量都为1.5×1011,而3次回收量分别为2.93×107,2.28×109及3.02×106。第3次筛选因未经扩增,故获得的噬菌体滴度较低,而前2次回收的噬菌体量有明显的增加趋势,表明阳性噬菌体已获得富集和扩增。
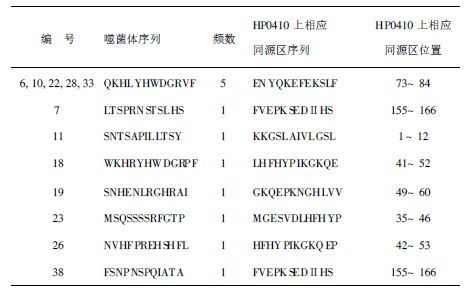
2.4 阳性噬菌体ELISA鉴定与测序经过3轮筛选,从最后滴定的平板上随机挑取40个克隆,扩增后ELISA鉴定获得25个阳性克隆。提取其中与E018结合特异性最高,吸光度(A450)>2的14株噬菌体进行DNA并测序。结果显示,14株噬菌体得到8个表位,其中有5株的氨基酸序列完全相同,提示其展示的是与E018亲和力最高的肽段,相应的HP0410同源区可能为E018特异性结合的抗原决定基。因此该序列应为HP0410的候选抗原表位之一。候选表位的HP0410同源区与预测的第1号HLAⅡ类分子结合结构域位置基本一致,提示该表位展示的是可以与HLAⅡ类分子结合的抗原决定基。噬菌体展示序列的HP0410同源区主要集中在第40~60,70~85和150~170位aa 3个区域,与生物信息学预测的高抗原性区域相符,提示这3个区域的肽段为HP0410的高抗原性区域,获得的表位是可被HLAⅡ类分子识别并提呈的抗原表位(表 1)。
| 表 1 噬菌体序列分析与同源性比较 |
2.5 HP0410的抗原表位分析
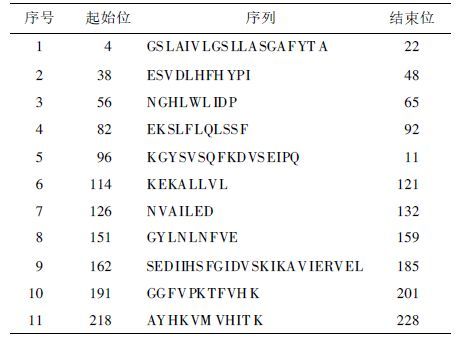
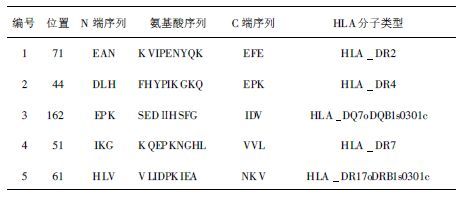
用Kolaskar和Tongaonkar方法和Hopp-Woods方法进行抗原性预测(表 2)。结果表明,HP0410的第30~60,70~90和160~185位氨基酸(aa)具有较高的抗原性,同时预测的HLAⅡ类分子结合结构域(表 3)都处在这些高抗原性区域内,提示这些肽段可能为良好的高抗原性表位。
| 表 2 HP0410高抗原性肽段 |
| 表 3 HP0410的HLAⅡ类分子结合结构域预测 |
2.6 HP0410对展示候选表位噬菌体的竞争-抑制实验
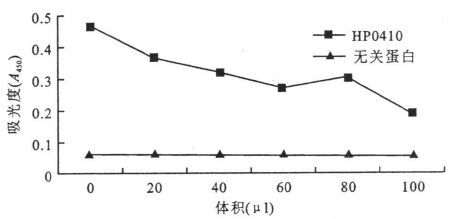
随着HP0410浓度的增加,展示候选表位的噬菌体与E018的结合明显受到抑制(图 5),提示HP0410与噬菌体竞争性结合到E018可变区上,噬菌体所展示的模拟空间构象表位和E018特异性结合的HP0410的抗原决定基因十分相似。
|
图 5 HP0410对唑菌体克隆-6的竞争抑制 |
3 讨论
噬菌体表面展示技术(phage display)是一种将外源蛋白与噬菌体衣壳蛋白融合展示在噬菌体表面的生物技术。该技术广泛应用于抗原表位分析[4] 、蛋白质相互作用以及筛选鉴定单克隆抗体等[5],可为表位疫苗的研制提供理论依据。研究发现,Hp疫苗可诱导起保护作用的Th2型免疫应答[6],但在MHCⅡ类分子缺失的小鼠中无法诱导出保护性免疫反应[7],表明CD4+ T淋巴细胞在抗Hp免疫应答中发挥非常重要的作用,只有能被参与外源性抗原提呈的MHCⅡ类分子结合并提呈的Hp疫苗候选抗原才能有效地激发抗Hp免疫应答。
本研究克隆并表达了幽门螺杆菌黏附素HP0410,采用生物信息学方法对其进行抗原性预测,表明HP0410的第40~50,70~90和160~180位氨基酸(aa)具有较高的抗原性。通过噬菌体展示技术获得了8个抗原表位,其中1个为模拟单抗E018识别的抗原决定基的候选表位。展示的多肽与HP0410的同源性不高,提示展示的可能为HP0410的模拟空间表位,而非线性表位。以上肽段的HP0410同源区与预测的HLAⅡ类分子结合结构域一致,提示这些区域可被HLAⅡ类分子识别并提呈,进而激发保护性免疫应答。综合噬菌体肽库结果与生物信息学预测,表明HP0410的第40~50、70~90和160~180位aa为高抗原性区域,HP0410的HLAⅡ类分子结合结构域恰好位于这3个区域内,提示这些区域可为HLAⅡ类分子识别并提呈,从而有效地激发免疫应答。
本研究获得的HP0410的3个抗原表位具有较高的抗原性,很可能可激发宿主的Th2型保护性免疫应答,提示HP0410是具有应用前景的幽门螺杆菌候选疫苗抗原。拟通过合成多肽免疫SPF小鼠以确证这些表位的免疫保护效果,为构建嵌合表位重组疫苗提供理论依据,并为研制针对黏附素的Hp口服疫苗奠定研究基础。
| [1] | 李丙生, 周曾芬. 幽门螺旋杆菌疫苗的研究现状[J]. 胃肠病学和肝病学杂志, 2004, 13(2) : 203–205. |
| [2] | Richard A Alm, James Bina, Beth M Andrews, et al. Comparative genomics of Helicobacter pylori:Analysis of the outer membrane protein families[J]. Infection and Immunity, 2000, 68(7) : 4155–4168. DOI:10.1128/IAI.68.7.4155-4168.2000 |
| [3] | Yan J, Y F Mao, Z X Shao. Frequencies of the expression of main protein antigens from Helicobacter pylori isolates and production of specific serum antibodies in infected patients[J]. World J Gastroenterol, 2005, 43 : 450–454. |
| [4] | Roberto Di Niro, Federica Ziller, Fiorella Florian, et al. Construction of miniantibodies for the in vivo study of human autoimmune diseases in animal models[J]. BMC Biotechnol, 2007, 7 : 46. DOI:10.1186/1472-6750-7-46 |
| [5] | Darly J Manayani, Diane Thomas, Kelly A Dryden, et al. A viral nanoparticle with dual function as an anthrax antitoxin and vaccine[J]. PLoS Pathog, 2007, 3(10) : e142. DOI:10.1371/journal.ppat.0030142 |
| [6] | Ghiara P, Rossi M, Marchdetti M, et al. Therapeutic intragastric vaccination against Helicobacter pylori in mice eradicates an otherwise chronic infection and confers protection against reinfection[J]. Infect Immun, 1997, 65 : 4997–5002. |
| [7] | Pappo J, Torrrey D, Gastriottal L, et al. Helicobacter pylori infection in immunized mice lacking major histocompatibility complex class I and class II function[J]. Infect Immun, 1999, 67 : 337. |
 2008, Vol. 24
2008, Vol. 24