2. 日本鹿儿岛大学医齿学综合研究科环境医学研究室;
3. 广西医科大学医学科学实验中心
微囊藻毒素污染与人类健康的关系问题已引起全球的广泛关注。微囊藻毒素-LR (microcystin-LR ,MCLR)是一种具有肝脏毒性的单环多肽毒素,是微囊藻毒素中毒性最强的一种。研究表明,MCLR 可以增加细胞内的活性氧(reactiveoxygen species ,ROS)的形成[1]。Ding 等[2]报道,MCLR 引起原代培养大鼠肝细胞产生DNA 链的断裂损伤。DNA 链的断裂损伤有很多种原因,因此,它不是ROS 引起的特异性的氧化性DNA 损伤标志物[3]。8-羟基脱氧鸟嘌呤核苷(8-O-HdG)是ROS 攻击DNA 分子中的鸟嘌呤碱基第8 位碳原子而产生的一种氧化性加合物,它是氧化性DNA 损伤中主要的和最重要的标志物[4]。有机阴离子转运多肽(OATP)家族的OATP1B1 和OATP1B3 是特异性分布于肝细胞基底外侧(窦状)质膜上的转运蛋白,负责介导胆酸盐等物质的跨细胞转运[5]。本研究选取高表达OATP1B1 的HT17 细胞株和不表达OATP1B1 或1B3 的Hep G2 细胞株[5],比较2 种人肝癌细胞株对MCLR 的毒性差异,利用较敏感的细胞株进一步研究MCLR 对人类细胞的氧化性DNA 损伤作用。
1 材料与方法 1.1 细胞和主要试剂HT17 细胞和Hep G2 细胞(日本东北大学老年医学研究所细胞资源中心惠赠)。MCLR 纯度>98 %(瑞士AL EXIS 公司),临用时用0.1 %二甲基亚砜溶解。二甲基亚砜(DMSO)(日本和光纯化学工业公司);鼠抗8-O2HdG单克隆抗体IF7 (美国R & D Systems 公司);过氧化物酶试剂盒和3 ,3′2 二氨基联苯胺(DAB)试剂盒(美国Vector Laboratories 公司);四甲基偶氮噻唑蓝(MTT)(日本同仁化学研究所);青霉素和链霉素(美国Gibco-BRL 公司);伊格尔最低必需培养基(MEM)和改良的伊格尔(DMEM)培养基(美国Sigma 公司)。
1.2 细胞培养和染毒HT17 细胞在含10 %加热失活小牛血清及100U/ ml 青霉素、100μg/ ml 链霉素,于MEM 培养基中,置37 ℃,5 % CO2 和95 % O2 条件下培养。Hep G2 细胞用DMEM培养基培养,培养条件同前。收集对数生长期细胞,调节细胞数为2 ×105/ ml ,培养24 h 后,换成含有不同剂量MCLR 的培养液继续培养,培养24 h 后,在倒置显微镜下观察细胞形态和生长情况。
1.3 MTT 法检测细胞毒性HT17 细胞和Hep G2 细胞以每孔1 ×104 个分别接种于96 孔板,培养24h 后,加入MCLR ,使毒素的浓度为0.2 ,0.5 ,1.0 ,2.0 和5.0μg/ ml ,并以0.1 %DMSO 作空白对照,每个剂量组设2 个平行样,继续培养24 h后,每孔加50μl MTT ,37 ℃继续孵育3 h ,小心吸尽孔板中的培养液,加入100μ1 DMSO ,室温下摇床振荡5 min 后,用酶标仪(日本Tosoh 公司)测定570 nm 波长处的吸光度(A )值。细胞存活率= (实验孔A 值/ 对照孔A 值)×100 %。
1.4 免疫酶染色法检测8-OHdG主要参照文献[6]的方法并稍作改进。
1.5 统计分析采用SPSS 11.0 统计软件处理数据。细胞毒性测定和8-OHdG含量测定分别采用方差分析的Tukey检验和Dunnett’s T3 检验。
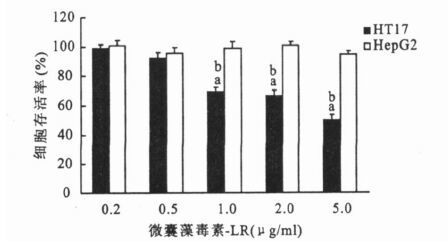
2 结 果 2.1 HT17 和Hep G2 细胞对MCLR 的毒性反应(1) 在倒置显微镜下观察发现,当MCLR 的剂量增加到1.0μg/ ml 时,HT17 出现细胞收缩、变圆,失去正常细胞间的紧密连接,呈悬浮生长,一些细胞脱离培养基后,凝集成团块状,细胞核变得模糊不清,活细胞数量减少。与之相反,Hep G2 细胞贴壁稳定生长,细胞间相互紧密连接。细胞形态呈梭形,核圆、清晰。(2)用MTT 法定量检测细胞毒性时发现,不同剂量的MCLR处理HT17 细胞24h 后,低剂量处理(≤0.5μg/ ml)未见细胞毒性。但随着处理浓度的增加,HT17 细胞存活率显著降低,存在明显的剂量-反应关系。最高剂量组(5.0μg/ ml )的HT17 细胞存活率是对照组的(50.42 ±3.98)%。在1.0 ,2.0和5.0μg/ ml 3 个剂量点上,HT17 细胞的存活率均明显低于Hep G2 细胞。与空白对照组比较,Hep G2 细胞的存活率在任一剂量点上均无显著改变(图 1)。
|
注:与空白对照组比较,a P<0.01 ;与HepG2 组比较,b P<0.01 。 图 1 不同剂量MCLR处理HT17 和HepG2 细胞的毒性效应 |
2.2 MCLR 对HT17 细胞氧化性DNA 损伤的作用
用免疫酶染色法检测HT17 细胞内8-OHdG时发现,8-OHdG染色主要位于细胞核内。在空白对照组细胞可以观察到清楚的本底,呈浅棕色,而0.2~2.0μg/ ml MCLR 处理后的细胞核呈现明显的深棕色。利用图像分析软件进行定量,0.2 ,0.5 ,1.0和2.0μg/ ml 剂量组的8-OHdG 染色强度值分别为0.42 ±0.04 ,0.46 ±0.05 ,0.48 ±0.04 和0.55 ±0.08 。非毒性剂量(0.2 和0.5μg/ ml)MCLR 处理的细胞8-OHdG染色强度明显高于空白对照组(0.34 ±0.02),(P<0.01),且随处理剂量的增加,8-OHdG 的染色强度亦增加。表明随着MCLR 处理剂量的增加,细胞内的8-OHdG含量亦增高。
3 讨 论MCLR 是一种毒性很强的肝毒素,能强烈抑制细胞丝氨酸苏氨酸蛋白磷酸酶(proteinp hosphatases ,PP)PPl 和PP2A 的活性,打破细胞内蛋白磷酸化/ 脱磷酸化的平衡,产生细胞毒性作用[1]。本研究发现,1μg/ ml 以上剂量的MCLR 能抑制HT17 细胞的增殖与活性,这个毒性剂量范围与原代培养大鼠肝细胞相近[7]。高表达OATP1B1 的HT17 细胞对MCLR的敏感性高于不表达OATP1B1 或OATP1B3 的Hep G2 细胞,这与Monks 等[5]采用表达OATP1B1 和OATP1B3 的HeLa 转染细胞检测MCLR 毒性的结果一致,提示OATP1B1介导MCLR 的转运在MCLR 毒性发挥中起非常重要的作用。Hep G2 和HL60 等细胞不表达OATP1B1 或OATP1B3 ,MCLR 不容易进入细胞产生毒性作用。
本研究采用免疫酶染色法检测细胞内8-OHdG 的含量。此法不用对DNA 进行分解处理,不需要较昂贵的仪器,特异性强。单克隆抗体IF7 对8-OHdG的特异性已为竞争性EL ISA 实验所证实。免疫酶染色法与高效液相色谱-电化学检测器分析(HPLC-ECD)法之间有非常好的线性关系,可以避免DNA 分解处理过程中导致的假阳性结果[6]。本研究发现,MCLR 处理HT17 细胞24 h 后,引起8-OHdG水平明显升高,染毒量与8-OHdG 水平之间呈现剂量-反应关系,提示MCLR 能引起细胞氧化性DNA 损伤。非毒性剂量的MCLR 亦诱导8-OHdG 的形成,提示观察到的氧化性DNA 损伤可能不是继发于细胞毒性。
在复制过程中,DNA 链上的8-OHdG可以与C 以外的其他碱基配对,引起G:C-T :A 颠换突变,在基因突变、细胞癌变以及肿瘤生长中起着重要作用[7]。非毒性剂量的MCLR 引起氧化性DNA 损伤提示长期接触低剂量的MCLR可能对人类健康产生潜在的远期危害,因此,应加强环境水体的中微囊藻毒素-LR 的监测。
| [1] | 蒋智华, 张志勇. 微囊藻毒素诱导细胞凋亡研究进展[J]. 中国公共卫生, 2007, 23(2) : 241–243. |
| [2] | Ding WX, Shen HM, Zhu HG, et al. Genotoxicity of microcystic cyanobacteria extract of a water source in China[J]. Mutat Res, 1999, 442(2) : 69–77. DOI:10.1016/S1383-5718(99)00064-9 |
| [3] | Takeuchi T, Nakajima M, Morimoto K. Relationship between the intracellular reactive oxygen species and the induction of oxidative DNA damage in human neutrophil-like cells[J]. Carcinogenesis, 1996, 17(4) : 1543–1548. |
| [4] | 刘爱林, 邹亚玲, 鲁文红, 等. 焦炉工人血清谷胱甘肽硫转移酶活力和尿8-羟基脱氧鸟苷水平[J]. 中华劳动卫生职业病杂志, 2005, 23(5) : 343–346. |
| [5] | Monks NR, Liu S, Xu Y, et al. Potent cytotoxicity of the phosphatase inhibitor microcystin LR and microcystin analogues in OATP1B1- and OATP1B3-expressing HeLa cells[J]. Mol Cancer Ther, 2007, 6(2) : 587–598. DOI:10.1158/1535-7163.MCT-06-0500 |
| [6] | Arima Y, Nishigori C, Takeuchi T, et al. 4-Nitroquinoline 1-oxide forms 8-hydroxydeoxyguanosine in human fibroblasts through reactive oxygen species[J]. Toxicol Sci, 2006, 91(2) : 382–392. DOI:10.1093/toxsci/kfj161 |
| [7] | Gehringer MM. Microcystin-LR and okadaic acid-induced cellular effects:a dualistic response[J]. FEBS Lett, 2004, 557(3) : 1–8. |
 2008, Vol. 24
2008, Vol. 24
