产超广谱β-内酰胺酶( ESBLs )和头孢菌素酶(AmpC)细菌日益引起重视[1-5]。产生 ESBLs 和 AmpC 酶是大肠埃希菌(E.coli)和肺炎克雷伯菌(K.pneu)对头孢类抗生素耐药的主要机制,并且在各地区流行的基因型不尽相同[2-5]。为了解江苏省镇江地区分离的E.coli和K.pneu的耐药特性、ESBLs和AmpC酶基因型分布以及细菌间耐药性转移方式,进行了本研究。结果报告如下。
1 材料与方法 1.1 材料 1.1.1 菌株来源2005年1月~2006年6月,从本地区3家综合性医院住院和门诊患者标本中分离的产ESBLs和(或)AmpC酶的大肠埃希菌(E.coli)74株,肺炎克雷伯菌(K.pneu)35株。质控菌株:E.coli ATCC25922(浙江杭州天和微生物试剂有限公司);K.pneu ATCC700603,产TEM-5,CTX-M-3,OXA-4型ESBLs的E.coli以及产MIR-1型AmpC酶的K.pneu(南京军区南京总医院邵海枫教授惠赠)。
1.1.2 主要试剂17种抗生素药敏纸片、培养基(英国Oxoid公司);聚合酶链反应(PCR)试剂盒及100bpDNA分子量标准、琼脂糖等(日本TaKaRa公司);根据GeneBank公布的ESBLs基因序列设计9对PCR引物;扩增ampC基因的PCR引物参照文献[6],由宝生物工程(大连)有限公司合成。
1.1.3 仪器Hettich-UNIVERSAL16R型低温高速离心机(德国Hettich公司);Mastercycler Personal 5332型PCR扩增仪(德国Eppendorf公司);国产BS 423型电泳仪(北京生化仪器厂);国产MD-300型紫外多功能分析仪(镇江美达生物仪器有限公司)。
1.2 方法 1.2.1 药敏试验及耐药酶表型检测细菌药敏试验采用K-B法,操作及结果判断参考美国国家临床实验室标准(NCCLS)2004年标准;产ESBLs菌株表型确诊试验参照文献[7]方法进行;AmpC酶检测采用文献[8]方法。
1.2.2 PCR检测耐药基因ESBLs基因扩增体系:10×Buffer 2.5 μl、MgCl(1.5 mmol/L)1.5 μl、dNTP(0.2 mmol/L)2.0 μl、Taq聚合酶1.25 U、引物各10 pmo1、模板DNA(煮沸法制备)3 μl,添加灭菌去离子水至总体积25 μl;ESBLs基因扩增条件:预变性94℃ 5 min,变性94℃ 1 min,退火1 min(退火温度根据引物而定),延伸72℃ 2 min,35个循环,最后72℃延伸10 min;ampC基因检测参照文献[6],采用多重PCR法进行。PCR产物用15 g/L的琼脂糖凝胶电泳后,溴乙啶染色,在紫外线下观察产物片段。
1.2.3 接合试验以产生ESBLs和(或)AmpC酶的大肠埃希菌和肺炎克雷伯菌作为供体菌,E.coli-C600作为受体菌,进行转质粒试验。操作参照文献[9]进行。
1.2.4 重复一致序列(ERIC)-PCR选择肠道菌广泛存在的菌体DNA中的重复序列ERIC-2(5'AAG TAA GTG ACT GGG GTG AGC G3')作为引物。ERIC-PCR扩增体系:10×Buffer 2.5 μl、MgCl(2.5 mmol/L)2.5 μl、dNTP(0.2 mmol/L)2.0 μl、TaqPolymerase 2U、引物各25 pmol、模板DNA(煮沸法制备)3 μl,添加灭菌去离子水至25 μl;扩增条件:预变性94℃ 5 min,变性94℃ 1 min,退火35℃ 1 min,延伸72℃ 2 min,48个循环,最后72℃延伸10 min。产物用15 g/L的琼脂糖凝胶电泳后,溴乙啶染色,在紫外线下观察。
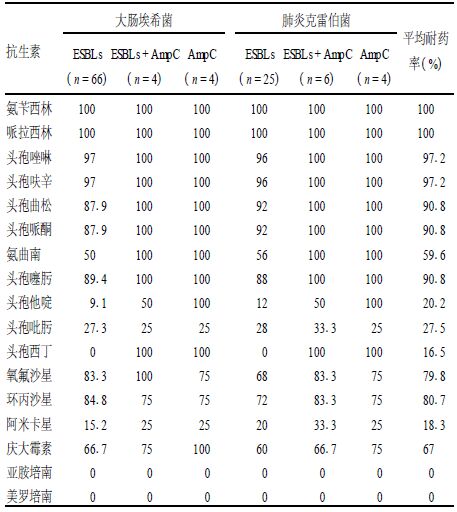
2 结果 2.1 产酶菌株对17种抗生素耐药率产酶菌株对亚胺培南、美罗培南、阿米卡星、头孢吡肟的敏感性较高,对其他13种抗生素的耐药性较强(表 1)。
| 表 1 产ESBLs和AmpC酶大肠埃希菌和肺炎克雷伯菌对17种抗生素耐药率(%) |
2.2 PCR
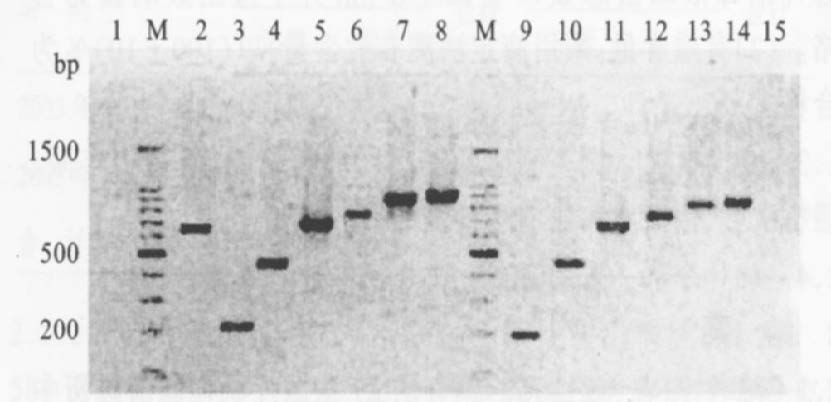
经PCR 扩增,发现ESBLs 以CTX-M 型检出率最高,占75.2 %(82/ 109) ,其次为TEM 型,占 35.8 %(39/ 109) ;AmpC 酶则以CIT 和DHA 型为主。
|
注:1,15:分别为蒸馏水和ATCC 25922对照;2~8:VEB-1、OXA-2G、OXA-1G、CTX-M-9G、CTX-M-1G、SHV、TEM型ESBLs阳性分离菌;9~14:OXA-2G、OXA-1G、CTX-M-9G、CTX-M-1G、SHV、TEM型ESBLs接合子;M:100bp分子量标准。 图 1 PCR扩增ESBLs 基因结果 |
|
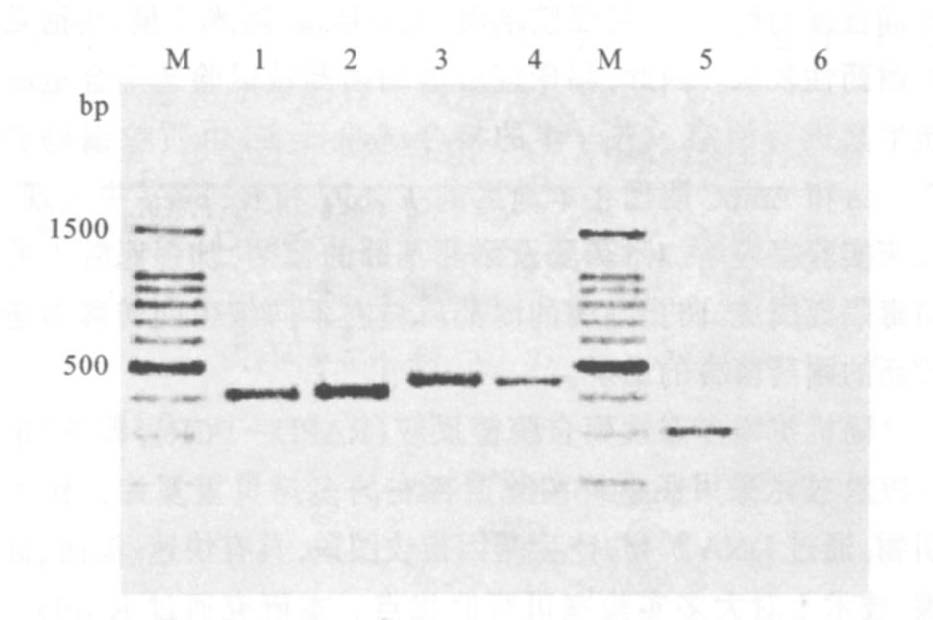
注:1 ,3 分别为DHA 型和CIT 型ampC 基因阳性分离菌;2 ,4 为DHA型和CIT 型ampC 基因接合子;5 :MIR - 1 型ampC 基因阳性对照菌; 6 :ATCC25922 对照;M:100bp 分子量标准。 图 2 PCR圹增ampC基因结果 |
2.3 接合试验
将产生ESBLs和(或)AmpC酶的74株大肠埃希菌和35株肺炎克雷伯菌分别与E.coli-C600进行接合试验,结果共有74株接合成功并能扩增出与供体菌相同的耐药基因片段,阳性率为67.9%。
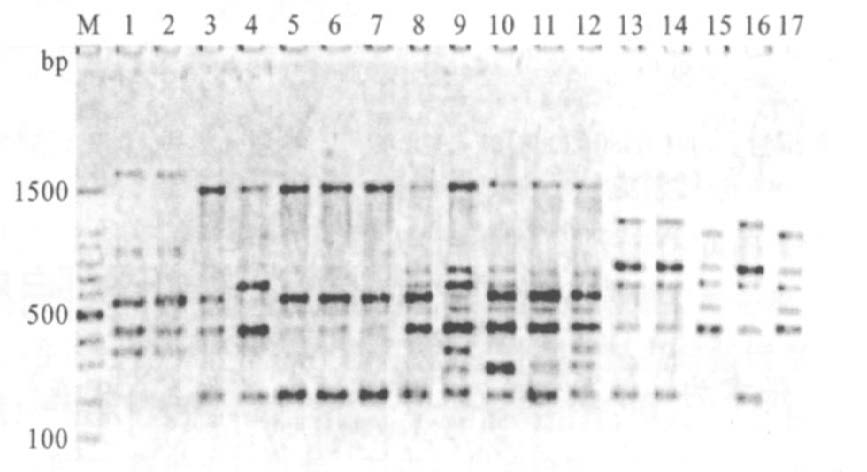
2.4 ERIC-PCR分型(图 3)74株E.coli和35株K.pneu均能扩增出清晰的DNA指纹图谱,扩增出的条带多在3~9条左右,大小多在200~1 500bp。
根据扩增片段数目、大小,将74株E.coli分成42型,其中11个型别分别含2株菌,6个型别分别含3株菌,3个型别分别含4株菌,22株菌各属1型。将35株K.pneu分成22型,其中6个型别分别含2株菌,2个型别分别含3株菌,1个型别含4株菌,13株菌各属1型。
|
注:M:100bp 分子量标准;1 与2 ,9 与12 ,10 与11 ,15 与17 带型相同;13 、14 、16 带型相同;3 ,5 ,6 ,7 带型相同;其他带型不同,提示有散 在克隆流行 图 3 ERIC- PCR分型结果 |
3 讨论
产ESBLs菌已在世界范围内广泛流行。国内以CTX-M和SHV为主要基因型,不同亚型的酶也呈区域性分布[4, 5, 10, 11]。本研究发现,本地区E.coli和K.pneu产生的ESBLs以CTX-M型最为常见,占75.2%;TEM型酶检出率为35.8%;SHV型酶则主要由K.pneu产生。所产AmpC酶则以CIT和DHA型为主。本次研究中,有14株产酶菌未能检出相关的耐药基因型,这些细菌可能产其他类型的β-内酰胺酶或存在其他耐药机制。有46.8%的菌株同时携带至少2种以上耐药基因。药敏试验结果显示,产酶菌株对头孢噻肟的耐药率高达90.8%,结合CTX-M型ESBLs的高检出率,分析其主要原因与临床头孢噻肟的高使用率有关。研究显示,产酶菌对β-内酰胺类、喹诺酮类和庆大霉素等存在不同程度的耐药,但对亚胺培南、美罗培南、阿米卡星、头孢吡肟耐药性较低。因此,临床应根据细菌药敏试验选用合适的抗生素进行治疗。进一步的接合试验证实,由质粒编码的ESBLs和AmpC酶已在本地区的E.coli和K.pneu中出现。临床实验室应增加耐药酶及耐药基因的检测,加强医院内的消毒隔离措施,防止细菌的耐药质粒在不同细菌间转移而造成新的耐药菌株的出现。
随机扩增多态性聚合酶链反应(RAPD-PCR),即ERIC-PCR技术采用肠道杆菌普遍存在的多拷贝重复片段作为引物,通过DNA扩增,产生基因指纹图谱,具有快速、简便、价廉、技术上对大多实验室可行的优点。本研究通过RAPD-PCR将74株E.coli分成42型,将35株K.pneu分成22型。结果表明,在本地区存在多克隆菌株的流行。
| [1] | 方平, 潘晓龙, 周东升, 等. 产超广谱β内酰胺酶和高产AmpC酶革兰阴性杆菌耐药性检测[J]. 中国感染与化疗杂志, 2005, 5(5) : 270–274. |
| [2] | 彭少华, 刘素玲, 程文娟, 等. 大肠埃希菌产质粒介导AmpC酶现状和基因型研究[J]. 中国感染与化疗杂志, 2006, 6(2) : 73–76. |
| [3] | 王锦娜, 邵海枫, 姚兵, 等. 大肠埃希菌中AmpC酶和质粒介导的ampC基因的发生和检测[J]. 临床检验杂志, 2006, 24(2) : 122–124. |
| [4] | Coque TM, Oliver A, Perez-Diaz JC, et al. Genes encoding TEM-4.SHV-2,and CTX-M-10 extended-spectrum β-lactamases are carried by multiple Klebsiella pneumoniae clones in a single hospital(Madrid,1989 to 2000)[J]. Antimicrob Agents Chemother, 1989, 46(2) : 500–510. |
| [5] | Chanawong A, M Zali FH, Heritage J, et al. Three cefotaximases,CTX-M-9,CTX-M-13,and CTX-M-14,among enterobacteriaceae in the People's Republic of China[J]. Antimicrob Agents Chemother, 2002, 46(3) : 630–637. DOI:10.1128/AAC.46.3.630-637.2002 |
| [6] | Pérez-Pérez F J, Hanson N D. Detection of plasmid mediated AmpC -Lactamase genes in clinical isolates by using multiplex PCR[J]. J Clin Microbiol, 2002, 40(6) : 2153–2162. DOI:10.1128/JCM.40.6.2153-2162.2002 |
| [7] | 韩善桥, 陆晓白, 李杰, 等. 肠杆菌科细菌产超广谱β-内酰胺酶检测及耐药性分析[J]. 中国抗生素杂志, 2003, 28(8) : 475–476. |
| [8] | 沈定霞, 白立彦, 罗燕萍, 等. 从大肠艾希菌和肺炎克雷伯菌中检测超广谱β-内酰胺酶和AmpC酶[J]. 军医进修学院学报, 2002, 23(1) : 18–20. |
| [9] | 邵海枫, 崔蕾蕾, 赵晓智, 等. 多重PCR技术检测肺炎克雷伯菌中质粒介导的AmpC酶基因[J]. 临床检验杂志, 2005, 23(6) : 414–417. |
| [10] | 陈升汶, 卢月梅, 张阮章, 等. 大肠埃希菌和肺炎克雷伯菌超广谱β内酰胺酶基因分型研究[J]. 中华检验医学杂志, 2006, 29(2) : 166–167. |
| [11] | 季淑娟, 陈亚岗, 俞云松, 等. 浙江省产超广谱β-内酰胺酶大肠埃希菌和肺炎克雷伯菌的基因分型[J]. 中华传染病杂志, 2006, 23(2) : 75–78. |
 2008, Vol. 24
2008, Vol. 24