DR5(Death receptor5,TRAIL-R1)是肿瘤坏死因子相关凋亡诱导配体(TNF-related apoptosis-inducing ligand,TRAIL)的受体成员之一[1],其抗人DR5单克隆抗体TRA-8[2]和AD5-10[3]均能诱导肿瘤细胞的凋亡,且对人正常肝细胞无细胞毒性作用。制备与DR5特异性结合的抗体有可能成为一种治疗癌症的有效途径。然而,制备单抗成本非常高。而多克隆抗体的制备相对简单且成本低。因此,本项目拟制备抗人DR5的多抗,进一步研究抗人DR5多抗杀灭肿瘤的效果。鉴于DR5是细胞表面受体,本实验采用其膜外段多肽作为抗原,克隆并在大肠埃希菌中表达了人DR5 cDNA的胞外区域重组多肽。为下一步制作多克隆抗体提供基础依据。
1 材料与方法 1.1 材料人肝癌细胞系HepG2(本校细胞工程实验李煜教授惠赠);大肠埃希菌BL21(DE3)(本校生物化学实验室侯鑫博士惠赠)。原核表达载体pGEX-4T-1和大肠埃希菌DH5a由本实验室保存。DMEM培养基(美国GIBCO公司);胎牛血清(FCS)(杭州四季青公司)。低分子量蛋白Marker(中国科学院上海生物化学研究所)。胰蛋白胨、酵母提取物(英国OXOID公司)。丙烯酰胺(美国Sigma公司);亚甲基双丙烯酰胺(美国Amresco公司)。RNAiso Reagent、RNA PCR Kit(AMV)、克隆载体pMD19-T、dNTPs及限制性内切酶(大连宝生物公司)。DNA凝胶回收试剂盒、Taq聚合酶、DNA Marker(北京Tiangen公司)。其他常规生物化学试剂为国产分析纯。大肠埃希菌的培养为常规液体或固体LB培养基。DNA、RNA条带观察及蛋白含量分析的核酸凝胶成像仪和UVIBand凝胶影像分析系统(英国UVITec公司)。
1.2 方法 1.2.1 细胞培养人肝癌细胞HepG2培养于DMEM培养基(10g/L DMEM粉末,0.044mol/L NaHCO3,0.01mol/L Hepes,0.07g/L青霉素,0.05g/L链霉素,10%FCS)中贴壁培养。37℃、5%CO2培养箱内培养24h后传代1次,再培养细胞至指数生长期。
1.2.2 引物的设计与合成根据GenBank上编号为AF016849的序列,用Oligo6软件设计DR5 cDNA胞外区域的1对引物。上游引物:5'-GGATCCGCTCTGATCACCCAACAAGAG-3';下游引物:5'-GAATTCTTAGAGAGAACAGGGAGAGGCAC-3'。2个引物5'端分别加入了BamH I和EcoR I酶切位点。预计扩增片段长度489bp。引物由日本TaKaRa公司合成。
1.2.3 RT-PCR检测肝癌细胞HepG2培养至指数生长期时,提取HepG2细胞的总RNA,取5μl总RNA进行琼脂糖凝胶电泳检测,再用紫外分光光度计测其浓度。然后用提取总RNA为模板进行反转录反应。反转录体系为10μl:模板RNA(248ng/μl)1μl,AMV Reverse Transcriptase 0.5μl,Oligo d T-Adaptor primer 0.5μl,10×RT Buffer 1μl,MgCl2 2μl,dNTPs Mixture 1μl,RNase Inhibitor 0.25μl,RNase Free H2O3.75μl。反转录反应条件为42℃ 30min,99℃ 5min,5℃5min。PCR反应体系为50μl:cDNA10μl,5×PCR Buffer 10μl,TaKaRa Ex Taq HS 0.25μl,上、下游引物各20pmol/μl,灭菌蒸馏水28.75μl。PCR反应最佳条件为94℃预变性2min,94℃变性30 s,65℃复性30 s,72℃延伸1min,35个循环,再用72℃延伸10min。反应结束后取6μl反应产物,琼脂糖凝胶电泳检测。
1.2.4 重组克隆载体的构建及测序将DR5 cDNA胞外区域PCR产物与pMD19-T克隆载体连接,连接体系为10μl:PCR产物2μl,pMD19-T载体1μl,ligation mix 5μl,ddH2O 2μl。14℃连接过夜之后,转化DH5a感受态菌。涂板14h后,选取若干个菌落,摇菌提取质粒,经质粒PCR初步筛选阳性克隆后,再用限制性内切酶EcoR I单酶切、BamH I和EcoR I双酶切鉴定。选定的阳性克隆命名为pMD-eDR5,将菌液送到TaKaRa公司测序。
1.2.5 DR5胞外区域原核融合表达载体的构建使用BamH I和EcoR I双酶切重组克隆载体pMD-eDR5,琼脂糖凝胶电泳后用AxyPrep DNA凝胶回收试剂盒回收eDR5目的片段;同样,用BamH I和EcoR I双酶切pGEX-4T-1,回收线形载体。用T4DNA连接酶(T4DNA连接酶0.5μl,T4 ligation buffer 1μl,pGEX-4T-1回收片段1μl,eDR5回收片段4μl)14℃连接过夜。将连接产物转化DH5a感受态菌,涂平板37℃培养过夜,挑取单菌落,摇菌提质粒,进行酶切鉴定,命名为pGEX-eDR5,然后测序。
1.2.6 原核融合表达载体在大肠埃希菌中的表达将重组表达载体pGEX-eDR5转入E.coli BL21(DE3)感受态菌中,涂板培养于含有Amp(100μg/ml)、葡萄糖(终浓度为0.2%)的LB固体培养基上,37℃培养10h后挑取单菌落接种入含Amp(120μg/ml)、葡萄糖(终浓度为0.2%)的LB液体培养基中,摇菌至A600=0.5后加入异丙基-β-D-硫代乳糖苷(IPTG)诱导表达。设计IPTG浓度梯度(50,100,150,200,250,300μg/ml),培养温度梯度(25,28,31,34,37℃),诱导时间梯度(1,2,3,4,5h)以选择最佳表达条件。最后收集菌液,通过可见光比色测定各组诱导样品的菌液浓度,计算各组样品在SDS-PAGE电泳时的上样量,以保证各泳道中的菌体量一致。超声波破碎、煮菌后离心收集上清液。
1.2.7 SDS-PAGE电泳鉴定配制5%的浓缩胶和10%的分离胶。分别用空BL21(DE3)菌、pGEX-4T-1转化的BL21(DE3)菌及低分子量蛋白Marker作为对照,与IPTG诱导的携带pGEX-eDR5的BL21(DE3)电泳,电流为10mA。考马斯亮蓝染色后脱色,待看清条带后分析其在不同IPTG浓度、温度、时间的表达情况。用UVI Band软件分析蛋白含量并确定目的蛋白的分子量。
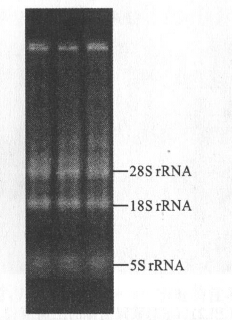
2 结果 2.1 肝癌细胞HepG2总RNA的提取(图 1) 从肝癌细胞中提取总RNA作为RT-PCR模板,提取的总RNA进行琼脂糖凝胶电泳检测。总RNA有点降解,但仍能看清rRNA 3个条带。用紫外分光光度计所测的A260、A280和A320分别为0.0344,0.0192和0.0034。A260/A280比值为1.9616,说明提取的RNA中蛋白含量和核酸降解程度较低。经RNA浓度换算,得到的RNA浓度为248ng/μl。
|
图 1 HepG2 总 RNA |
2.2 RT-PCR产物琼脂糖凝胶电泳鉴定
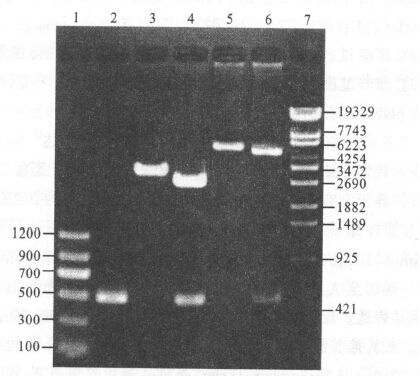
(图 2) 人DR5 cDNA胞外区域RT-PCR产物进行琼脂糖凝胶电泳,结果在约500bp处有一条明亮的带,与预期结果一致。
|
注:1:DNA标准分子量II;2:RT-PCR产物(489bp);3:pMD-eDR5的EcoR I单酶切,酶切产物片段大小为3179 bp;4:pMD-eDR5的EcoR I和BamH I双酶切,酶切产物片段大小各为2.69 Kb和489 bp;5:pGEX-eDR5的EcoR I单酶切,酶切产物片段大小为5469 bp;6:pGEX-eDR5的EcoR I和BamH I双酶切,酶切产物片段大小为4.89 Kb和489 bp;7:DNA分子量标准λEcoT14。 图 2 eDR5 RT-PCR产物和重组载体的限制性酶切结果 |
2.3 重组克隆载体和重组表达载体的酶切鉴定及测序结果构建好的pMD-eDR5和pGEX-eDR5重组载体用EcoR
I单酶切、BamH I和EcoR I双酶切后的电泳结果见图 2的3~6泳道,双酶切均切下与RT-PCR产物相同大小的片断,与预期结果相符。
经测序,pMD-eDR5质粒和pGEX-eDR5质粒中插入的人DR5胞外区cDNA片段序列一致。测出的目的片段长度为489bp,与GenBank编号为AF016849的原序列对比,发现有个同义突变位点。在原序列中对应的碱基是G,是编码脯氨酸密码子CCG的第3个碱基,克隆后该密码成为CCC,但仍编码脯氨酸,因此,此突变不影响DR5 cDNA胞外区域的蛋白质性质。
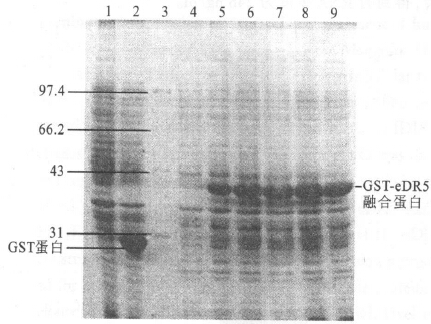
2.4 eDR5在大肠埃希菌中的表达(图 3) 经IPTG诱导,融合表达裁体pGEX-eDR5在E.coli BL21(DE3)中有较高的表达。经对温度、时间、IPTG浓度梯度调整后,发现IPTG浓度在50~300μg/ml范围内对GST-eDR5融合蛋白的表达无明显影响;不同温度诱导对融合蛋白表达量也无明显影响(未显示电泳图)。A600=0.5时加入终浓度100μg/ml的IPTG,37℃诱导融合表达载体pGEX-eDR5数小时结果显示,诱导4h时可溶性融合蛋白含量最高(泳道8),诱导到5h蛋白量不再增加(泳道9)。经UVI Band软件分析融合表达蛋白占细菌总蛋白的19%。
|
注:1:大肠埃希菌BL21(DE3)破碎菌体的上清液;2:转化pGEX-4T-1的BL21(DE3)破碎菌体的上清液;3:低分子量标准蛋白质(97.4,66.2,43,31,20.1,14.4kD);4~9:转化pGEX-eDR5的BL21(DE3)经IPTG诱导0,1,2,3,4和5h后的破碎菌体上清液。 图 3 重组表达载体pGEX-eDR5在E.coli BL21(DE3)中的表达 |
3 讨论
人DR5是由411个氨基酸组成的I型跨膜蛋白[4]。DR5胞外区域与其配体TRAIL结合后引发细胞内凋亡信号的传导,最终导致细胞凋亡[5, 6]。因此,只需DR5胞外区域蛋白作为抗原来免疫动物,就可获得DR5多克隆抗体。本实验应用RT-PCR技术,从肝癌细胞总RNA中成功地克隆出DR5 cDNA胞外区域,经测序结果与GenBank上的序列基本一致。制备高效价的多克隆抗体需要高纯度的抗原蛋白。原核表达操作简便、目的蛋白表达量高,可以很快得到可纯化的抗原蛋白,因此,又进行克隆基因片段的原核表达研究。考虑到真核基因在原核表达系统中的表达可能因密码偏爱而受影响,本研究选用了广泛应用于表达重组蛋白的带有GST标签的pGEX-4T-1载体,将DR5胞外区域基因置于可溶性的GST下游,在大肠埃希菌中得到了有较高表达量的可溶性GST-eDR5融合蛋白。为摸索GST-eDR5融合蛋白最佳诱导表达条件,进行IPTG浓度、温度、时间梯度调整。结果表明,IPTG浓度对GST-eDR5融合蛋白的表达无明显影响;在诱导时间相同的情况下,不同温度时的可溶性GST-eDR5融合蛋白的表达量也无明显差别;当IPTG浓度100μg/ml,37℃诱导4h时融合蛋白表达量最高,占细菌总蛋白的19%。
本实验获得的GST-eDR5的原核表达系统为下一步DR5多肽纯化、制备DR5多克隆抗体和进一步研究DR5多抗预防和杀灭肿瘤的效果提供了基础依据。
| [1] | Preet MC, Michael E, Alan J, et al. Death receptor 5, a new member of the TNFR family, and DR4 induce fadd-dependent apoptosis and activate the NF-kB pathway[J]. Immunity, 1997, 7 : 821–830. DOI:10.1016/S1074-7613(00)80400-8 |
| [2] | Kimihisa I, Weimin L, Limin Z, et al. Tumoricidal activity of a novel anti-human DR5 monoclonal antibody without hepatocyte cytotoxicity[J]. Nature Medicine, 2001, 7(8) : 954–960. DOI:10.1038/91000 |
| [3] | Yabin G, Caifeng C, Yong Z, et al. A novel anti-human DR5 monoclonal antibody with tumoricidal activity induces caspase-dependent and caspase-independent cell death[J]. J Biol Chem, 2005, 280(51) : 41940–41952. DOI:10.1074/jbc.M503621200 |
| [4] | Henning W, Mariapia ADE, Richard SJ, et al. TRAIL-R2:a novel apoptosis-mediating receptor for TRAIL[J]. The Embo Journal, 1997, 16(17) : 5386–5397. DOI:10.1093/emboj/16.17.5386 |
| [5] | LeBlanc HN, Ashkenazi A. Apo2L/TRAIL and its death and decoy receptors[J]. Cell Death Differ, 2003, 10 : 66–75. DOI:10.1038/sj.cdd.4401187 |
| [6] | Fiona CK, Gavin RS. Following a TRAIL:update on a ligand and its five receptors[J]. Cell Research, 2004, 14(5) : 359–372. DOI:10.1038/sj.cr.7290236 |
 2008, Vol. 24
2008, Vol. 24
