2. 长治医学院
O6-甲基鸟嘌呤DNA甲基转移敏(O6-methylguanine-DNA-methyltransferase,MGMT)定位于人类染色体10q26,是一种高效的DNA直接修复酶,能特异修复DNA序列中的O6-烷基鸟嘌呤(O6-methylguanine,O6-mG)损伤,维持基因组的精确性和完整性,从而防止烷基化合物诱导的致癌作用,是人类细胞中迄今发现的唯一修复该损伤的甲基转移酶[1]。为研究其基因多态性与食管癌的关系以及与环境因素在食管癌发生中的交互作用,本研究采用1∶1配对病例对照研究方法,选择我国食管癌高发区之一的长治地区作为研究现场,对该地区食管癌发生的相关因素进行调查,并应用聚合酶链反应-限制性片段长度多态性(PCR-RFLP)技术对该地区食管癌患者及正常对照的MGMT多态性基因型进行检测,为探讨食管癌高发原因提供依据。
1 对象与方法 1.1 对象采用1∶1病例对照研究方法。研究对象选自2001年8月~2005年7月间长治地区2所医院(均为“三甲”医院)就诊者。病例选择:经内窥镜和临床病理确诊为食管癌的病人(排除经放疗和化疗者)201例。对照选择:与病例配对来自同的医院其他科室的无消化道疾病、无肿瘤病史及肿瘤临床症状患者201例。配对条件:同年龄(相差不超过5岁),同性别,同居住地区,同时间就诊(相差不超过1个月),在长治地区生活15年以上的汉族常住居民。
1.2 方法 1.2.1 问卷调查调查内容主要包括一般人口学特征、饮食习惯、生活行为方式(如吸烟、饮酒)、精神创伤史、食管癌家族史等,各变量均给予明确的定义,以减少选择偏移和信息偏移,吸烟定义为过去或目前吸烟1支/d以上,持续1年以上;经常食用腌制食品指过去或目前每周食用至少3次,持续5年以上。调查员与患者进行面对面调查填写。
1.2.2 MGMT基因型检测[2](1) DNA制备:抽取各研究对象肘静脉血2 ml,加酸性枸酸盐葡萄糖溶液(ACD)抗凝剂抗凝后,-20 ℃冰箱保存备用;用白细胞快速提取法提取DNA。(2)引物设计:上游:5'-CCAGAGGTTTACTAAGCCCC-3'下游:5'-TTACCGACCTTGC TGGAAAAC-3',引物由上海生工合成。PCR反应体积及反应条件:25 μl反应体系中包含100 ng基因组DNA,0.4 μmol/L引物,200 μmol/L dNTP,1.5 mmol/L MgCl2,10×反应缓冲液2.5 μl,0.5 U Taq酶。循环参数为:94 ℃预变性5 min,37个循环:94 ℃变性30 s,56 ℃退火30 s,72 ℃终延伸7 min。(3)MGMT酶切分型:20 μl酶切反应体系包括PCR产物10 μl,5个单位的限制性内切酶Ear Ⅰ,相应的Buffer Y+/TANGOTM酶切反应缓冲液1.2 μl,混匀后于37 ℃下水浴孵育过夜。酶切产物在3%琼脂糖凝胶电泳,电压80 V,60 min,溴化乙锭染色。
1.3 统计分析遗传平衡性检验Hardy-Weinberg,基因型频率用x2检验,应用Logistic多因素回归分析估计危险度OR及其95%CI。采用SPSS 12.0软件进行统计分析,统计检验水平取双侧α=0.05。
2 结果 2.1 一般情况共调查食管癌患者201例,对照201例。病例组与对照组男性均为130例,占64.68%;女性71例,占36.32%。性别比为1.83∶1。病例组最小年龄38岁,最大年龄82岁,平均年龄(58.75±8.61)岁;对照组最小年龄37岁,最大年龄80岁,平均(58.81±8.58)岁
2.2 食管癌可疑危险因素Logistic回归多因素分析(表 1)最终进入Logistic回归模型的变量有7个,其中摄入较多肉蛋类食品为食管癌的保护因素,吸烟、喜热食、喜硬食、经常吃腌制食品、情绪因素、食管癌家族史为食管癌的危险因素。
| 表 1 食管癌危险因素条件Logicstic回归分析 |
2.3 遗传平衡性检验(Hardy-Weinberg检验)(表 2)
MGMT各基因型的对照组分布符合Hardy-Weinberg遗传平衡检验,x2=1.25,P>0.05,表明研究对象的选择无遗传学偏差。
| 表 2 MGMT基因型频率在对照组实验值与理论值的分布 |
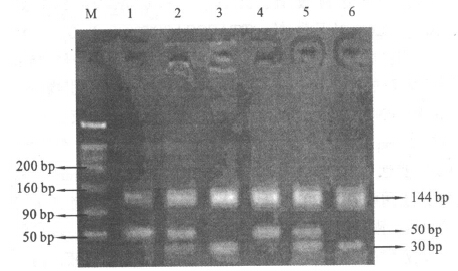
2.4 MGMT基因的电泳结果(图 1)
MGMT基因PCR特异扩增的片段长度为194 bp,当为突变型时,可产生144和50 bp 2个新的片段;当为野生型时,可产生144,20和30 bp 3个新的片段;当为杂合型时,可产生144,50,30和20 bp的4个片断,其中20bp片段无法清楚显示。
|
图 1 MGMT多态位点Ear Ⅰ酶切电泳图 |
2.5 MGMT基因型多态性分布比较(表 3)
病例组和对照组MGMT各基因型分布差异有统计学意义(x2=9.80,P<0.01);携带MGMT基因杂合型和突变基因型个体发生食管癌的危险性高于携带野生基因型个体,OR值分别为1.33(95%CI=1.01~2.07)和1.47(95%CI=1.03~2.54)。
| 表 3 MGMT基因型频率分布及食管癌危险性关系 |
2.6 MGMT基因多态性与腌制食品的交互作用(表 4)
| 表 4 MGMT基因与食用腌制食品的交互作用分析 |
食用腌制食品且携带有MGMT突变基因型者与不食用腌制食品且不携带突变基因者比较更易患食管癌(OR=2.38,95%CI=1.49~3.79),且大于食用腌制食品和MGMT对食管癌的单独作用,说明食用腌制食品与MGMT基因间存在交互作用。交互作用指数S=1.77>1,表明同时携带MGMT突变基因型并食用腌制食品者之间存在正交互作用,说明两因素同时存在所致食管癌发病率是两因素单独存在时所致食管癌发病率之和的1.77倍。交互作用归因比API=[OR11-(OR10+OR01)+1]/OR11=0.25,表明MGMT突变基因型与食用腌制食品同时存在时,食管癌发病率中有25%是由于两因素的交互作用所致。未发现MGMT基因多态性与吸烟、饮酒、精神刺激、食管癌家族史等之间存在交互作用。
3 讨论本研究结果表明,MGMT各基因型分布在病例组和对照组分布差异有统计学意义(x2=9.80,P<0.01);携带MGMT杂合基因和突变基因型个体发生食管癌的然险性比携带野生基因型个体分别高1.33倍(95%CI=1.01~2.07)和1.47倍(95%CI=1.03~2.54)。对于MGMT第3外显子基因多态性对肿瘤发生及人群易感性的影响机制局未明确。有文献报道[3-5]:MGMT第三外显子存在第84位密码子多态性改变(Leu被Phe取代),此位点的多态性改变在肺癌、宫颈癌、胃癌、肝癌、大肠癌等肿瘤患者和正常对照组中的检出率性差异均无统计学意义。
吸烟、饮酒是西方食管癌发生的重要危险因素,刘伯奇等的研究也认为吸烟是食管癌重要的致病因素[6]。本研究显示,吸烟、喜热食、喜硬食、经常吃腌制食品、情绪因素、食管癌家族史为食管癌危险因素。同时发现,食用腌制食品且携带有MGMT突变基因型者比不食用腌制食品且不携带突变基因型者更易患食管癌(OR=2.38,95%CI=1.49~3.79);且交互作用指数S=1.77>1,交互作用归因比API=0.25,表明携带MGMT突变基因型与食用制食品之间存在协同作用,即MGMT易感基因型-食用腌制食品同时存在时的危险度比两者单独存在时的危险度要高。王国荣等的研究也表明,腌制食品可增加消化道肿瘤发生的危险性[7]。本文发现,吸烟和MGMT突变基因型对食管癌发生的联合作用(OR=1.08)与它们各自的单独作用差别不大。
本研究认为,MGMT基因多态性与长治地区人群食管癌的易感性有关,同时与腌制食品间存在协同作用。因此,大力普及卫生知识,倡导健康的生活方式,改变不良的生活习惯并定期进行体检对预防食管癌及早期治疗有重要的作用。
| [1] | 齐健. MGMT基因的多态性与肿瘤的关联[J]. 医学新知杂志, 2003, 13(4) : 234–263. |
| [2] | 韩彦波, 冯向先, 李佩珍, 等. CYP1A1?SULT1A1基因多态性与食管癌遗传易感性[J]. 中国公共卫生, 2005, 21(1) : 3–6. |
| [3] | Inoue R, Abe M, Nakabeppu Y, et al. Characterization of human polymorphic DNA repair methyltransferase[J]. Pharmacogenetics, 2000, 10(1) : 59–66. DOI:10.1097/00008571-200002000-00008 |
| [4] | 路滟, 徐耀初, 沈靖, 等. O6-甲基鸟嘌呤-DNA甲基转移酶基因多态性与胃癌遗传易感性的关系[J]. 疾病控制杂志, 2006, 10(3) : 222–225. |
| [5] | 刘汝青, 庄志雄, 何春华, 等. O6甲基鸟嘌呤DNA甲基转移酶基因多态性与肿瘤易感性的关系[J]. 癌变·畸变·突变, 2002, 14(2) : 101–106. |
| [6] | 刘伯齐, 姜晶梅, 陈铮鸣, 等. 中国103个地区吸烟与食管癌风险研究:死因调查中的病例对照方法学研究[J]. 中华医学杂志, 2006, 86(6) : 380–385. |
| [7] | 王国荣. 食盐?腌制食品摄入与胃癌的关系[J]. 中华腹部疾病杂志, 2005, 5(11) : 封3. |
 2008, Vol. 24
2008, Vol. 24





