2. 哈尔滨医科大学公共卫生学院营养与食品卫生教研室
植酸(phytic acid,IP6,肌醇六磷酸)主要存在于豆类和谷类植物体中,具有天然生物活性成分物质,是一种抗营养因子[1]。有资料表明[2],植酸具有预防和治疗多种肿瘤的药用活性,且天然低毒,已成为抗肿瘤新药研究与开发的热点。本研究以人胃癌(SGC)7901细胞株为离体实验模型,探讨植酸对抑制性卡巴蛋白(IkB-)表达影响及胃癌细胞增殖的抑制作用机制。
1 材料与方法 1.1 材料 1.1.1 人胃癌细胞株SGC-7901细胞(北京市肿瘤研究所)。细胞培养于含10%国产优级胎牛血清、1%谷氨酰胺、1%双抗的RPMI1640培养液中,置于37℃、5%CO2孵育箱中,用0.02%的乙二胺四乙酸二钠盐(EDTA)进行传代培养。
1.1.2 试剂RPMI1640培养基(美国Gibco公司);植酸(50%水溶液)(美国Sigma公司),用无菌去离子水配成储存液(100×),临用时用2%培养液稀释成终浓度为0,2.0,2.5利3.0mmol/L作用于细胞;鼠抗人P65单克隆抗体与兔抗人β-actin、抑制性卡巴蛋白(IkB-)多克隆抗体(美国Santa Cruz生物技术公司,北京中杉生物技术公司);碱性磷酸酶标记抗兔与抗鼠IgG(美国Pregema公司)。
1.2 方法 1.2.1 四甲基偶氮噻唑蓝(MTT)实验常规培养SGC-7901细胞,选择指数生长期细胞,用乙二胺四乙酸二钠盐(EDTA)消化,调整细胞数为2.5×104/ml,接种于96孔培养板,每孔200l,实验组分别给予终浓度为1.5,2.0,2.5,3.0,3.5mmol/L的植酸,对照组加入等量的新鲜培养液,每个剂量组设5个平行孔。分别培养24,48和72h后加入浓度为5g/L的MTT液20l,继续培养4h,吸弃上清,加入150l二甲基亚砜(DMSO)在平板摇床微振荡10min,于酶标仪上490nm波长处测定各孔的吸光度(A)值,计算植酸对SGC-7901细胞的生长抑制率。
1.2.2 倒置显微镜下形态学观察将终浓度为3.0mmol/L植酸的2%胎牛血清的RPMI-1640完全培养液,及不含植酸的2%胎牛血清的RPMI-1640完全培养液作为空白对照液,培养24h后,倒置显微镜观察细胞形态变化。
1.2.3 单细胞凝胶电泳实验用100l磷酸盐缓冲液(PBS)配制0.8%正常溶点凝胶,沸水溶解,载玻片上于4℃固化5min。浓度分别为0,2.0,2.5和3.0mmol/L的植酸作用SGC-7901细胞48h后的细胞悬液,取10l在37℃与90l低溶点胶混合加到第一层胶上,4℃固化10min后,浸没于裂解液中,4℃解1h。蒸馏水洗后,水平移入电泳槽,避光静止解旋20min。25V电压电泳20min。用2.4mol/L三羟基氨基甲烷(Tris,pH 7.5)漂洗3次后滴加5g/ml溴化乙锭(EB)30l,24h内阅片,观察不同浓度植酸对DNA的损伤影响。
1.2.4 蛋白印迹(Westernblot)检测常规收集同一时间点不同浓度的细胞,加细胞裂解液,提取蛋白质并测其浓度(Bradford法)。蛋白提取液变性,进行聚丙烯酰氨凝胶电泳(SDS-PAGE)电泳分离蛋白质。再将其转移到硝酸纤维素膜(NC膜)上,0.1%牛血清白蛋白(BSA)封闭1h后,用相应的一抗(2h)、二抗(1h)在杂交箱内反应。用碱性磷酸酶显色后在凝胶数字成像仪上拍照。
1.3 统计分析采用SPSS 13.0软件进行分析。
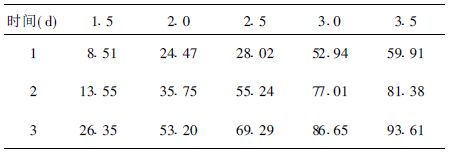
2 结果 2.1 MTT测定结果(表 1)用不同浓度的植酸作用于SGC-7901细胞,根据MTF法用酶标仪住490mm波长下检测细胞的吸光度(A),连续检测3d,用各剂量组的平均吸光度(A)值表示细胞的增殖情况,植酸作用下计算出细胞的生长抑制率。植酸对SGC-7901细胞有生长抑制作用,在每个时间点,随着植酸浓度的增加,细胞增殖速度均减缓,植酸对细胞增殖的抑制率均增加,其对细胞生长的抑制作用呈现剂量-效应关系;对于每个剂量组,随着时间的延长,植酸对细胞的增殖抑制率也逐渐增加,呈现时间-效应关系,当植酸浓度达到3.5mmol/L时,细胞基本停止生长。
| 表 1 不同浓度植酸、不同时间对胃癌SGC-7901细胞的生长抑制率( mmol/ L,%) |
2.2 植酸对SGC-7901细胞形态学的影响(图 1)
分别用浓度为0和3.0mmol/L的植酸处理细胞24h,在倒置显微镜下观察细胞基本生长状态的改变及形态的变化。

|
图 1 植酸(IP6)作用SGC-7901细胞24h的细胞形态 |
2.3 单细胞凝胶电泳实验检测植酸对DNA损伤的影响
荧光显微镜下可见,对照组细胞DNA呈圆形,边界清晰;植酸作用组细胞DNA呈现由圆形、致密红色核心(彗头)和朝向阳极的尾端DNA碎片(彗尾)构成的彗星形状。植酸(IP6)作用SGC-7901细胞48h,浓度分别为0,2.0,2.5和3.0mmol/L,DNA损伤率分别为5.9%,11.0%,34.6%和63.1%。随着植酸作用浓度的增加,细胞的彗星拖尾率也逐渐增大,呈现剂量-反应关系(P<0.05)。
2.4 蛋白印迹检测IkB-、NF-kBP65蛋白表达结果(图 2,3)植酸(IP6)作用胃癌细胞36h,IkB-蛋白表达随着IP6剂量的增加而呈递增趋势(数字成像仪上密度扫描值分别为0.790,0.805,0.885,0.930)。植酸(IP6)作用胃癌细胞72h,NF-kBP65蛋白表达随着IP6剂量的增加而呈递减趋势(数字成像仪上密度扫描值分别为0.521,0.493,0.450,0.256)。

|
图 2 植酸(IP6)作用SGC-7901细胞36h的IkB-蛋白表达 |

|
图 3 植酸(IP6)作用SGC-7901细胞72h的P65蛋白表达 |
3 讨论
MTT法测定结果表明,植酸对人胃癌SGC-7901细胞增殖具有抑制作用,呈剂量依赖性和时间依赖性。通过形态学和生化研究方法观察到细胞凋亡所具有的典型特征改变,证明植酸能够引起人胃癌SGC-7901细胞DNA损伤,诱导细胞凋亡的发生。
IkB-是IkB家族中的重要一员,细胞在静息状态下,存在于胞浆中,含有1个30~33氦基酸重要序列(锚蛋白重复区,ARM)[3-5],与细胞核因子(NF-kB)[4, 5]的Rel同源区(RHD)发生作用,覆盖NF-kB亚基P65的核定位序列(NLS),与NF-kB的二聚体组成三聚体,并使之滞留于胞质中,从而阻止NF-kB进入胞核与目标基因启动区域的特定序列结合,而处于无活性状态。当细胞受到外源性刺激时,IkB迅速裂解,NF-kB被激活并从三聚体中释放出来,借助于暴露出来的核定位信号进入细胞核,可调控与炎症、细胞增殖及凋亡等效应相关基因的转录,促进蛋白合成[6, 7]。本研究结果显示,植酸作用组IkB-蛋白的表达比正常对照组高,NF-kBP65蛋白的表达均比正常对照组低,呈剂量-反应关系。结果提示,植酸可能通过诱导IkB-的表达而抑制NF-kB信号传导通路的传导进而抑制下游基因的表达,从而促进细胞的凋亡。
综上所述,植酸在诱导SGC-7901细胞凋亡过程中,NF-kB的抑制因子IkB-活性增强,进而抑制核转录因子NF-kB的表达,可能会抑制下游凋亡抑制基因的表达,启动细胞的凋亡。细胞凋亡是一个程序化的复杂生理过程,它的启动和发展需要多种基因及其产物的参与。植酸是否通过其他信号传导通路启动细胞的凋亡尚需进一步研究。
| [1] | 李丹, 崔洪斌. 植酸对人胃癌细胞增殖抑制作用的体内实验[J]. 营养学报, 2006, 28(1) : 51–53. |
| [2] | T ant ivejkul K, Vucenik I, Eiseman J, et al. Inosit ol hexaphosphat e(IP6)enhances th e ant i-prolif erat ive ef fects of adriamycin and ta?? moxif en in breast cancer[J]. Breast Cancer Res Treat, 2003, 79(3) : 301–312. DOI:10.1023/A:1024078415339 |
| [3] | Huguet C, Crepieux P, Laudet VR. NF-]B transcript ion factors and I KB inhibt ors: evolut ion from a unique common ancestor[J]. Oncogene, 1997, 15(24) : 2965–2974. DOI:10.1038/sj.onc.1201471 |
| [4] | Whit eside ST, Israel AI. ]B prot eins: st ructure, funct ionand regula?? tion[J]. Cancer Biol, 1997, 8(2) : 75–82. DOI:10.1006/scbi.1997.0058 |
| [5] | May MJ, Ghosh SRel. NF-KB and IKB prot eins: an overiew[J]. Cancer Biol, 1997, 8(2) : 63–73. DOI:10.1006/scbi.1997.0057 |
| [6] | S hishodia s, Koul D, Aggarwal BB. Cyclooxygenase(COX)-2 in?? hibitor celecoxib abrogat es TNF-in duced NF-]B act ivation through inhibit ion of activat ion Of IkB-?? kinase and AKt in hu?? man non-small cell lung carcinoma: correlat ion w ith suppression of COX-2 synthesis[J]. J lmm unol, 2004, 173 : 2011–2022. |
| [7] | Lin A, KarinM. NF-]B in cancer: a marked t arget[J]. Cancer Bi?? ol, 2003, 13(2) : 107–114. |
 2008, Vol. 24
2008, Vol. 24