2. 沈阳军区药品检验所;
3. 沈阳军区总医院
鸡半胱氨酸蛋白酶抑制剂(chicken cystatin,cC)是由116个氨基酸组成的非糖基化蛋白质,含有2个二硫键,分子量约为14kD,是一种分泌性蛋白[1]。cC与人半胱氨酸蛋白酶抑制剂C(cystatin C)在结构上有许多相似性[2]。已经证实,用cC研究人cystatin C引起的淀粉样血管病的发病机制具有极大的可行性、经济性和便利性[3]。制备cC的传统工艺是从鸡蛋清中来提取的,但是鸡蛋清中cC的含量仅为0.01%,而且加工过程复杂,因此,用基因工程方法制备cC具有重要意义。研究表明,由于cystatin含有二硫键,大肠埃希菌表达体系在产量和纯化方面限制了它的应用性[4, 5]。为了克服上述缺陷,本实验室计划利用独特的PCR引物将cC的cDNA克隆至载体pPICZαA并转化到毕赤酶母X-33菌株中,实现具有天然氮末端的重组cC的可溶性分泌表达。结果报告如下。
1 材料与方法 1.1 材料限制性内切酶、T4 DNA连接酶、Pyrobest DNA聚合酶(上海生工生物工程公司);RNA提取试剂盒、RT-PCR试剂盒(大连宝生物公司);引物合成、DNA测序分析(大连宝生物公司合成);酵母菌株、质粒pPICZαA、pGEM-T载体(美国Invitrogen公司);菌种(北京鼎国生物公司);木瓜蛋白酶(USPP6000Pmg)(国药集团化学试剂有限公司);酪蛋白(北京奥博星生物技术责任有限公司)。
1.2 方法 1.2.1 RNA提取、RT-PCR和克隆鉴定利用RNA提取试剂盒从鸡输卵管中分离出总RNA,再利用RT-PCR试剂盒进行两步RT-PCR以获得编码cC的DNA片断。上游引物为5′-CTCGAGAAAAGAAGCGAGGACCGCTCCC GGCTCCTG-3′(下划线部分为XhoI酶切位点,阴影部分为载体pPICZαA中α-factor的部分序列),下游引物为5′-TCTAGATTACTGGCACTTGCTTTCCAGCAGTTT-3′(下划线部分为XbaI酶切位点)。含有XhoI和XbaI的cC cDNA先被克隆到pGEM-T载体中,然后转化E.coli XL-1 Blue感受态细胞。通过蓝/白筛选和酶切分析确定阳性克隆。挑取鉴定的阳性克隆进行目的基因测序。
1.2.2 pPICZαA-cC重组表达载体的构建和转化pPICZαA-cC重组表达载体操作参照文献[3]。构建后的载体用限制酶SacⅠ将经过筛选确定得到的阳性重组质粒pPICZαA-cC线性化后,电击法转化毕赤酵母X-33菌株,将转化处理后的菌液涂布于含100 μg/ml Zeocin的酵母膏胨葡萄糖琼脂培养基(YPD)平板上,30℃培养2~3 d,从中筛选得到8个抗Zeocin的转化子,提取转化子基因组DNA,进行PCR鉴定。
1.2.3 重组cC的诱导表达及回收将重组酵母接种到5ml YPD液体培养基中,30℃,250 r/min摇床培养,当A600值为3左右时,将0.5 ml菌体转接至50ml YPD液体培养基中进行次级培养。培养24h后,4890 r/min离心5min,弃上清。用200 ml酵母膏胨脂培养基(YPM)重悬沉淀的菌体,30℃,250 r/min培养,并于诱导表达起始后,每隔24h补加1 ml 100%的甲醇溶液。诱导表达3 d后,4℃,5060 r/min离心10min去菌体回收上清液。
1.2.4 硫酸铵分段盐析在离心后回收的上清液中加入不同饱和度的硫酸铵进行分段盐析,1h静置后,10 000 r/min离心30min,用1ml磷酸缓冲液溶解沉淀,并装入透析袋于10倍体积的磷酸缓冲液中4℃透析,每2h更换缓冲液一次。透析12h后,Bradford法测定蛋白浓度[6]。
1.2.5 底物活性十二烷基磺酸钠-聚丙烯酰胺凝胶电泳(SDS-PAGE)分析在制备SDS-PAGE分离胶时加入0.1%(w/v)的酪蛋白,浓缩胶的配制及电泳条件与SDS-PAGE方法相同。电泳后的凝胶先用2.5%的TritonX-100(曲拉通X-100,聚乙二醇辛基苯基醚)洗2次,每次30min,然后在含有2mmol/L半胱氨酸、1mmol/L乙二胺四乙酸二钠盐(EDTA)和0.01mg/ml木瓜蛋白酶的磷酸缓冲液(0.10mol/L,pH为6.0)中温浴(40℃)2.5h。经染色、脱色后用全自动图像分析系统进行扫描。
1.2.6 cC抑制活性曲线的测定测定cC的抑制活性曲线操作按文献[7]方法。
2 结果 2.1 天然氮末端重组cC的表达载体的构建和鉴定在本实验的引物设计中,将cC的第一个氨基酸Ser直接连在Glu-Lys-Arg的后面,同时在2条引物的末端加入了XhoI和XbaI酶切位点,直接与pPICZαA的XhoI和XbaI酶切片断相连接。其中上游引物包括表达载体pPICZαA的一部分(XhoI酶切位点)和cC成熟肽编码序列的第一个碱基开始的24个碱基,下游引物包括从cC成熟肽编码序列终止码开始反向的27个碱基和1个XbaI酶切位点。以含有cC cDNA的克隆质粒为模板,经PCR扩增得到约369bp(包括引物)的DNA片段,将该片段亚克隆到pGEM-T载体上后,用XhoI和XbaI双酶切,插入表达载体pPICZαA多克隆位点中(XhoI和XbaI双酶切大片断),然后转化大肠埃希菌DH5α。经XhoI和XbaI酶切,重组子有约367bp的片段插入,该重组质粒命名为pPICZα-cC。为进一步检测重组质粒中外源基因的改造结果是否有突变发生,对插入部分进行序列测定。测序结果表明,改造后的基因与预期设计的序列完全一致,扩增和构建中没有发生基因突变。
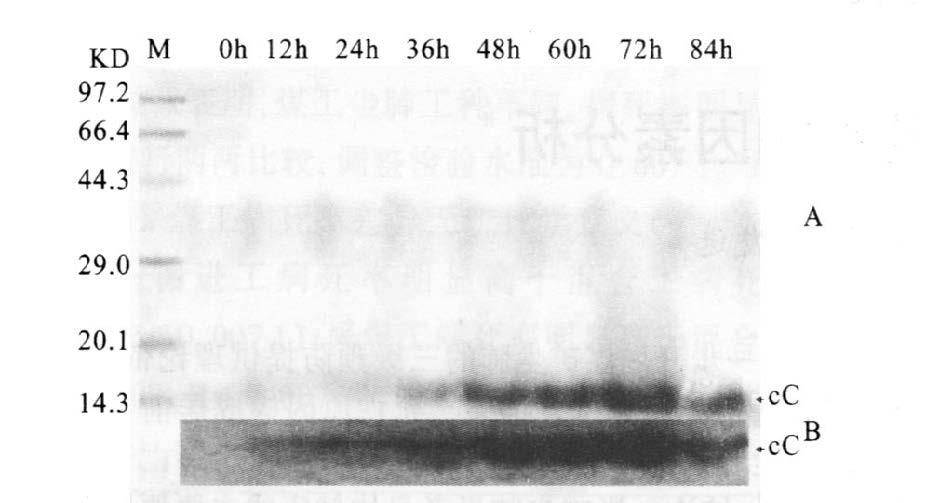
2.2 在毕赤酵母中表达的重组cC特性(图 1,2)酵母培养上清液经SDS-PAGE电泳及考马斯亮蓝染色后,可见重组蛋白条带,质量约为14kD,0h没有蛋白表达,12、24、36h所表达的蛋白略少,表达量随诱导时间的延长而增加,72h表达的蛋白表达量达到最高,而84h重组蛋白的量减少,可能是被培养液中蛋白酶降解所致。电泳后用TritonX-100除去凝胶中的SDS,然后将凝胶在木瓜蛋白酶溶液中温浴,木瓜蛋白酶便可分解凝胶中的底物(酪蛋白)。底物被分解处考马斯亮蓝染色时不着色,而重组cC所在位置保护了底物不被木瓜蛋白酶分解,用考马斯亮蓝染色时能被染色,因此,在透明背景下可见重组cC所在位置呈蓝色条带,根据蓝色条带的有无、灰度可定性和半定量判断cC抑制活性的高低。毕赤酵母所表达的重组cC经底物活性SDS-PAGE和考马斯亮蓝染色后,可见明显的具有抑制活性的蛋白条带,该条带的灰度与SDS-PAGE的条带灰度基本成对应关系。
|
注:图 1A:常规SDS-PAGE图谱分析;M:低分子量标准蛋白;诱导时间为0~84 h。图 1B:底物活性SDS-PAGE图谱分析:诱导时间为0~84 h。 图 1 诱导菌上清液的SDS-PAGE图谱分析 |
|
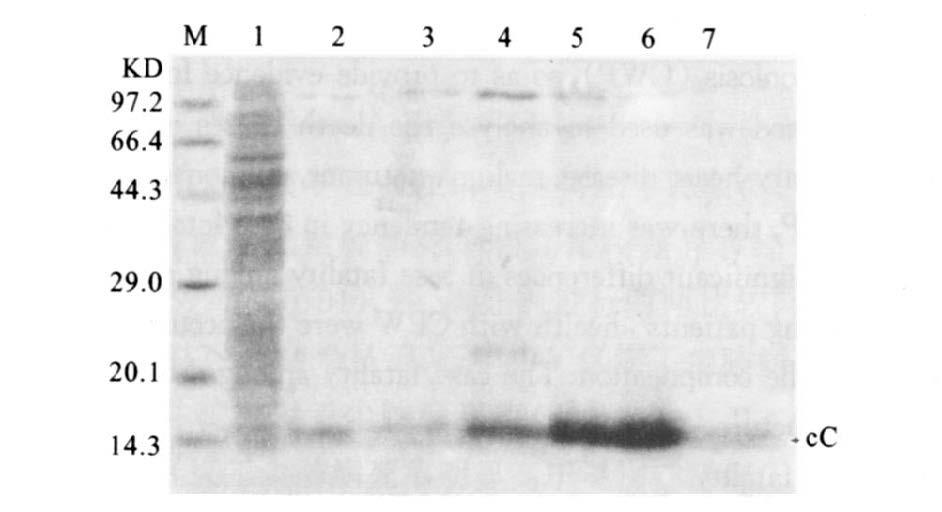
注:M:低分子量标准蛋白;1:诱导菌的菌体蛋白;2:培养基上清液中的可溶性蛋白;3,4,5,6,7:30%,40%,50%,60%,70%饱和度的硫酸铵沉淀出的蛋白分析。 图 2 硫酸铵梯度沉淀法纯化重组cC的SDS-PAGE图谱分析 |
诱导表达72h的上清液经Bradford法测定蛋白浓度约为2.95mg/ml,经SDS-PAGE凝胶用全自动图像分析系统扫描,重组蛋白占总蛋白的纯度为85.9%,表明在上清液中大部分都是cC和少量的杂蛋白。为了除掉这些杂蛋白,采取硫酸铵分段盐析方法,用10%,20%,30%,40%,50%,60%,70%饱和度的硫酸铵沉淀重组cC,用缓冲液溶解透析后利用SDS-PAGE检测,可以看到上清液经过50%~60%饱和度硫酸铵盐析后能得到所要表达的重组蛋白,其中在60%硫酸铵分划里重组cC占总蛋白的93.1%。
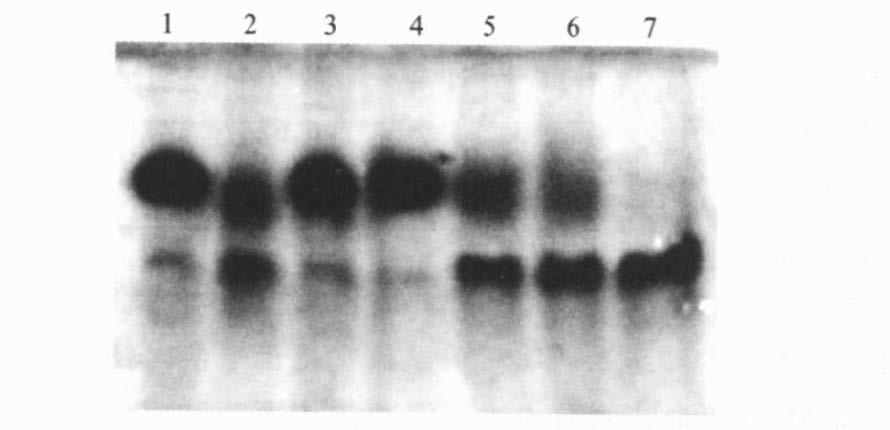
2.3 绝大多数的重组cC可形成分子内二硫键(图 3)不同量的β-巯基乙醇和盐酸胍(Gdn·HCl)处理cC样品进行Native-PAGE分析。电泳结果表明,未经β-巯基乙醇和盐酸胍处理的重组cC样品中,约92.9%的具有二硫键,而用不同量的β-巯基乙醇和盐酸胍组合处理后,随着二硫键被破坏的程度加深,cC的条带逐渐下移,5mol/L盐酸胍与10% β-巯基乙醇的组合几乎完全打开了分子内的二硫键。因此,Native-PAGE分析结果表明,在本实验所选用的毕赤酵母表达体系中,具有天然氮末端重组cC大多数可以形成分子内二硫键。
|
注:1:对照样; 2:3.3% β-巯基乙醇处理cC;3:0.5mol/L盐酸胍处理cC;4:5 mol/L 盐酸胍处理cC;5:3.3% β-巯基乙醇和5mol/L 盐酸胍处理cC;6:6.6% β-巯基乙醇和5mol/L盐酸胍处理cC;7:10% β-巯基乙醇和5mol/L盐酸胍处理cC。 图 3 不同浓度β-巯基乙醇和盐酸胍对cC作用的Native-PAGE图谱分析 |
2.2 重组cC与天然cC相比具有相似的蛋白酶抑制剂活性
重组cC与天然cC在底物活性SDS-PAGE分析中没有明显的区别,重组cC和购买的天然cC的的抑制活性相似,但是重组cC的活性略低,这可能与重组cC的二硫键形成比率有关。另外,重组cC的量在0.75μg以内时,抑制活力随重组cC增加成比例增强,具有很好的线性关系,直线回归方程为y=0.5086x+0.0148(R2=0.9677)。当重组cC的量大于0.75μg时,曲线逐渐呈现平缓趋势,不符合上述直线回归方程,这可能是由于竞争性抑制作用,此时木瓜蛋白酶已经完全被抑制的原因。由此可见,重组cC与天然cC具有相似的蛋白酶抑制活性,暗示重组cC与天然的cC相比具有相似的三级结构。
3 讨论以往在毕赤酵母中表达得到的cC的氮末端常含有一定长度的残余信号肽,不仅在一定程度上影响cC的天然活性,更重要的是有可能对利用cC研究形成淀粉样纤维的机制起到干扰作用。本实验通过独特的引物设计在毕赤酵母表达系统中首次成功表达了具有天然氮末端的有抑制活性的重组cC。文献[3]的表达量(34.4±0.5)mg/L对比,本实验中72h后表达量(28.2±1.5)mg/L略低,可能与Glu-Ala重复子对于Kex2的切割效率有一定的影响有关。
另外,利用本试验方法表达出来的重组cC,经Native-PAGE电泳,表明绝大部分具有分子内二硫键,说明具有天然氮末端的cC可更好的保持其天然三维结构不被破坏。这种在酵母体内的成功表达具有天然氮末端的cC,还可以为利用酵母细胞研究分子伴侣对蛋白表达调控提供科学有效的模型。有研究曾利用酵母表达体系研究蛋白二硫键异构酶家族之一的EPS1蛋白对可形成淀粉样纤维的具有二硫键溶菌酶及cC的分泌量和活性的调控。结果表明EPS1蛋白在酵母蛋白质量调控途径中的重要作用[8]。而该研究是基于混有多余的Glu-Ala 重复子的重组cC的,因此,具有天然氮末端的cC的成功表达将为该方面的研究提供更为科学合理的依据。
| [1] | Chen GH, Tang SJ, Chen CS, et al. High-level production of recombinant chicken cystatin by Pichia pastoris and its application in mackerel surimi[J]. Agric Food Chem, 2001, 49 : 641–646. DOI:10.1021/jf000992s |
| [2] | Sanders A, Jeremy Craven C, Higgins LD, et al. Cystatin forms a tetramer through structural rearrangement of domain-swapped dimmers prior to amyloidogenesis[J]. Mol Biol, 2004, 336 : 165–178. DOI:10.1016/j.jmb.2003.12.011 |
| [3] | He JW, Song YT, Nobuhiro U, et al. Characterization of recombinant amyloidogenic chicken cystatin mutant I66Q expressed yeast[J]. Biochem, 2005, 137(4) : 477–485. DOI:10.1093/jb/mvi064 |
| [4] | 江善宗. 生物技术在水产食品加工上之应用—利用生物技术生产鱼肉蛋白降解抑制剂[J]. 福州大学学报: 自然科学版, 2002, 11(30) : 672–680. |
| [5] | Bedi GS, Zhou T, Bedi SK. Production of rat salivary cystatin S variant polypeptides in Escherichia coli[J]. Arch Oral Biol, 1998, 43(3) : 173–182. DOI:10.1016/S0003-9969(98)00011-9 |
| [6] | 汪家政, 范明. 蛋白质技术手册[M]. 北京: 科学出版社, 2002: 8. |
| [7] | 马冬梅, 白俊杰, 简清, 等. 中华鲟半胱氨酸蛋白酶抑制剂在毕赤酵母中的表达和活性分析[J]. 生物工程学报, 2003, 19(5) : 598–602. |
| [8] | Jianwei He, Sakamoto T, Song Y, et al. Effect of Eps1p deletion in Saccharomyces cerevisiae on the secretion of foreign proteins which have disulfide bridges[J]. FEBS Letters, 2005, 579 : 2277–2283. DOI:10.1016/j.febslet.2005.03.019 |
 2008, Vol. 24
2008, Vol. 24

