辽宁省自1985年将流行性乙型脑炎(乙脑)疫苗纳入计划免疫后,乙脑发病率大幅降低,尤其是2000年以来一直维持较低发病率水平。2007年9月辽宁省东部某市乙型脑炎发病数急剧上升,蚊虫监测显示,乙脑主要传播媒介三带喙库蚊密度指数明显增加。为了解辽宁省乙型脑炎病毒状况及其变化,本文采用逆转录-聚合酶链式扩增(RT-PCR)分析了该地区蚊虫标本病毒分离株基因型别。现将结果报告如下。
1 材料与方法 1.1 材料 1.1.1 标本采集2007年8月16日~9月1日,选择该市3个乡镇的39个畜舍,采用诱蚊灯于每天19:00~21:00采集蚊虫,采集分类后每50只为1批,装入冻存管于液氮罐中冻存。共采集77批蚊虫标本,其中74批为三带喙库蚊,其余3批为淡色库蚊。
1.1.2 细胞及试剂金黄色地鼠肾细胞系(BHK-21)细胞为本实验室保存;RNA提取试剂盒(Rneasy mini kit)和胶回收试剂盒(Quick GelExtration Kit)(美国Qiagen公司);PCR产物克隆用载体pMD19-T、JM109感受态细胞、AMV逆转录酶及TaqDNA聚合酶(日本TaKaRa公司);其他试剂均为分析纯。
1.1.3 参考毒株基因Ⅰ型(GⅠ)9株,其中中国参考株5株,分别为SH-53、SH-81、SH-83、SH-96和SH-101;韩国2株,为K94P05和KV1899;日本和柬埔寨各1株,分别为Ishikawa和M859。基因Ⅱ型(GⅡ)2株,为分离自马来西亚的JE827和MaSAr01994。基因Ⅳ型(GⅣ)2株,为分离自印度尼西亚的JKT7003和JKT8442。基因Ⅲ型(GⅢ)8株,其中中国参考株6株,分别为Ha-3、Beijing-1、HW、p3、SA14-14-2和SA-14;日本和印度各1株,分别为JaOArS982和GP78。西尼罗病毒(WN)分离自美国。
1.1.4 引物用Primer5Premier引物设计软件,参照SA14-14-2参考株序列,设计2对乙脑病毒特异性引物,引物序列如下:(1) JEV258:5′TAGTTTACAGCATTAGCCCCGACCA3′;JEV1584:5′CGTAAAACGCTTCAGTGTTCAGTCC3′;扩增片段长度1327bp。(2)E1300:5′TTGGTAAGGGAAGCATTGACACA3′;E2465:5′GGTCGCTAAGAACACGAGCACAC3′;扩增片段长度1166bp。引物由北京三博远志生物技术有限责任公司合成。
1.2 方法 1.2.1 蚊虫标本处理及病毒分离参考文献[1]方法,从液氮罐中取出冻存管,将蚊虫标本迅速倒人研磨器中,加入Eangle,s液1 ml清洗,吸出液体后再加入l ml Eangle,s研磨液,反复研磨至组织碎片基本消失为止。将研磨液吸入离心管,4℃,12 000 r/min离心20 min。用0.22 μm孔径滤器过滤上清液。取0.5 ml过滤液接种BHK-21细胞,置37 ℃、5%CO2培养箱,1 h后弃去接种液体,加入7 ml细胞维持液(血清含量为2%),细胞置于37 ℃、5%CO2培养箱中继续培养,逐日观察细胞病变;在BHK-21细胞中连续盲传3代,弃去无病变者,将发生病变者连续传代,使之出现规律病变。
1.2.2 病毒RNA提取及RT-PCR鉴定按Rneasy mini kit操作说明,从病变细胞维持液中提取病毒RNA;提取纯化后的RNA保存在-80 ℃冰箱中备用。以提取的病毒RNA为模板,分别用2种乙脑病毒特异性下游引物(JEV1584和E2465) 在AMV逆转录酶的作用下逆转录获得病毒cDNA,反应条件为42 ℃,逆转录60 min,95 ℃变性10 min。然后以病毒cDNA为模板进行PCR分析,PCR反应条件:94 ℃预变性3 min,94 ℃变性1 min,55 ℃退火1 min,72 ℃延伸1 min 30 s,35个循环,72 ℃延伸10 min。PCR结束后,扩增的特异性片段经1.5%琼脂糖凝胶电泳鉴定;以2对引物扩增均获得预计大小的片段为阳性判定标准。
1.2.3 基因克隆、测序及序列分析阳性PCR产物采用Quick Gel Extration Kit回收后克隆于质粒pMDl9-T载体,转化大肠埃希菌JM109感受态细胞,通过蓝白斑筛选与菌落PCR鉴定,PCR扩增阳性的克隆由北京三博远志生物技术有限责任公司测序。采用Chen等[2, 3]建立的乙脑病毒基因分型法进行基因分型。采用Blastn对数据库进行比较,序列分析为Dnastar软件。碱基配对用ClustalX软件,以西尼罗病毒为外群(outgroup),采用Mega 3.1软件中的邻位相连法(Neighbor-joining)构建进化树,确信限度估计设为1000[4]。
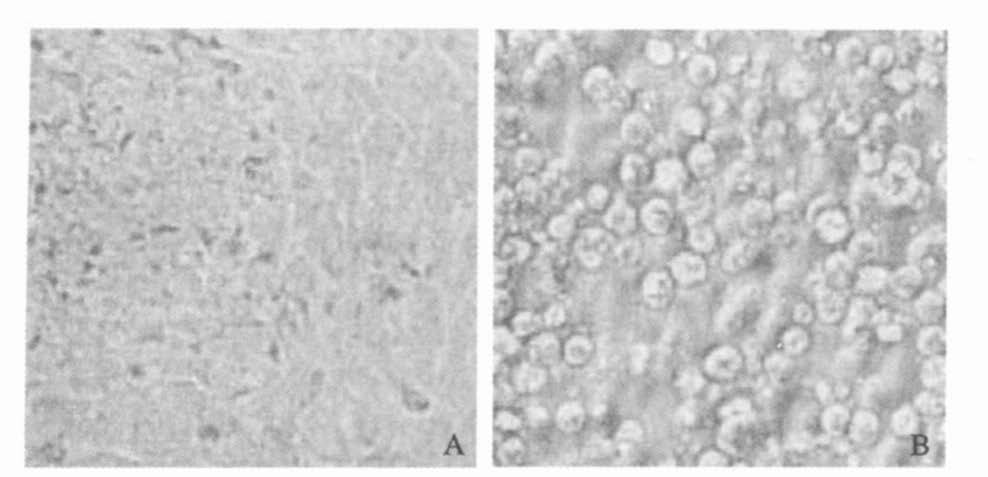
2 结果 2.1 病毒分离(图 1)77批蚊虫标本研磨液分别接种BHK-21细胞后,共有22批细胞出现规律性病变。细胞病变集中在72 h~96 h;病变表现为聚集、圆缩和脱落;病变全部来自三带喙库蚊标本。
|
注:A:正常BHK21细胞(对照);B:感染病毒的BHK21细胞 图 1 感染及未感染的BHK21细胞(×400) |
2.2 分离株RT-PCR检测(图 2)
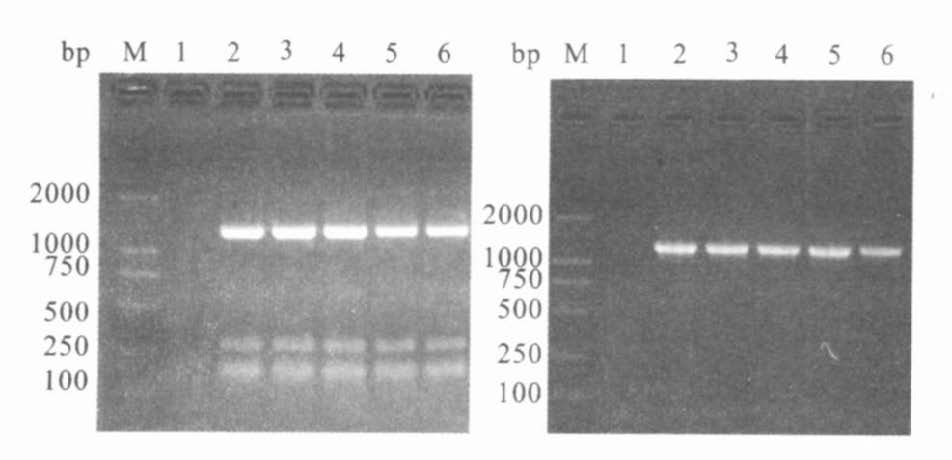
从病变细胞维持液中提取病毒RNA 22株,PCR扩增结果表明,22株病毒均为乙脑病毒。
|
注:M:DNAMarker;1:阴性对照;2~6:病毒分离株。A:使用引物JEV258和JEV1584扩增;B:使用引物E1300和E2465扩增。 图 2 PCR扩增产物的电泳图谱 |
2.3 病毒DNA序列分析(图 3)
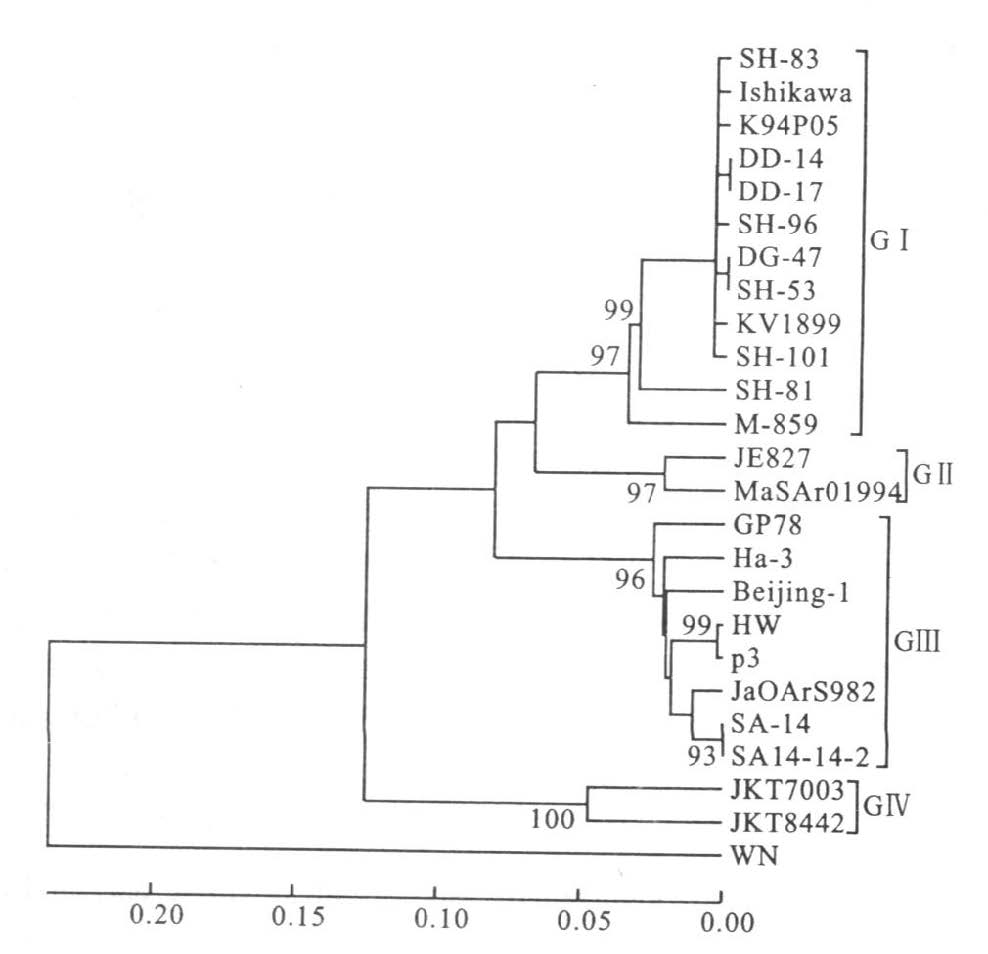
随机选择其中3株(DD14、DD17和DG47)进行基因分型。图 3可见,这3株乙脑病毒分离株同属基因Ⅰ型。
|
图 3 PrM基因核苷酸序列系统发生树分析 |
2.4 E基因编码Domain区段核苷酸及所编码氨基酸分析
用Dnastar对此区段1233个核苷酸(978~2210)进行分析。结果显示,DD14、DD17和DG47这3株病毒之间的核苷酸及其所编码氨基酸的同源性分别为99.3%和100%。这3株病毒与广泛使用的减毒活疫苗株SA14-14-2Domain相比,共有12个氨基酸位点变异,分别位于DomainⅠ的E-138(K→E)、E-176(V→I)、E-177(A→T)位,DomainⅡ的E-107(F→L)、E-129(T→M)、E-222(A→S)、E-244(G→E)、E-264(H→Q)、E-279(M→K)位,DomainⅢ的E-315(V→A)、E-327(S→T)、E-366(A→S)位。与K94P05株相比核苷酸和氨基酸同源性分别为98.6%~99.3%和99.5%,有2个氨基酸位点变异,分别位于DomainⅡ的E-76(M→T)位和E-244(Q→E)位。与SH-53株相比,也有2个氨基酸位点变异,分别位于DomainⅠ的E-176(V→I)位和DomainⅢ的E-327(S→T)位。此外,这3株病毒与SA14-14-2株相比还有位于Domain区段外E-439(R→K)和E-447(D→G)2个氨基酸位点变异。
3 讨论本文结果表明,分离自辽宁省东部某市3个乡镇蚊虫标本的22株病毒均为基因Ⅰ型乙型脑炎病毒,与K94P05株(韩国)、KV1899株(韩国)、Ishikawa株(日本)、M859株(柬埔寨)、SH-53(中国)等株[5]基因型别相同,是继2002年王俊文等[6]从我省分离到基因Ⅰ型乙脑病毒后再次分离到基因Ⅰ型乙脑病毒。22株病毒均分离于三带喙库蚊标本,淡色库蚊标本中未分离到病毒。沿海城市监测到大量三带喙库蚊且从中分离出乙脑病毒,提示辽宁省今后几年很可能出现一个乙脑的发病高峰。
乙脑病毒E基因编码病毒包膜糖蛋白,糖蛋白的活性区域由3个Domain、411个氨基酸残基组成[7, 8]。其中DomainⅢ参与受体结合,是重要的抗原决定簇;DomainⅢE-327位点又是决定抗原性的关键位点[9]。本文结果显示,日本Ishikawa株、韩国K94P05株与疫苗株SA14-14-2Domain相比,存在E-327(S→T)位点变异。本文分离到的病毒株与SA14-14-2株相比,同样存在E-327(S→T)位点变异,提示在辽宁省首次分离到乙型脑炎病毒变异株。
| [1] | 黄品贤, 宋花玲, 张忆萍, 等. 早春猪舍三带喙库蚊自然感染乙脑病毒调查[J]. 中国公共卫生, 2004, 20(11) : 1356–1357. |
| [2] | Chen WR, Tesh RB, RicoHesse R. Genetic variation of Japanese encephalitis virus in nature[J]. J Gen Virol, 1990, 71 : 2915–2922. DOI:10.1099/0022-1317-71-12-2915 |
| [3] | Chen WR, RicoHesse R, Tesh RB. A new genotype of Japanese encephalitis virus from Indonesia[J]. Am J Trop Med Hyg, 1992, 47 : 6l–69. |
| [4] | Van Den Hurk AF, Montgomery BL, Northill JA, et al. Short report:the first isolation of Japanese encephalitis virus from mosquitoes collected from mainland Australia[J]. Am J Trop Med Hyg, 2006, 75(1) : 21–25. |
| [5] | 王环宇, 付士红, 李晓宇, 等. 我国首次分离到基因I型乙型脑炎病毒[J]. 中华微生物学和免疫学杂志, 2004, 24 : 843–849. |
| [6] | 王俊文, 付士红, 王环宇, 等. 辽宁省乙脑病毒的分离与鉴定[J]. 中华实验和临床病毒学杂志, 2006, 20 : 61–65. |
| [7] | Kolaskar A S, Kulkarni-Kale U. Prediction of three-dimensional structure and mapping of conformational epitopes of envelope glycoprotein of Japanese encephalitis virus[J]. Virology, 1999, 261 : 31–42. DOI:10.1006/viro.1999.9859 |
| [8] | Mason PW, Dalrymple JM, Gentry MK, et al. Molecular characterization of a neutralizing domain of the Japanese encephalitis virus structural glycoprotein[J]. J Gen Virol, 1989, 70(Pt 8) : 2037–2049. |
| [9] | Solomon T, Ni H, Beasley DW, et al. Origin and Evolution of Japanese encephalitis virus in southeast Asia[J]. J Virol, 2003, 77(5)) : 3091–3098. |
 2008, Vol. 24
2008, Vol. 24

