2. 广西医科大学生理学教研室
血管内皮细胞已证明具有多种自分泌及旁分泌功能,为体内最大内分泌器官[1]。组织纤溶酶原激活物(tissHe plasminogen activator,t-PA)和纤溶酶原激活物抑制剂-1 (Plasminogen activatorinhibitor-1,PAI-1) 主要由内皮细胞产生[2]。内皮细胞结构和功能障碍可以减弱体内纤溶系统的功能,促进动脉粥样硬化的发生与发展。因此,从保护血管内皮细胞形态和功能研究新型有效的抗血栓药物,对血栓性疾病的防治具有良好的发展前景及临床使用价值。海带多糖具有抗血栓形成作用,能保护受损血管内膜完整性[3]。本文旨在探讨肾上腺素刺激下,海带多糖对体外人脐静脉内皮细胞t-PA和PAI-1表达和分泌的影响,从内皮细胞抗血栓功能方面探讨其对心血管系统的保护作用。
1 材料与方法 1.1 材料 1.1.1 细胞系人脐带静脉内皮细胞系ECV-304(上海午立公司)。复苏后于37℃,5%CO2培养箱中静置培养,传至3~4代。
1.1.2 海带多糖提取物从广西北部海湾购取海带,利用酶解碱浸提取并进一步分离纯化得一个多糖组分-L01。临用前用10%的小牛血清配成1g/L的贮液,过滤除菌,分装后40℃冰箱内保存备用。
1.1.3 主要仪器与试剂1450超净工作台(苏州市黄埔空调净化设备有限公司);CO2培养箱(美国Thermo Forma公司);XSB-1A倒置显微镜(梧州光学仪器厂);450(96 well Plate Reader)酶标仪(美国Bio-Rad公司)。肾上腺素针剂(广州明兴制药厂,批号:MD2301) ;胎牛血清培养液(美国Gibico公司);小牛血清(杭州四季青公司);胰蛋白酶(美国DIFCO公司);琼脂糖(西班牙Biowest公司);组织纤溶酶原激活物(t-PA)、纤溶酶原激活物抑制物(PAI-1) 试剂盒(上海西唐生物技术公司,批号为:0509103,0505219) ;W6701RNA抽提纯化试剂盒(上海华舜生物工程有限公司);K1621逆转录试剂盒(美国Fermentas公司);PCR扩增试剂盒(美国MBI公司);引物合成(上海生工生物公司)。
1.2 方法 1.2.1 细胞培养液中t-PA和PAI-1水平测定第3代HUVEC用10%小牛血清培养液制成1×105/ml细胞悬液,接种入24孔培养板中,37℃,5%CO2培养箱中培养24h待细胞基本融合处于对数生长期,随机分为6组,每组8孔,加入各种干预药物。实验分组:空白对照组为10%小牛血清,M-L01对照组(10μg/ml海带多糖L01) ,模型组(10μg/ml肾上腺素),L-L01低剂量组(1μg/ml海带多糖L01+10μg/ml肾上腺素)、M-L01中剂量组(10μg/ml海带多糖L01+10μg/ml肾上腺素)、H-L01高剂量组(100μg/ml海带多糖Lol+10μg/ml肾上腺素),分别于给药后24,48,72h收集培养液,采用酶联免疫吸附法检测培养液中的t-PA,PAI-1水平。
1.2.2 逆转录多聚酶链反应(RT-PCR)检测t-PA和PAI-ImRNA的表达细胞培养和分组方法同上,分别于给药后24,48,72h,收集细胞,提取总RNA,行RT-PCR,检测t-PA和PAI-1mRNA的表达。(1) 总RNA抽提:用W6701RNA抽提纯化试剂盒一步法提取细胞总RNA,紫外分光光度仪测定吸光度,波长A260nm/A280nm均在1.8~2.0之间,计算RNA含量。琼脂糖变性凝胶电泳鉴定RNA。(2) cDNA的合成:取RNA2μg采用AMV逆转录酶进行逆转录合成cDNA,按照反转录试剂盒说明步骤进行操作。PCR扩增:根据文献[4]设计引物。引物序列为:β-actine上游:5′-AAGCAGGAG TATGACGAGAGTCCG-3′;下游:5′-GCCTTCATACATCTCAAGTTG G-3′;t-PA上游:5′-CAGCGAGCCAAGGTGTT T-3′;下游:5′-GGCTGACCCATTCCCAAA-3′,PAI-1上游:5′-CAGACCAAGAG CCTCTCCAC-3′;下游:5′-ATCACTTGGCCCATGAAAAG-3′;反应体系为50μl;各组cDNA产物2μl,5U/μl Taq酶0.5μl,10×buffer5μl,dNTP5μl,β-actine上下游引物各1μl,t-PA或PAI-1上下游引物各1μ1,MgCl23μl,无菌双蒸水30.5μl,反应条件为94℃变性1min,61℃退火1min,72℃延伸1min,35个循环。每个PCR反应重复3次。2%琼脂糖凝胶电泳,并用溴化乙锭染色,凝胶成像系统扫描,测目标基因和β-actine条带的灰度比值,用二者的灰度比值代表目的基因相对表达含量。
1.3 统计分析采用SPSS 12.0统计软件,组间比较采用单因素方差分析。
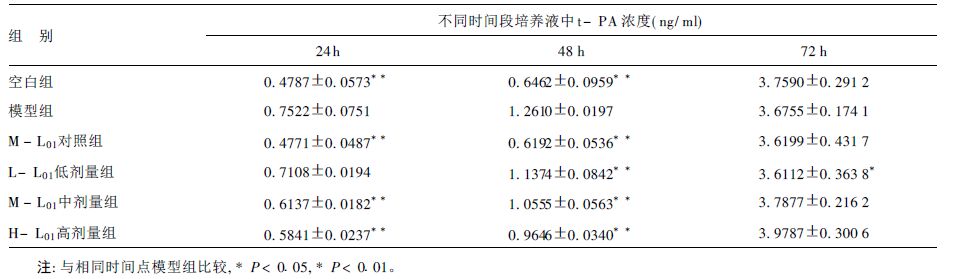
2 结果 2.1 肾上腺素和海带多糖L01对HUVEC分泌t-PA的影响(表 1)与空白对照组比较,M-L01对照组单独作用时,对HUVEC分泌t-PA无影响(P>0.05) 。给药24,48h后模型组培养液t-PA含量高于其他组,培养72h模型组培养液t-PA含量与其他组比较差异无统计学意义(P>0.05) 。与模型组比较,24h低剂量的L01组未表现出明显降低t-PA水平的作用,中高剂量的L01能够使培养液的t-PA含量明显降低(P<0.01) 。48h各浓度组的L01都能使培养液中的t-PA含量明显降低(P<0.01) 。
| 表 1 肾上腺素和海带多糖L01对HUVEC培养液中t-PA含量影响(x ± s, n= 8) |
2.2 肾上腺素和海带多糖L01对HUVEC分泌PAI-1影响(表 2)
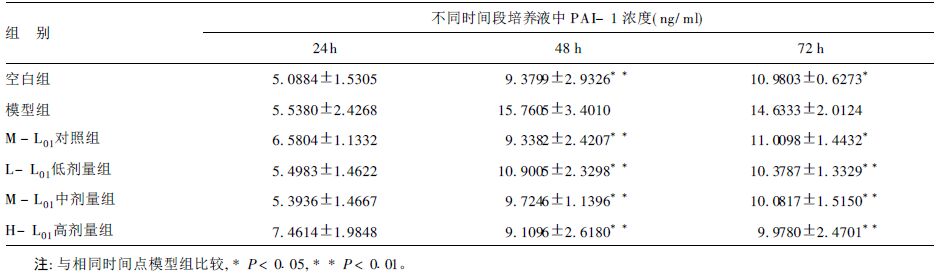
与空白对照组比较,M-L01对照组单独作用时,对HUVEC分泌PAI-1无影响(P>0.05) ;给药48,72h后模型组HUVEC培养液中PAI-1含量显著升高(P<0.01,P<0.05) 。与模型组比较,给药48,2h后L-L01,各剂量组均能显著抑制这种升高趋势(P<0.01) ,表明L013个剂量均能显著抑制肾上腺素刺激内皮细胞所致PAI-1分泌增加。
| 表 2 肾上腺素和海带多糖L01对HUVEC培养液中PAI-1含量影响(x ± s, n= 8) |
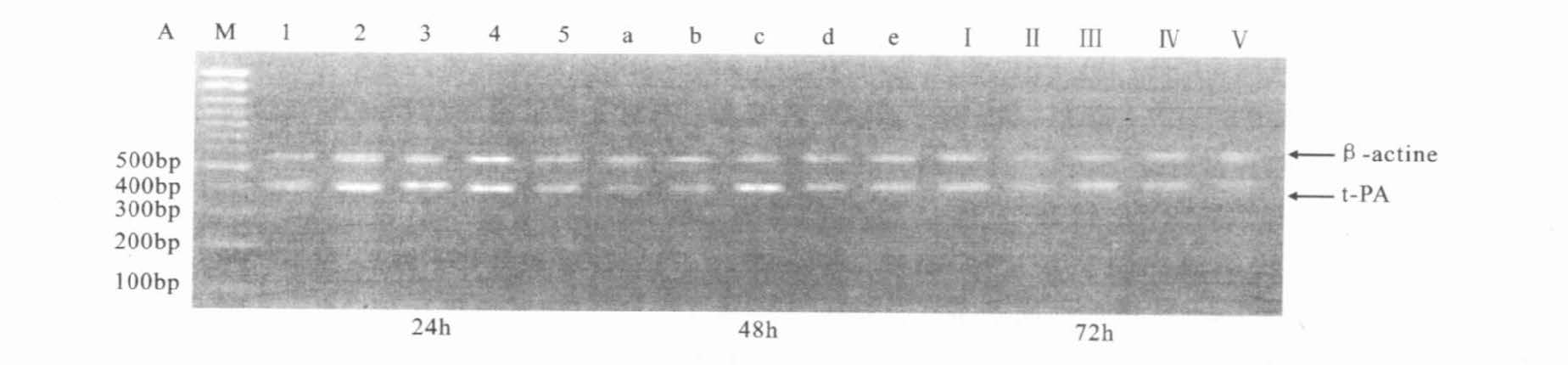
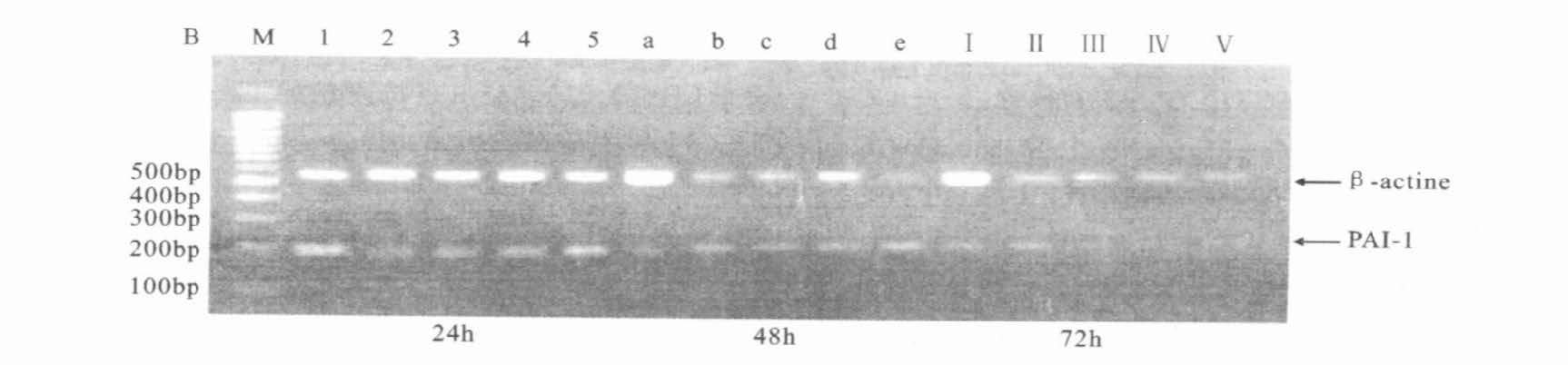
2.2.1 肾上腺素和海带多糖L01对内皮细胞t-PA及PAI-1的mRNA基因表达(图 1,图 2)
内皮细胞可以在转录水平表达t-PA及PAI-1,t-PA的mRNA PCR产物长度为409bp,PAI-1的mRNA PCR产物长度为202bp,β-actinePCR产物长度为559bp。
|
注:M:DNA分子量标准; 1,a,I:空白对照组; 2,b,II:模型组;3,c,III H-L01:高剂量组; 4,d,Ⅳ M-L01:中剂量组; 5,e,V L-L01:低剂量组。 图 1 各组不同时间t-PA表达的RT-PCR的检测结果 |
|
注:M:DNA分子量标准; 1,a,I:空白对照组; 2,b,II:模型组;3,c,III H-L01:高剂量组; 4,d,Ⅳ M-L01:中剂量组;5,e,V L-L01低剂量组。 图 2 各组不同时间点PAI-1mRNA表达的RT-PCR的检测结果 |
2.2.2 肾上腺素和海带多糖L01对内皮细胞t-PA及PAI-1的mRNA基因转录产物相对含量分析
经密度扫描半定量分析显示:各实验组和对照组比较,t-PA mRNA的表达各时间段均未见明显差异。与空白对照组比较,给药24h后各组PAI-1mRNA表达差异无统计学意义;48,72h后,模型组明显上调PAI-1mRNA的表达(0.650 8±0.025 0与0.814 2±0.069 8) (P<0.01) 。与模型组比较,HUVEC PAI-1mRNA表达明显下调,高剂量组(0.539 6±0.044 5) ,(0.573 8±0.039 3) (P<0.01) ;中剂量组(0.589 2±0.019 3) ,(0.578 5±0.042 9) (P<0.05,P<0.01) ;低剂量组72h(0.647 1±0.077 1) (P<0.05) ,表明L013个剂量组均能在不同程度下调肾上腺素所致HVECPAI-1mRNA表达增加。
3 讨论实验中应用儿茶酚胺类药肾上腺素刺激脐静脉内皮细胞后,24和48h培养液中t-PA含量明显增高。而联合给海带多糖L01各浓度组相同时间段t-PA含量均有不同程度的下降,且具有一定量效关系。72h培养液中t-PA含量各组均升高,但差异无统计学意义。当L01单独加入到培养液时,t-PA含量无明显影响。同时,肾上腺素刺激人脐静脉内皮细胞48h和72h,培养液中PAI-1含量明显增加,尤其以48h增高更为明显,PAI-1mRNA的表达明显上调。而联合海带多糖L01组分泌PAI-1明显减少,PAI-lmRNA明显下调。肾上腺素对PAI-1的影响是通过诱导PAI-1mRNA及其产物的表达来实现的。在心脑血管系统中,PAI-1含量的增高,血液处于高凝状态,可能会导致动脉硬化、血栓形成,这对机体是不利的。海带多糖L01通过在转录水平上影响和调节PAI-1的分泌,使PAI-1分泌减少,减少这种不利因素,防止血栓形成。因此,t-PA抗原水平和PAI-1活力对抗共同反映了纤维蛋白溶解作用和内皮功能。t-PA和PAI-1抗原的增高表示患者的纤溶功能的降低,其原因可能为血管内皮细胞受到激惹或损伤导致t-PA和PAI-1合成与释放紊乱有关[5, 6]。实验中t-PA和PAI-1含量在肾上腺素刺激下不同时间段,都不同程度有所上升,但PAI-1上升更为明显,且其合成也增加,故t-PA/PAI-1比值下降。海带多糖L01能够拮抗肾上腺素的这种作用,使t-PA/PAI-1比值升高,从而增加自发性纤溶活性,而发挥抗血栓作用。
| [1] | Lehman, Edward BS, Halltt JW, et al. Circulating and tissue endothelial immunoreactivity in advanced atherosclerosis[J]. N Engl J Med, 1991, 325 : 997–1001. DOI:10.1056/NEJM199110033251404 |
| [2] | Van Mourik, Lawtence DA, Loskutoff DJ. Purification of an inhibitor of plasminogen activator(antiactivator) synthesized by endothelial cells[J]. Biol Chem, 1984, 259 : 1491–1492. |
| [3] | 谢露, 陈蒙华, 刘爱群. 海带多糖对血管损伤大鼠血小板活性的影响[J]. 中国公共卫生, 2005, 2l(8) : 95–960. |
| [4] | Saed G M, Diamond M P. Modulation of the expression of tissue plasminogen activator and its inhibitor by hypoxia in human peritoneal and adhesion fibroblasts[J]. Fertility Stertility, 2003, 79(1) : 164–168. DOI:10.1016/S0015-0282(02)04557-0 |
| [5] | 王志坚, 赵水平. 心力哀竭患者纤溶参数变化及药物干预效果的评价[J]. 中国循环杂志, 2002, 17(1) : 38–40. |
| [6] | 陈世德, 陶新智, 伍伟锋. 慢性心力哀竭患者血浆组织型纤溶酶原激活物和纤溶酶原激活物抑制物-1含量变化及其临床意义[J]. 临床荟萃, 2004, 19(13) : 724–726. |
 2008, Vol. 24
2008, Vol. 24