多年来,伤寒和副伤寒的诊断都是经过普通培养和生化试验,主要为细菌培养和肥达氏凝集反应。传统的阳性诊断一般需要4~5 d。因此,有必要发展更快速准确的新的诊断方法。PCR方法用于伤寒和副伤寒诊断常用的靶基因有fliC-d基因[1]、Vi抗原基因[2]和16S rRNA基因[3]。但因为相同基因的存在,单一的靶基因往往许多非伤寒血清型的沙门菌也有阳性条带,因此特异性不强。本文根据Vi抗原基因(viaB)、H抗原基因(filC-a)和O抗原合成基因(rfbS和rfbE)为靶基因设计特异性引物,采用复合PCR方法确定和区别伤寒和甲型副伤寒沙门菌血清型。现将结果报告如下。
1 材料与方法 1.1 材料(1) 试验菌株:伤寒沙门菌12株、甲型副伤寒沙门菌12株、其他沙门菌23株、霍乱弧菌2株、枸橼酸杆菌2株、大肠埃希菌3株,共54株,由本室保存或本所菌种保藏中心提供。(2) 主要试剂与仪器:Tap NDA聚合酶、100bp NDA Ladder(加拿大BBI公司);dNTP(上海生工公司);PCR仪(德国Biorad公司)。
1.2 方法 1.2.1 引物设计根据rfbS、rfbE、flic和vi基因序列设计PCR引物[4],由上海生物工程有限公司合成。引物序列(5′-3′)如下:(1) rfbS-1:CTTGCTATGGAAGACATAAACGAACC;rfbS-2:CGTCTCCATCAAAAGCTCCATAGA;(2) rfbE-1:GAGGAAGGGAAATGAAGCTTTT;rfbE-2:TAGCAAACTGTCTCCCACCATAC;(3) fliC-1:AATCAACAACAACCTGCAGCG;fliC-2:TAGTGCTTAATGTAGCCGAAGG;(4) vi-1:GTTATTTCAGCATAAGGAG;vi-2:CTTCCATACCACTTTCCG。
1.2.2 PCR模板的制备各菌株由普通营养琼脂划线培养过夜,以无菌接种环刮取菌落,于100 μl灭菌水中混匀,煮沸10 min;12 000 r/min离心5 min,取上清,以无菌水适当稀释的作为扩增模板。
1.2.3 PCR反应体系10×Buffer 5 μl、dNTP Mixture(2.5 mol/L)3μl、引物rfbS-1(5 μmol/L)1μl、引物rfbS-2、rfbE-1、rfbE-2、fliC-1、fliC-2(5 μmol/L)各2 μl、引物vi-1、vi-2((5 μmol/L)各3 μl、模板2 μl、Taq酶(5U/μl)0.5 μl,MgCl2 3 μl,总反应体积为50 μl。95℃预变性5 min;95℃变性50 s,57℃退火50 s,72℃延伸50 s,共30循环;最后1次循环延伸72℃ 5 min。反应完毕后扩增产物经2%琼脂糖凝胶电泳鉴定。
1.2.4 特异性检测54株试验菌株1.2.2制备模板,进行复合PCR反应体系的特异性检测。
2 结果 2.1 复合PCR检测方法的建立4对引物的浓度及退火温度进行优化,找到不同引物的合适比例,用同一反应管可以很清晰地扩增出不同菌株的预期片段。
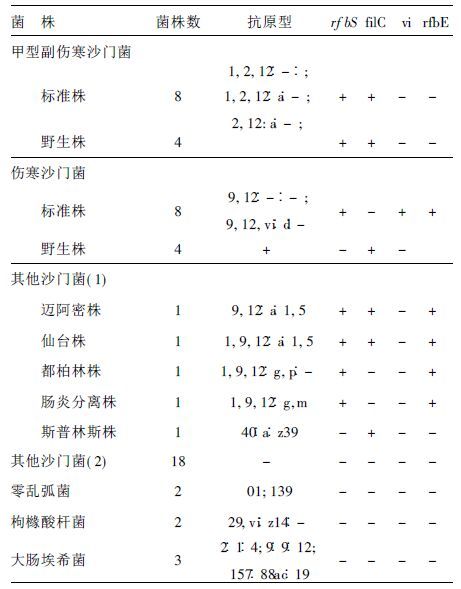
2.2 54株不同菌株特异性分布(表 1)表 1可见,伤寒和甲型副伤寒沙门菌rfbS基因均为阳性,rfbS基因还可检出沙门菌属O2和O9群菌株。其他在复合PCR中可产生阳性条带的沙门菌菌株,如迈阿密、仙台、都柏林、肠炎、斯普林斯株等沙门菌血清型,因具有O9或H∶a血清型,虽然可产生相应的阳性条带,但均与甲型副伤寒和伤寒沙门菌产生的带型不同,可以完全区分开。
| 表 1 54株不同菌株PCR扩增反应特异性分布 |
2.3 不同菌株PCR特异性图谱(图 1)
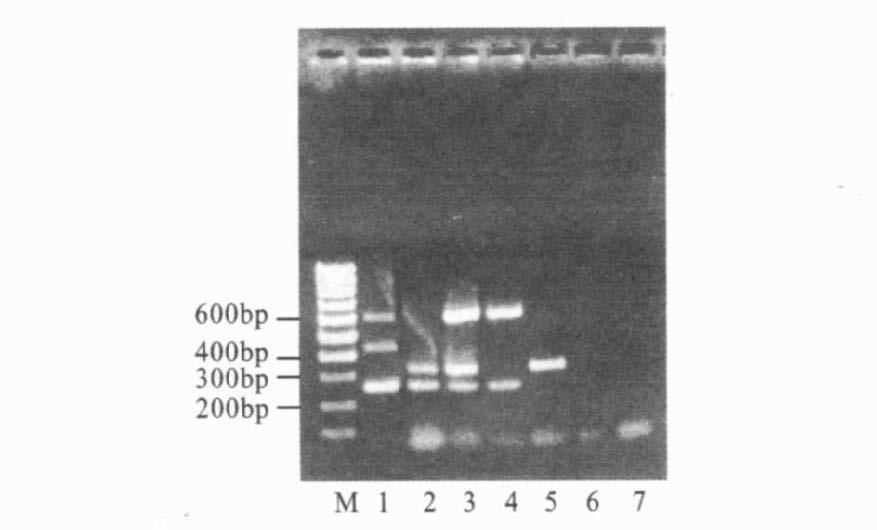
图 1可见,伤寒沙门菌(包括8株标准菌株和4株临床分离的野毒株)均出现258,439和615 bp条带,甲型副伤寒沙门菌(包括8株标准菌株和4株临床分离的野毒株)均出现258和329 bp条带。该2种菌株的带型与其他沙门菌或其他菌株可完全分开。
|
注: M : 100 bp DNA Ladder; 1: 伤寒杆菌; 2: 甲型副伤寒杆菌; 3: 迈阿密与仙台株沙门菌; 4: 都柏林与肠炎株沙门菌; 5: 斯普林斯株沙门菌; 6: 其他沙门菌; 7: 阴性对照。 图 1 不同菌株的PCR反应条带 |
3 讨论
本文结果表明,rfbS基因存在于伤寒和甲型副伤寒沙门菌,但甲型副伤寒沙门菌中的rfbS基因并不能编码有活性的CDP-泰威糖差向异构酶,因为有1个碱基的缺失导致读码框的位移变异使第4位密码子转变为终止密码子。本研究以缺失区域设计引物来特异性扩增伤寒沙门菌的rfbS,而甲型副伤寒沙门菌的该基因不被扩增。
一般认为,伤寒沙门菌均含有Vi抗原一种与其毒性密切相关的抗原。Wain等[5]对巴基斯坦伤寒高发区的临床样本分离的2 222株伤寒沙门菌进行检测,发现只有12株经Vi血清凝集试验阴性,而其中11株经PCR检测含Vi抗原基因,这一结果经对伤寒沙门菌Vi抗原最敏感的免疫荧光法得到证实。因此,绝大多数伤寒沙门菌均含有Vi抗原基因,即使Vi血清凝签订试验证实其表型为Vi抗原阴性,但它们的基因组中仍含有Vi抗原基因。其他仅有很少几种细菌也具有Vi抗原,如丙型副伤寒沙门菌(Salmonella dublin)。本试验中仅有伤寒沙门菌可扩增出Vi基因的特异性439 bp条带,而对于同样产Vi抗原的丙型副伤寒沙门菌(6,7,vi∶c∶1,5) 和枸橼酸杆菌(29,vi∶z14∶-),虽然血清凝集试验证实有很强的Vi血清凝集反应,但复合PCR却不能扩增出Vi基因的阳性条带,可能是因为不同血清型菌株其Vi基因的内在序列存在差异所致,有待进一步探讨。
本研究的复合PCR方法对于检测伤寒和甲型副伤寒沙门菌特异性很强,但该方法以纯化的单菌落菌株为模板,是否适合直接检测临床标本还有待于进一步研究。
| [1] | Massi MN, shirakawa T, Gotoh A, et al. Rapid diagnosis of typhoid fever by PCR assay using one pair of primers from flagellin gene of salmonella typhi[J]. J Infect, Chemother, 2003, 9(3) : 233–237. DOI:10.1007/s10156-003-0256-4 |
| [2] | Hashimoto Y, Itho Y, Fujinaga Y, et al. Development of nested PCR based on the ViaB sequence to detect salmonlla typhi[J]. J Clin Microbiol, 1995, 33 : 775–777. |
| [3] | Zhu Q, Lim CK, Chan YN. Detection of salmonella typhi by polymerase chain reaction[J][J]. J Appl Bacteriol, 1996, 80 : 244–251. DOI:10.1111/jam.1996.80.issue-3 |
| [4] | Hirose K, Itoh KI, Nakajima H, et al. Selective amplification of tyv(rfbE), prt(rfbS), viaB, and fliC genes by multiplex PCR for identification of salmonella enterica Serovars Typhi and Paratyphi A[J]. J Clin Microbiol, 2002, 40(2) : 633–636. DOI:10.1128/JCM.40.02.633-636.2002 |
| [5] | Wain J, House D, Zafar A, et al. Vi Antigen expression in salmonella enterica Serovar Typhi clinical isolates from Pakistan[J]. J Clin Microbiol, 2005, 43(3) : 1158–1165. DOI:10.1128/JCM.43.3.1158-1165.2005 |
 2008, Vol. 24
2008, Vol. 24