2. 安徽省淮南市新华医院
肝硬化是肝脏纤维结缔组织弥漫性增生伴有肝细胞结节状再生,是肝细胞在多种因素作用下反复损伤的慢性病理过程。外周血单个核细胞(peripheral blood mononuclear cells,PBMC)是多种免疫细胞集合体,含多种免疫活性细胞,分泌产生多种细胞因子。白细胞介素-8(interleukin-8,IL-8) 为1987年第一个被发现并克隆的CXC家族(C为半胱氨酸,X为任意氨基酸)趋化因子[1],有ELR+结构,是潜在的血管生成因子。为了解IL-8在介导肝硬化发病机制中的作用,筛选29例慢性乙肝后肝硬化患者,检测外周血IL-8及其mRNA水平。现将结果报道如下。
1 材料与方法 1.1 临床资料我校教学医院2005年9月~2006年12月收治的HBV感染后肝硬化患者,其中男20例,女9例,平均年龄(44.5±8.9) 岁,其中代偿期17例,失代偿期12例,HBV-DNA(+)10例,丙氨酸转氨酶(ALT)升高13例,天冬氨酸转氨酶(AST)升高15例,AST/ALT>1.017例,临床诊断符合2005年全国病毒性肝炎会议修订诊断标准[2],病程均超过6个月,无合并HAV、HCV、HDV、HEV、HIV感染及其他自身免疫性疾病,3个月内未系统使用抗病毒和免疫抑制剂治疗。另选25名本市中心血站体检正常献血员为对照组,其中男16名,女9名,平均年龄(32.0±9.1) 岁。
1.2 试剂与仪器聚蔗糖-泛影葡胺(Ficoll-Hypaque)(上海试剂二厂);HBV-DNA诊断试剂(上海中亚基因研究所);ELISA法 IL-8试剂盒(法国DLACLONE公司);Trizol试剂(美国Invitrogen公司);cDNA合成试剂(上海申能博采生物科技有限公司);半自动生化仪-ECOM-F6124(德国eppendorf公司);EXL808全自动酶标仪和EXL-50X全自动洗板机(美国Bio-Tek公司);LightCycler FastStart DNA Master SYBR GreenⅠ(德国Roche公司);iCycle(R)荧光实时定量PCR仪(美国Bio-Rad公司)。
1.3 方法 1.3.1 标本采集分批采取患者晨起空腹静脉血5ml,分别置2支含肝素的无菌eppendorf管和2支洁净的eppendorf管。肝素抗凝血以Ficoll-Hypaque常规分离PBMC,普通管常规分离血清备检。
1.3.2 HBV-DNA检测取100μl待测血清加入等体积的细胞裂解液,提取HBV-DNA模板,采用荧光定量PCR法,按照试剂盒说明操作。HBV上游引物(5′→3′):ACT GTT CAA GCC TCC AAG CTG,下游引物(5′→3′):CCC GAG ATC TTC TGC,扩增片段长度600bp。扩增参数为94℃预变性5min,然后94℃ 50s,55℃40s,72℃ 90s,循环35次,72℃延长4min,4℃保存,琼脂糖凝胶电泳,紫外透射仪下判断结果。
1.3.3 血清IL-8检测采用ELISA法。以试剂盒提供标准品绘制标准曲线,每批检测设空白、阴性、阳性对照各2孔,取100μl待测血清和100μl辣根过氧化物酶标记的抗趋化因子单克隆抗体,加至包被有相应趋化因子单克隆抗体的酶标反应板孔内,37℃孵育1h,磷酸盐(PBS)缓冲液洗涤5次,加100μl底物3-3甲基苯并噻唑啉-6-磺酸盐,室温30min,加2mol/L H2SO4终止反应,在EXL808全自动酶标分析仪上(450±2) nm处读取吸光度(A)值,每孔测定2次,取均值,依标准曲线确定血清IL-8含量。
1.3.4 PBMC中IL-8mRNA检测采用Real-time PCR法。将抗凝血用等量无Ca2+、Mg2+的Hank's液稀释,分离的PBMC以1640完全培养液调整细胞数至(1~2) ×109个/L悬液,以Trizol试剂抽提PBMC总RNA,并逆转录为cDNA,置-86℃冰箱备检。以SYBR GreenⅠ荧光标记法检测PCR产物,总反应体系为25μl,包括上下游引物各0.4mmol/L,MgCl2 2.5mmol/L,Ex-Taq 1.25U,dNTPs,2mmol/L 1×PCR buffer (500mmol/L KCl,100mmol/L Tris,20μg/L gelatin,pH 8.3) ,2×SYBRTM GreenⅠ液。2μl标准品或模板cDNA,模板cDNA以1∶5稀释。趋化因子引物设计参照Hirata等方法进行[3, 4],IL-8上游引物(5′→3′):CTT TGT CCA TTC CCA CTT CTG A,下游引物(5′→3′):TCC CTA ACG GTT GCC TTT GTA T,扩增片段长度306bp;甘油醛-3-磷酸脱氢酶(GAPDH)上游引物(5′→3′):ACC ACA GTC CAT GCC ATC AC,上游引物(5′→3′):TCC ACC ACC CTG TTG CTG TA,扩增片段长度452bp。PCR 扩增反应参数如下:95℃预变性300s,然后95℃ 50s,55℃ 40s,72℃ 90s共35个循环,最后72℃延伸300s。为克服系统误差以甘油醛-3-磷酸脱氢酶(GAPDH)为参照,以log cDNA/log GAPDH比值代表其mRNA水平。
1.4 标准品和标准曲线制备以GAPDH为对照,将起始浓度为(106 copies/μl)的GAPDH,按1:10设6个梯度浓度稀释,即106,105,104,103,102,0copies/μl。
1.5 统计分析IL-8含量及其mRNA水平以x±s表示;采用SPSS 11.5软件进行t或t′检验;Excel进行相关分析。
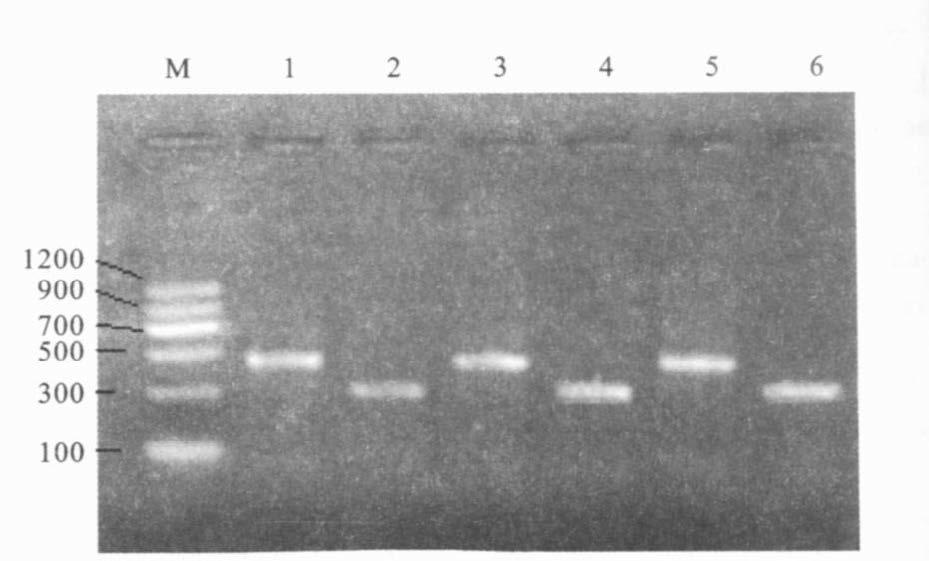
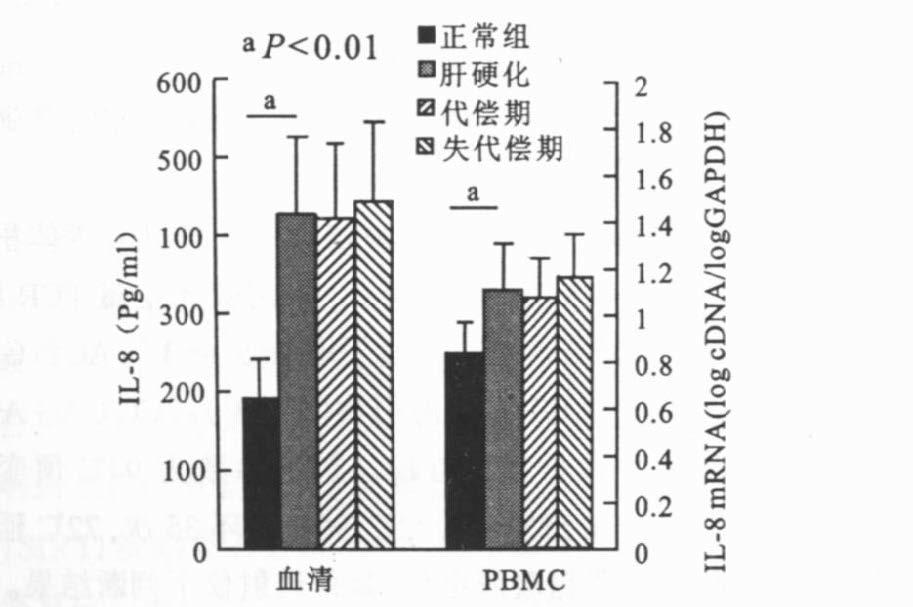
2 结果 2.1 IL-8及其mRNA表达(图 1,图 2)HBV感染后的肝硬化患者血清内IL-8水平及PBMC内IL-8 mRNA含量均显著高于正常对照组(P<0.01) ,且失代偿期略高于代偿期。
|
图 1 肝硬化患者外周血IL-8及其mRNA水平 |
|
注:1,2:对照者;3,4:患者1;5,6:患者2。1,3,5:GAPDH;2,4,6:IL-8。 图 2 PBMC内IL-8mRNA表达 |
2.2 IL-8与IL-8
mRNA相关性肝硬化患者血清内IL-8水平与PBMC内IL-8 mRNA表达相关(r=0.5465,P<0.005) 。
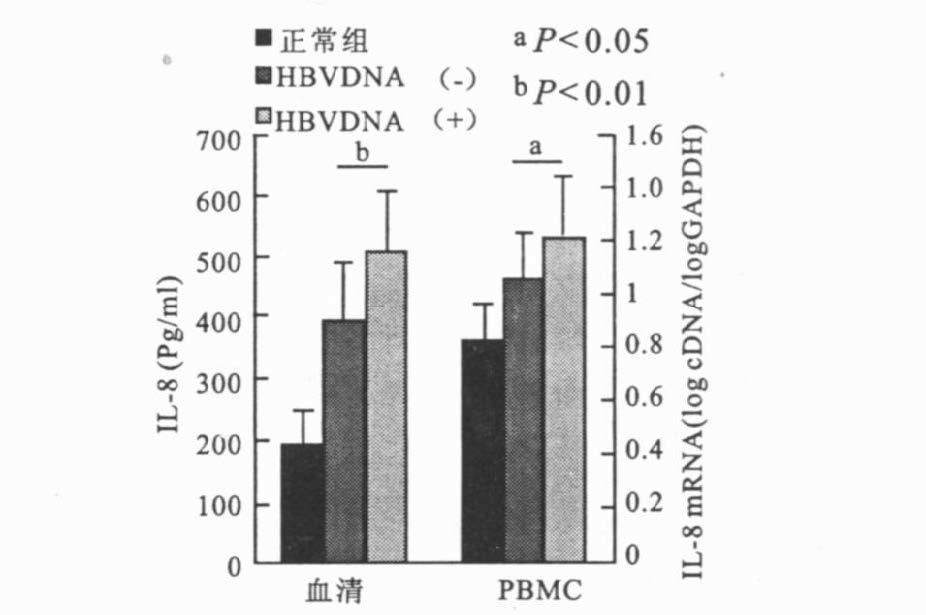
2.3 血清HBV-DNA与IL-8水平关系(图 3)29例肝硬化患者中HBV-DNA(+)组血清内IL-8含量及PBMC内IL-8 mRNA表达水平均高于HBV-DNA(-)组(P<0.01,P<0.05) 。
|
图 3 IL-8及其mRNA与HBV-DNA关系 |
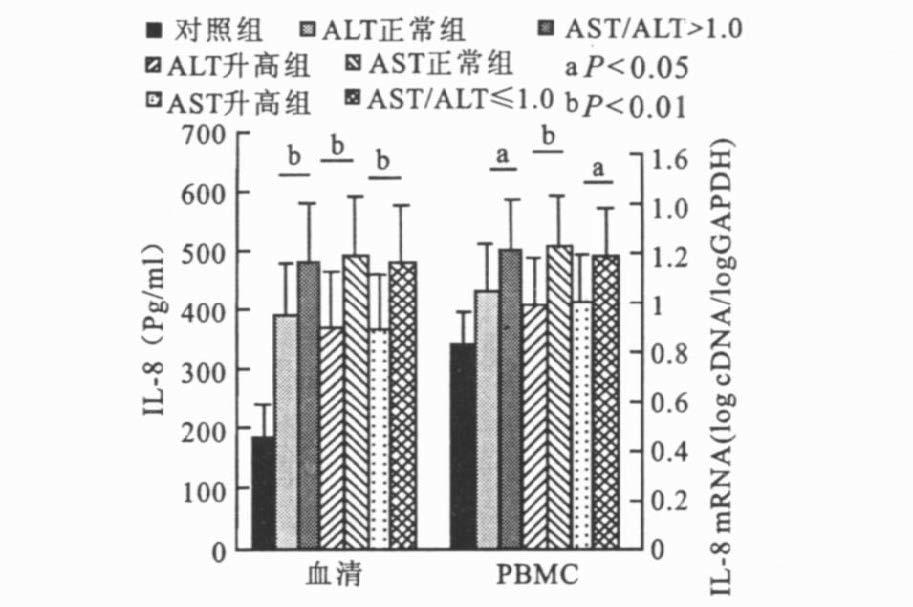
2.4 转氨酶水平与IL-8表达相互关系(图 4)
根据ALT、AST水平将患者分为ALT、AST正常组、升高组。IL-8及PBMC IL-8 mRNA水平与ALT及AST显著相关(P<0.05或P<0.01) ,且AST/ALT>1.0组高于AST/ALT≤1.0组(P<0.05或P<0.01) 。
|
图 4 IL-8及其mRNA表达水平与转氨酶关系 |
3 讨论
IL-8是一种具有高度活性的小分子多肽,可由多种免疫细胞如单核-巨噬细胞、T淋巴细胞及中性粒细胞以及HBV感染的肝细胞等分泌,LPS、IL-1、TNF-α可刺激其大量表达[5],通过对中性粒细胞及T细胞、单核细胞的趋化作用,本研究结果显示,HBV感染后肝硬化患者血清IL-8表达水平显著增高,与对照组相比,差异有统计学意义(P<0.01) 。肝硬化失代偿期IL-8及其mRNA的表达略高于代偿期,肝细胞受损加重,全身高动力循环,门脉高压,多系统受累,IL-8增高,间接激活肝星形细胞,胶原沉积,结缔组织增生,影响肝硬化的病理进程。采用Real-time PCR检测发现,肝硬化患者PBMC内IL-8 mRNA表达水平升高,与血清蛋白表达水平具有一致性,与对照组相比差异有统计学意义(P<0.01) ,提示PBMC中IL-8 mRNA高表达可能是导致血清IL-8水平升高的主要原因。Mahe等[6]研究发现,HBV-x蛋白转染细胞可刺激IL-8 mRNA及其蛋白水平表达增强。因此,检测PBMC中IL-8 mRNA的表达对了解肝脏的损伤程度有重要意义,可为肝损伤的早期诊断提供依据。
实验结果显示,肝硬化患者病毒复制组IL-8及其mRNA表达水平与非复制组相比较,差异有统计学意义(P<0.05或P<0.01) ,提示IL-8表达水平与病毒复制诱导的局部炎症反应程度有一定关系。HBV除可诱导肝细胞合成大量的肿瘤坏死因子-α(tumor necrosis factor alpha,TNF-α)外,还可作为TNF-α强刺激剂,直接诱导单核巨噬细胞产生TNF-α,升高的TNF-α可进一步诱导肝细胞、Kupffer细胞及PBMC、内皮细胞合成和释放大量IL-8,扩大其生物学效应。
实验结果显示,肝硬化患者IL-8及其mRNA的含量与ALT、AST水平呈正相关,表明IL-8的表达水平在一定程度上反映肝硬化的炎症活动状况,对了解肝硬化的进展有重要意义。肝细胞损伤主要来自宿主的免疫应答[7],HBV感染机体内免疫复合物增加,刺激机体产生大量的TNF-α、IL-6等前炎症因子,这些因子本身可诱使肝脏微循环障碍,血液通透性增加,全身高动力循环,肝细胞水肿变性,继而坏死,ALT、AST大量释放入血,并可刺激IL-8表达增强。肝硬化患者肝功能异常,功能性肝细胞数目及活性减少,使趋化因子的分解代谢障碍,可能是IL-8增加的重要原因。
综上所述,HBV感染后肝硬化患者外周血IL-8及其mRNA水平升高,通过趋化中性粒细胞、单核细胞等,释放促炎性细胞因子,引起炎症反应,并在清除肝炎病毒的同时,刺激纤维组织增生,加重肝细胞损伤和炎症反应。
| [1] | 王健, 赵金红. 趋化因子受体研究进展[J]. 现代预防医学, 2006, 33(2) : 165–171. |
| [2] | 中华医学会肝病学分会、感染病学分会. 慢性乙型肝炎防治指南[J]. 中华肝脏病杂志, 2005, 13(12) : 881–891. |
| [3] | Hirata H, Arima M, Cheng G, et al. Production of TARC and MDC by naive Tcells in asthmatic patients[J]. J Clin Immunol, 2003, 23(1) : 34–45. DOI:10.1023/A:1021948214742 |
| [4] | Haque NS, Zhang X, French DL, et al. CC chemokine I-309 is the principal monocyte chemoat tractant induced by apolipoprotein (a) in human vascular endothelial cells[J]. Circulation, 2000, 102(7) : 786–792. DOI:10.1161/01.CIR.102.7.786 |
| [5] | 肖纯凌, 王任群, 赵肃, 等. 大气污染对大鼠肺炎性细胞因子影响[J]. 中国公共卫生, 2007, 23(1) : 83–84. |
| [6] | Mahe Y, Mukaida N, Akiyama M, et al. Hepat it is Bvirus X protein transactivates human interleukin-8 gene through acting on nuclear factork B and CCAAT/enhancer-binding protein-like cis-elements[J]. J Biol Chem, 1991, 266(21) : 13759–13763. |
| [7] | 王平平, 王健. H BV 致病的细胞分子机制[J]. 广东医学, 2006, 27(3) : 128–130. |
 2008, Vol. 24
2008, Vol. 24

 , 项桂菊2, 胡孝彬2
, 项桂菊2, 胡孝彬2