2. 第四军医大学西京医院中医科;
3. 第四军医大学预防医学系流行病学教研室;
4. 陕西省妇幼保健院产科
孕妇孕期使用乙肝免疫球蛋白(Hepatitis B immunoglobulin,HBIG)是阻断乙型肝炎病毒(Hepatitis Bvirus,HBV)宫内传播的主要方法之一。有研究认为,HBIG能降低孕妇体内HBV病毒载量,从而达到预防HBV宫内传播的效果[1, 2]。然而其保护作用及预防机制都存有争议[3]。本研究对HBIG的保护作用及其对孕妇体内HBV病毒载量、HBsAg滴度的影响机制进行探讨,为HBIG的应用提供进一步证据。
1 对象与方法 1.1 对象选取2002年10月~2004年10月在陕西省妇幼保健院待产、HBsAg阳性孕妇及其所产新生儿210名为干预组,孕妇平均年龄(27.2±2.3)岁;选取1993~1997年HBsAg阳性孕妇402例及其所产新生儿为对照组,孕妇平均年龄(24.4±3.6)岁。干预组于孕晚期使用HBIG,每月1次(200U/次),使用3~5次;具体剂量依据检测HBeAg状态、孕妇主观要求而定;对照组孕妇孕期不采取任何干预措施。
1.2 血清标本收集产前采集孕妇肘静脉血;采集新生儿出生24h内,未接受主、被动联合免疫前的股静脉血,1500r/min离心分离血清,-20℃保存备用。
1.3 孕妇乙肝标志物检测孕妇血清HBsAg、HBeAg采用酶联免疫试剂盒(ELISA)检测(上海科华生物工程股份有限公司),采用倍比稀释方法检测孕妇HBsAg滴度,然后用ELISA方法进行检测。采用PCR方法检测孕妇血清HBV DNA,引物、PCR反应条件见参考文献[4];PCR阳性标本再行荧光定量PCR检测(上海轩吴科技发展有限公司)。HBVDNA滴度>103拷贝/ml判为阳性,否则判为阴性;判为阳性者进一步量化。
1.4 宫内感染诊断标准干预组孕妇所产婴儿股静脉血HBsAg检测采用HBsAg诊断试剂(美国雅培公司),检测程序及结果判读由Abbott System自动完成,以信噪比(Signal/Noiseratio,S/N)≥5为宫内感染诊断标准。对照组宫内感染病例的诊断标准以Western杂交方法检测新生儿外周血HBsAg(美国雅培公司)。
1.5 统计分析采用SPSS 10.0软件进行分析。
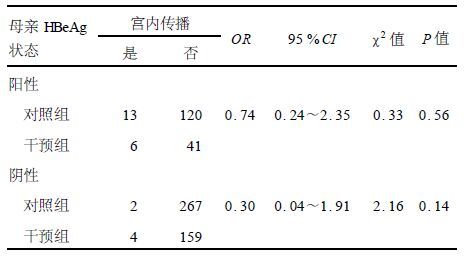
2 结果 2.1 孕期使用HBIG的保护作用(表 1)干预组210例孕妇中,HBeAg阳性47例,HBVDNA阳性40例;10例新生儿发生宫内感染。HBeAg阳性孕妇平均使用HBIG(3.85±1.25)次,HBeAg阴性孕妇平均注射(3.13±0.83)次。对照组HBsAg阳性孕妇402例中,HBeAg阳性133例;15例新生儿发生宫内感染。对照组和干预组孕妇HBeAg状态经χ2检验差异有统计学意义(χ2=7.98,P<0.01)。对孕妇HBeAg状态进行分层分析,分层后2组宫内感染率差异均无统计学意义,合并OR=1.06,说明孕期使用HBIG的保护作用有限。
| 表 1 HBIG干预组与历史对照组宫内感染率比较 |
2.2 HBIG使用剂量对孕妇病毒载量的影响 2.2.1 HBIG使用剂量与孕妇HBsAg滴度的关系
受血清标本量影响,本次共检测干预组孕妇血清HBsAg滴度179例,其中孕妇HBeAg状态、孕期HBIG注射剂量、宫内感染率等方面经统计学检验,与其余31例比较,差异均无统计学意义。46例孕妇血清HBsAg滴度<1:2000;26例为1:4000,51例为1:8000,26例为1:16000,18例为1:32000,8例为1:64000,2例孕妇滴度为l:1280000,2例孕妇滴度为1:2560000。HBIG注射剂量与HBsAg滴度相关系数:r=0.012(P=0.866)。
2.2.2 HBIG使用剂量与孕妇HBV DNA拷贝数的关系210例HBsAg阳性孕妇经过PCR检测,HBVDNA阳性40例;定量分析显示6例孕妇HBVDNA拷贝数为109个,有1例为108个,有10例为107个,有14例为106个,有2例为104个,103个0例,<103个3例。HBIG使用剂量与孕妇HBVDNA拷贝数相关系数r=0.039(P=0.836)。
3 讨论孕期使用HBIG是目前预防HBV宫内感染的常用措施,其主要依据是HBIG能中和病毒,降低孕妇体内的病毒载量,从而达到预防目的。然而HBIG的作用机制、预防效果都存有争议。高结坤等对HBsAg阳性孕妇使用HBIG,发现孕妇使用HBIG后新生儿血清HBsAg和HBVDNA检出率明显低于对照组,新生儿抗HBs阳性率显著高于对照组,其结论为孕期使用HBIG可预防宫内感染[4]。然而,Yuan等对HBsAg母亲及其新生儿进行长期随访,并持续监测孩子的外周血乙肝标志物,并没有发现HBIG保护作用[3]。本次研究未发现HBV DNA拷贝数、HBsAg滴度与孕期使用HBIG剂量的相关性,也未发现孕期使用HBIG对宫内传播具有保护作用。尽管没有收集到使用HBIG前HBVDNA拷贝数、HBsAg滴度等基线资料,但如此低的相关系数(接近于0),说明孕期使用HBIG对孕妇体内的病毒载量无影响。
预防HBV宫内感染,干预措施必须满足以下条件:(1)干预时机一定要在宫内传播发生时或之前,而目前关于宫内感染的时机还不确定[5, 6]。(2)HBIG对外周血HBV中和达到100%,而目前孕期使用剂量还远达不到[6]。本次研究发现,HBIG干预后宫内感染发生率为4.7%,与对照组比较差异无统计学意义,提示孕期使用HBIG不具保护作用。本次调查结果表明,孕期使用HBIG对HBV宫内传播保护作用有限;孕期使用HBIG对孕妇HBsAg滴度、HBVDNA含量无影响。
| [1] | Xiao XM, Li AZ, Chen X, et al. Prevention of vertical hepatitis B transmission by hepatitis B immunoglobulinin the third trimester of pregnancy[J]. Int J Gynaecol Obstet, 2007, 96(3) : 167–170. DOI:10.1016/j.ijgo.2006.11.011 |
| [2] | 高结坤, 胡先. 乙肝免疫球蛋白阻断乙肝病毒母婴垂直传播的研究[J]. 中国优生与遗传杂志, 2006, 14(10) : 45–46. |
| [3] | Yuan J, Lin J, Xu A, et al. Antepartum immunoprophylaxis of three doses of hepatitis B immunoglobulin is no effective:a single-centre randomized study[J]. J Viral Hepat, 2006, 13(9) : 597–604. DOI:10.1111/jvh.2006.13.issue-9 |
| [4] | Shao ZJ, Xu DZ, Xu JQ, et al. Maternal hepatitis B virus (HBV) DNA positivity and sexual intercourse arcassociated with HBV intrauterine transmission in China:a prospective case-control study[J]. J Gastroentero Hepatol, 2007, 22(2) : 165–70. DOI:10.1111/jgh.2007.22.issue-2 |
| [5] | Ranger RS, Alain S, Denis F, et al. Hepatitis viruses:mother to child transmission[J]. Pathol Bio (Paris), 2002, 50(9) : 568–775. DOI:10.1016/S0369-8114(02)00351-6 |
| [6] | 崔恒春, 闫永平, 邵中军, 等. 免疫预防后HBeAg 与HBV 宫内感染分析[J]. 中国公共卫生, 2006, 22(7) : 824–826. |
| [7] | Samuel D. Management of hepatitis B in liver transplantation patients[J]. Semin Liver Dis, 2004, 24(Suppl 1) : 55–62. |
 2008, Vol. 24
2008, Vol. 24

 , 姜庆五3, 徐剑秋4
, 姜庆五3, 徐剑秋4