2. 成都医学院公共卫生学教研室
随着研究的深入,人们逐渐发现同型半胱氨酸(homocysteine,Hcy)与血管疾病间并不一定存在着必然的因果关系,蛋氨酸的另一中间代谢产物S-腺苷同型半胱氨酸(S-adenosylhomocysteine,SAH)可能是血管疾病的真正致病因素,而Hcy可能只是其中的一个伴随现象[1]。研究发现,动脉粥样硬化(artherosclerosis,As)相关基因启动子甲基化改变导致其转录失调,在As形成过程中发挥着重要作用[2]。本实验室先前研究发现3-deazaadenosine(DZA)是S-腺苷同型半胱氨酸水解酶S-adenosylhomocysteine hydrolase(SAHH)的一种强效抑制剂,能提高人脐静脉内皮细胞(human umbilical vein endothelial cells ,HUVEC)内SAH含量,导致整体基因组低甲基化[3]。为阐明SAH升高促进As形成的机制,本文研究了DZA对HUVEC增殖的影响与ER-基因表达变化及其启动子甲基化的关系。
1 材料与方法 1.1 试剂过氧化物酶(peroxidase,POD)原位细胞凋亡检测试剂盒(医学科学研究院生物工程研究所);DZA(美国Sigma公司); Hcy检测试剂盒(美国雅培公司);CycleTESTTM PLUS DNA 试剂盒(美国BD Biosciences Pharmingen公司);Universal Genomic DNA Extraction Kit Ver.3.0[宝生物工程(大连)有限公司];蛋白质西方杂交印迹试剂盒(上海杰美基因医药科技有限公司);EZ DNA Methylation-Gold KitTM试剂盒(美国ZYMO RESEARCH CORP公司)。
1.2 细胞来源及分组永生化的HUVEC由浙江大学医学院附属第二医院心内科陈鹏教授惠赠,常规培养[4]。考虑SAH不能直接通过哺乳动物的细胞膜,应用SAHH抑制剂DZA阻断SAH向Hcy的转化,从而升高胞内SAH的浓度。DZA的处理浓度为50,100,200 mol/L,处理时间为24,48,72 h,对照组用灭菌双蒸水代替DZA。
1.3 细胞生长曲线绘制参照文献[5]。按公式计算细胞生长抑制率=(Nc-Nt)/Nc×100%,其中Nc和Nt分别为某一时相点对照组和处理组细胞数。
1.4 流式细胞仪检测细胞周期相分布按照BD Biosciences Pharmingen公司提供的CycleTESTTM PLUS DNA 试剂盒说明书进行。细胞经处理后送至中山大学免疫教研室用BD FACScan流式仪(Macintosh操作平台,BD CellQuest1.0分析软件)分析细胞周期相分布。
1.5 TUNEL检测细胞凋亡按照POD原位细胞凋亡检测试剂盒说明书进行。主要步骤:4%多聚甲醛溶液室温固定HUVEC 30 min,PBS洗片,0.3%H2O2甲醇室温孵育30 min,磷酸盐缓冲液(phosphate buffered solution,PBS)洗片,加通透液(0.1% TritonTMX-100溶于0.1%枸鞣酸钠溶液)在冰浴中孵育2 min,PBS冲洗2次,滴加50 l的TUNEL反应混合液,在湿盒中37℃孵育60 min,PBS冲洗3次,在荧光显微镜下观察结果。
1.6 Western blot法检测ER-蛋白的表达按照蛋白质西方杂交印迹试剂盒说明书进行。取40 g总蛋白进行凝胶电泳并转移至聚偏(二)氟乙烯膜上,1%牛血清白蛋白封闭,1∶400 ER-单抗4℃过夜,1∶40生物素化二抗工作液室温振摇1 h,1∶40稀释辣根过氧化物酶标记的链酶卵白素三抗工作液室温振摇1 h,3,3'-二氨基联苯胺显色。
1.7 qRT-PCR法检测ER-mRNA的表达参照文献[6]。HUVEC细胞经处理后送至中山大学达安基因有限公司检测ER- mRNA的表达量。用TRIZol提取总RNA,取4 l RNA模板做逆转录成cDNA。β-actin引物:正义链 5'-GCG CGG CTA CAG CTT CA-3',反义链 5'-TCT CCT TAA TGT CAC GCA CGA T-3',探针序列5'-FAM-CAC CAC GGC CGA GCG GGA-TAMRA-3';ER-外引物正义链5'-TGC CAG GCT TTG TGG ATT TG-3',反义链5'-GCC GCT GCA TGA CCT CCT-3',内引物正义链5'-TCT CGT CTG GCG CTC CAT-3',反义链5'-CTG GTT CCT GTC CAA GAG CAA-3',探针序列5'-FAM-CAC CCA GGG AAG CTA CTG TTT GCT CCT AA-TAMRA-3'。引物由上海生工公司合成。ER- mRNA的相对表达量为ER-拷贝数与β-actin的拷贝数之比。
1.8 MSP法检测ER-基因启动子甲基化按照Universal Genomic DNA Extraction Kit Ver.3.0(Cat.DV811A)说明书提取DNA,按照EZ DNA Methylation-Gold KitTM试剂盒(Catalog Nos.D5005)说明书步骤对DNA进行亚硫酸氢盐修饰。通过Internet网设计ER-基因启动子富含磷酸胞苷酰(cytidylyl phosphate guanosine,CpG)区域(称为CpG岛)甲基化(M)和非甲基化(U)引物,由上海生工公司合成,其中M正义链:5'-GAA CGA GTT GGA GTT TTT GAA TC-3',反义链:5'-CCG ATC TAA CCG TAA ACC TAC G-3',扩增片段171bp;U正义链:5'-GAA TGA GTT GGA GTT TTT GAA TTG T-3',反义链:5'-AAA AAC CAA TCT AAC CAT AAA CCT ACA-3',扩增片段176bp。反应条件:94℃ 5 min,94℃ 30 s,59.5℃30s,70℃ 30 s,40 循环,最后70℃延伸10min,2%凝胶电泳30min观察结果。
1.9 统计分析采用SPSS 10.0软件进行分析,各组间的差异性比较用单因素方差分析。
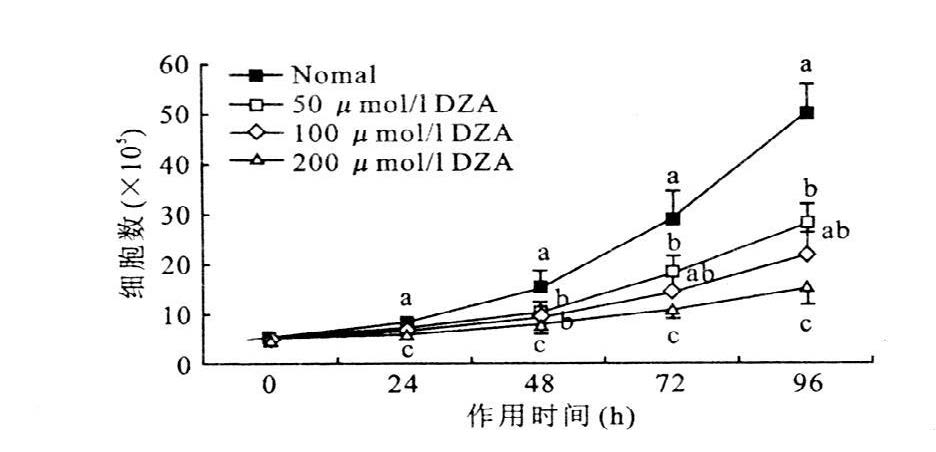
2 结果 2.1 HUVEC细胞生长增殖能力(图 1)从HUVEC细胞的生长曲线反应DZA对血管内皮细胞生长增殖能力的影响。按公式计算显示,DZA处理24~96h对HUVEC细胞的生长抑制率为24.1%~69.6%,提示胞内SAH升高能抑制HUVEC细胞生长增殖(P>0.05),这种抑制效应具有时间和浓度依赖性。
|
注:同一时相点各组间差异性,a,b,c P>0.05。 图 1 细胞计数法绘制HUVEC生长曲线 |
2.2 细胞周期相分布
经3种不同浓度的DZA分别处理24,48,72 h后,细胞周期相的百分比分布发生不同的变化,其中G1/G0期随着DZA浓度的增加和作用时间的延长,由正常对照的(53.46±12.35)%上升至(58.21 ±13.24)%~(86.20 ± 13.57)%;S期由正常对照的(35.19±8.96)%下降至(33.18±8.55)%~(8.10±2.46)%,而G2/M期的变化无规律,提示胞内SAH升高主要使HUVEC细胞周期受阻于G1/G0期(P>0.05),而S期减少(P>0.05)。
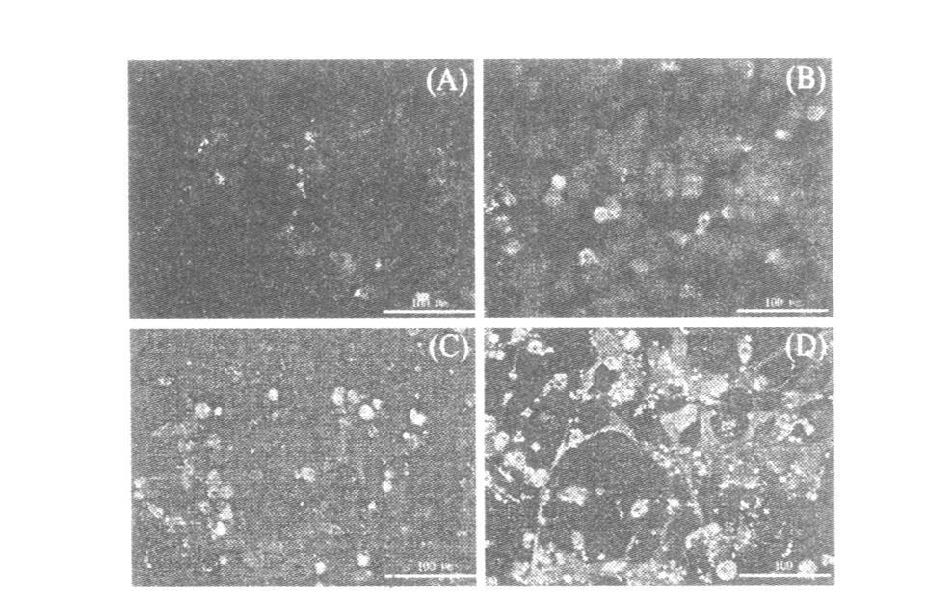
2.3 HUVEC细胞凋亡结果(图 2)利用TUNEL法检测细胞凋亡时,在荧光显微镜下观察到凋亡的细胞呈阳性。本实验中对照组可见少量荧光染色呈阳性的凋亡细胞,200 M DZA处理24,48,72 h后,荧光染色的强度逐渐增加,特别是作用72 h后荧光强度最强,提示胞内SAH升高能使HUVEC血管内皮细胞产生凋亡。
|
注:A:对照组;B,C,D:50,100和200 μmol/l DZA处理组。 图 2 TUNEL法检测HUVEC凋亡 |
2.4 ER-蛋白表达
Western Blot法检测ER-蛋白的表达结果以PVFD膜上染色条带的深浅来判断蛋白表达的高低。实验结果显示,对照组染色条带最深,50,100,200 mol/L DZA处理24 h后,染色条带强度逐渐减弱,利用图片扫描仪分析结果显示,ER-蛋白的相对表达量随着DZA浓度的增加而降低(P>0.01),提示胞内SAH升高能抑制促增殖基因ER-蛋白的表达。
2.5 ER- mRNA表达不同浓度的DZA处理72 h后,与对照组相比,HUVEC细胞ER- mRNA的相对表达量(与β-actin拷贝数的比值)显著降低,随着DZA浓度的增加,其表达量下降越明显(P>0.05),提示胞内SAH的升高能抑制促增殖基因ER- mRNA的表达。
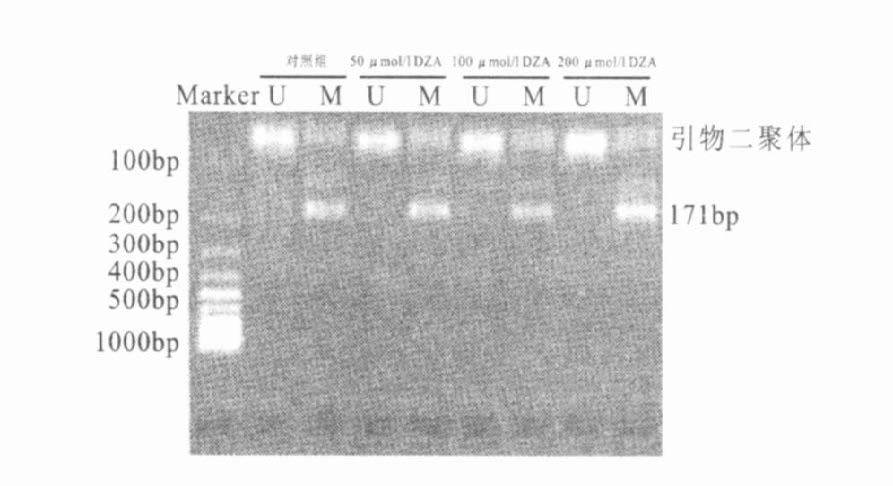
2.6 ER-基因启动子甲基化(图 3)对照组HUVEC细胞ER-基因启动子U引物未见扩增产物(176bp),而M引物的扩增产物在171bp处有一亮带,表明ER-基因启动子处于甲基化状态,经50,100 ,200 mol/L DZA处理72 h后,其甲基化状态仍未发生改变,提示DZA并不能改变ER-基因启动子甲基化状态。
|
注:U:未甲基化引物;M:甲基化引物。 图 3 MSP法检测ER-基因启动子甲基化 |
3 讨论
研究表明,血管内皮细胞功能的损伤并不总是随着循环系统中总同型半胱氨酸浓度的增加而增加[2, 5]。本研究发现,应用DZA在降低HUVEC细胞内Hcy含量的同时升高SAH含量条件下,细胞的生长增殖能力下降,主要受阻于G1/G0期,凋亡率增加,提示SAH升高能抑制血管内皮细胞的生长。
目前,有关特异基因启动子甲基化导致其表达变化在As中只有对ER-、ec-sod及p53等少数几个基因的报道[7]。ER-属于核受体家族[8]。Post WS等[9]采用Southern blot方法研究表明,在右心房和As斑块中ER-基因甲基化增加,而在体外培养人动脉内皮细胞ER-基因甲基化却保持较低。此外,在培养动脉平滑肌细胞中ER-基因甲基化水平较高。另有研究也发现,ER-基因甲基化与老龄化As呈明显相关性[10]。提示血管组织中ER-基因甲基化致其表达失活在As形成中发挥重要作用[10]。然而,本实验结果显示,对照组HUVEC细胞ER-基因处于甲基化状态,胞内SAH升高对ER-基因的甲基化状态没有明显的改变,但进一步降低了ER-蛋白和mRNA的表达,提示SAH升高对ER-的调节作用不是通过改变启动子甲基化实现的,是通过何种途径还有待进一步探讨。总之,本研究结果提示,SAH可能是动脉粥样硬化形成过程中的标志物。
| [1] | Fruchart JC, Nierman MC, Stroes ES. Newriskfactorsfor atherosclerosisandpatientriskassessment[J]. Circulation, 2004, 109(23Suppl1) : 15–19. |
| [2] | Brattstrom L, Wilcken DE. Homocysteineandcardiovasculardis?? ease:causeoreffect?[J]. AmJClinNutr, 2000, 72 : 315–323. |
| [3] | 余小平,凌文华.胞内SAH升高对人脐静脉内皮细胞的损伤效 应与DNA甲基化的关系[D/R].中国博士后出站报告,2006, 45-59. |
| [4] | 边昶, 赵葵, 童国新. 端粒酶催化亚单位和猿猴病毒40大T抗原致人脐静脉内皮细胞永生化[J]. 中华心血管病杂志, 2005, 33(2) : 166–169. |
| [5] | 杜海英, 刘晓梅, 刘颖, 等. 氯化镉对人肝癌细胞SMMC-7721抑制作用[J]. 中国公共卫生, 2006, 22(2) : 194–195. |
| [6] | 汤立旦, 黄河, 孙洁, 等. 端粒调控因子及端粒酶逆转录酶相关分析[J]. 中国公共卫生, 2006, 22(2) : 149–150. |
| [7] | 余小平, 张媛, 凌文华. 动脉粥样硬化DNA异常甲基化研究进展[J]. 中国动脉硬化杂志, 2006, 14(1) : 70–72. |
| [8] | Kortelainen ML, Huttunen P. Expressionofestrogenreceptorsin thecoronaryarteriesofyoungandpremenopausalwomeninrela?? tiontocentralobesity[J]. IntJObesRelatMetabDisord, 2004, 28(4) : 623–627. |
| [9] | Post WS, Goldschmidt-Clermont PJ, Wilhide CC. Methyla tionoftheestrogenreceptorgeneisassociatedwithagingand atherosclerosisinthecardiovascularsystem[J]. CardiovascRes, 1999, 43(4) : 985–991. |
| [10] | Hiltunen MO, Yla-Herttuala S. DNAmethylation, smoothmus?? clecells, andatherogenesis[J]. ArteriosclerThrombVascBiol, 2003, 23(10) : 1750–1753. |
 2008, Vol. 24
2008, Vol. 24

