2. 南开大学环境科学与工程学院
城市回用水作为可循环再利用的水资源可以部分缓解大城市(北京、天津)的严重缺水状况,可用于农田灌溉、市政景观用水、河道补充、居民冲厕和洗车等,甚至可以进行地下水回灌。但国外研究表明,城市污水处理后的排放出水中含有种类不同浓度的有毒有害物质[1],由于污水处理厂的出水对生态环境以及人类健康产生直接影响,因而其潜在的各种环境风险受到广泛关注,尤其是目前普遍关心的环境致突变物的潜在风险[2]。我国回用水方面研究起步较晚,处理工艺较落后,对于这一重要水资源的利用还处于起步阶段。国内此方面的实验研究报道多集中于某些具体化学污染物和病原微生物,且数量相对较少[3, 4]。为了解城市回用水的遗传毒性,进行了本研究。
1 材料与方法 1.1 试剂丝裂霉素C(MMC)(浙江海正药业股份有限公司);环磷酰胺(CP)(江苏恒瑞医药股份有限公司);S 9mix自制;RPMI Medium1640(美国Gibico公司);胎牛血清(美国Hyclone公司);胰酶、秋水仙碱、细胞松弛素B(Cyto-B),低渗液(0.075mol/L的KCl),固定液(甲醇:冰醋酸3:1),Giema染液,四甲基偶氮噻唑蓝(MTT,5mg/ml)、二甲基亚砜(DMSO)(美国Sigma公司)。试验菌株:TA98、TA100,经菌种鉴定5个遗传特性都符合其规定标准。细胞株:中国仓鼠肺成纤维(CHL)细胞(天津药物研究院)。染色体数目为25,核型稳定。
1.1.2 实验仪器自动固相萃取仪(美国Zymark公司);Rotavapor R-200旋转蒸发器(德国BCHI公司);固相萃取柱(英国International Sorbent Technology LTD公司),规格:3ml,500mg;CO2培养箱(美国Thermo forma公司);Finnpipette 41405微量加样枪(芬兰Labsytems公司);紫外可见分光光度计(北京通用仪器设备有限公司);20RP52D高速冷冻离心机(日本日立公司)。
1.2 水样的采集时间分别于丰水期(2005年8月)、枯水期(2006年3月)采集某城市污水处理厂回用水处理工艺中的入水和回用水。入水是经过污水处理工艺的二级出水,进一步经过混凝、过滤和消毒等回用处理工艺即为回用水。
1.3 实验方法 1.3.1 水样的预处理采集水样后加入1%甲醇溶液抑制微生物生长。加入硫酸调节pH=3左右,以孔径0.45m滤膜过滤水样。过滤后水样在IL中加入定量内标混标。(1)固相萃取柱的调理(condition):对水样进行固相萃取前,将C18固相萃取柱置于Zymark真空固相萃取仪上,先用10ml甲醇以5ml/min流速冲洗,然后以2×5ml去离子高纯水(流速5ml/min)冲洗。(2)水样的萃取:调理后同样以5ml/min流速萃取水样(1.0L)。萃取后,萃取柱用空气干燥10~15min,以除去残留的水分。吸附在C18柱上的化合物用2×2.5ml乙酸乙酯淋洗。乙酸乙酯淋洗所得萃取物用无水硫酸钠脱去水分,然后旋转蒸发浓缩,最后在35℃水浴用弱氮气进一步浓缩到约1ml。
1.3.2 Ames试验(1)按文献[5]试验设2000,1000,500,250ml/皿4个剂量,用DMSO配制,同时设溶剂对照。阳性对照为敌克松(50g/皿)。(2)每个剂量及对照均做3个平行样,并重复试验1次。在37℃培养48h,计数每皿回变菌落数。
1.3.3 体外胞质阻滞法微核试验取生长状态良好的CHL细胞5×105个接种于培养瓶内,加入4.9ml培养液培养24h,加入3种不同稀释浓度(浓度为)的受试液各100l,使每瓶染毒最终浓度为66.7,33.3,16.7ml,设3个平行样。阴性对照加入DMSO 100l,阳性对照丝裂霉素C(MMC),终浓度为0.1g/ml。染毒培养24h后更换新鲜培养液,加入细胞松弛素B(终浓度3g/ml),在37℃5%的CO2培养箱中培养18h,收集细胞。低渗2~3min后加入1ml甲醇-冰乙酸固定液,固定10min,离心弃上清。再加入固定液2ml如此反复固定2次,制成细胞悬液。将细胞悬液滴在载玻片上,自然风干。用10%Giemsa染液染色15~20min,蒸馏水分色30s,晾干后镜检阅片,照相。每个剂量组计数3000个双核细胞,每张载玻片计数1000个双核细胞,计算微核率()。用每1000个细胞的平均数及标准差,总微核数和与对照组的相对数表示,微核的出现呈泊松分布,比较试验组与对照组的差异。
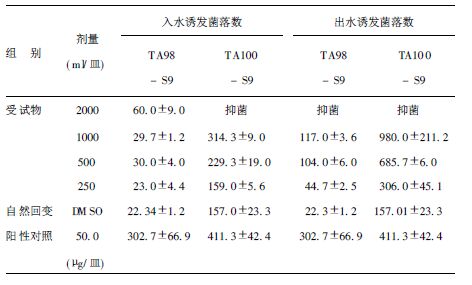
2 结果 2.1 Ames实验结果(表 1,2)| 表 1 丰水期城市回用水水样Ames试验结果( x ± s) |
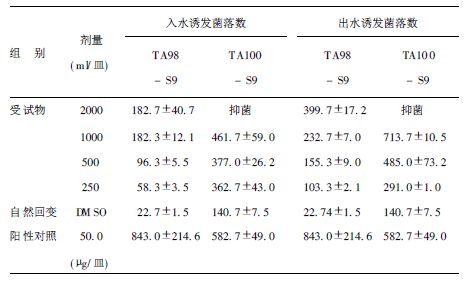
| 表 2 枯水期城市回用水水样Ames试验结果( x ± s) |
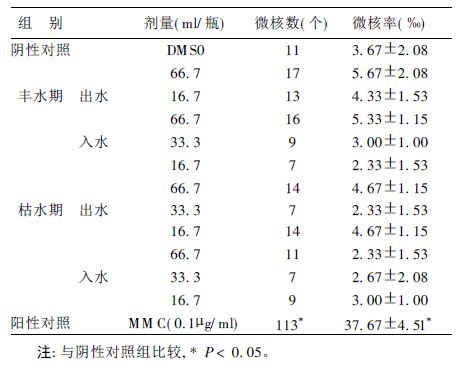
2.2 体外胞质阻滞微核试验结果(表 3)
表 3可见,丰水期和枯水期水样均未显示出明显的致突变性。
| 表 3 城市回用水CHL细胞体外胞质阻滞微核试验结果( x ± s) |
在体外胞质阻滞微核试验中,阳性对照组比阴性对照组微核率明显增加,且差异有统计学意义(P>0.05);水样各剂量组的微核率与阴性对照组比较,差异无统计学意义(P>0.05),城市回用水并未显示出明显的遗传毒性。
3 讨论近年来,我国北方大中型城市水资源紧张,城市排放污水回用(water recycling)的可行性研究得到了世界各国政府及学术界的广泛关注[6],尤其是其环境致突变物的潜在风险。在应用Ames试验对饮水样的研究发现,在相当于原水1000ml/皿剂量下2次水样萃取物TA98和TA100菌落回变数均超过自然回变菌落数的2倍,且呈剂量-反应关系,表明城市回用水具有一定的致突变作用。城市回用水处理后并未完全去除有机污染物,仍存在致突变物,也可能由于工艺流程设计上的原因,城市污水厂处理污水的过程中产生了新的致突变物质,如朱凤鸣[7]在对自来水的研究中发现,氯化消毒过程中,可产生致突变物卤代烃,表现出一定的致突变性。
体外胞质阻滞法微核试验是利用细胞松弛素B具有阻止细胞胞质分裂的特性,将所计数的细胞限制在分裂的双核细胞中,利用细胞微核率的变化来反映有害环境的遗传危害。在体外胞质阻滞微核试验中,阳性对照组比阴性对照组微核率明显增加,且差异有统计学意义(P>0.05);水样各剂量组的微核率与阴性对照组比较差异无统计学意义(P>0.05),城市回用水并未显示出明显的遗传毒性。城市回用水的遗传毒性强弱主要取决于水中污染物的种类、特性和浓度。本试验的阴性结果可能与细胞代谢活化相关,也可能是由于体现的遗传学终点和敏感性的原因。此外,城市回用水提取物为复杂的有机成分混合物,不同成分间可能存在复杂的相互作用也可能导致本试验为阴性结果。综上所述,城市回用水的遗传毒性尚有待深入研究。
| [1] | Kolpin D W, Furlong E T, Meyer M T. Pharmaceut icals, Hor mones, an d other organic waste w at er cont aminant s in U. S.st reams, 1999 -2000. A Nat ional Reconnaissan ce[J]. Environ ment al Science & Technology, 2002, 36 : 1201–1211. |
| [2] | Pet rovic M, Sole M, Lopez de Alda M, et al. Endocrine disruptors in sewage t reatment plant s, receiving river waters, and sediment s: in t egrat ion of chemical analysis and biological eff ect s on feral carp[J]. Environmental Toxicology and Chemist ry, 2002, 10 : 2146–2156. |
| [3] | 仇付国, 王晓昌. 城市回用污水中病毒对人体健康风险的评价[J]. 环境与健康杂志, 2003, 20(4) : 197–199. |
| [4] | 仇付国, 王晓昌. 污水再生利用的健康风险评价方法[J]. 环境污染与防治, 2003, 25(1) : 49–51. |
| [5] | 尹松年. 工业化学品鉴定规范及实验方法[M]. 北京: 人民卫生出版社, 1998: 52-57. |
| [6] | He Pingjing, Phan L, Gu Guow ei, et al. Reclaimed municipal w ast ewater-a pot ential w ater resouce in Ch ina[J]. Water S cience and T echnology, 2001, 43(10) : 51–58. |
| [7] | 朱凤鸣, 杨叶梅, 周俊杰, 等. 自来水中有机污染物的检测及评价[J]. 中国公共卫生, 2005, 21(12) : 1500–1501. |
 2008, Vol. 24
2008, Vol. 24