2. 山东省莱阳市第二人民医院泌尿外科;
3. 济宁医学院营养学教研室;
4. 兰州大学基础医学院病理学教研室
肾小球硬化是多种肾脏疾病末期的最终结局,导致肾功能衰竭,对机体造成极大危害。在此病理改变过程中,肾小球系膜细胞的表型转化发挥着重要作用。自1982年提出脂质代谢异常的肾毒性学说后[1],近年来有关低密度脂蛋白(LDL)与肾脏纤维化的关系成为肾脏病学研究中的热点,但多集中于肾小管上皮细胞与肾间质的关系[2],而对其能否促进体外培养的系膜细胞(MCs)发生表型转化则缺乏研究。本实验采用LDL作用于体外培养的MCs,于细胞水平观察其能否诱导MCs发生表型转化及其对细胞生长和功能的影响。
1 材料与方法 1.1 材料胎牛血清(杭州四季青生物公司);胰蛋白酶(西安华美生物公司);小鼠抗大鼠-平滑肌肌动蛋白(-SMA)单克隆抗体,兔抗大鼠结缔组织生长因子(CTGF)单克隆抗体,链酶亲和素-生物素-过氧化物酶复合物(SABC)试剂盒及蛋白印迹(Western blot)检测试剂盒(武汉博士德生物公司);LDL(中国医学科学院基础医学研究所生化室);RPMI1640培养液(美国GIBCO公司)。
1.2 实验方法 1.2.1 细胞培养大鼠肾小球MCs引自中山大学医学院,经鉴定后用于本实验。实验中肾小球MCs细胞株以含10%胎牛血清(10%FCS)的RPMI 1640培养液,置37℃,5% CO2饱和孵箱内培养。每2~3 d换液和传代。当细胞长至贴壁80%~90%且台盼蓝染色活细胞达95%以上时,将含10%FCS的RPMI 1640培养液完全吸出,换成由不含胎牛血清的RPMI 1640培养液配制的不同浓度的LDL(0,25,50,100,150 g/ml),继续在孵箱内培养,中间换液及传代时继续按上述条件刺激。
1.2.2 细胞毒性实验取消化后的MCs以每孔5×105个/ml接种于12孔培养板,24 h后细胞接近于铺满孔底时换无血清RPMI 1640培养液培养24 h,使多数细胞同步于静止期后分为5组:(1)正常对照组(A组);(2)25 g/ml LDL组(B组);(3)50 g/mlLDL组(C组);(4)100 g/mlLDL组(D组);(5)150 g/ml LDL组(E组);于培养后24,36和48 h收集细胞,台盼蓝染色,进行活细胞计数。
1.2.3 细胞增殖水平测定实验步骤同上,细胞同步后分为5组,接种于96孔培养板,于孵箱中培养24,48和72 h后,加入四甲基偶氮噻唑蓝(MTT) 10 l/孔,37℃继续培养4 h,终止培养,吸弃孔内上清液,加入二甲基亚砜(DMSO)90 l/孔,振荡10 min,充分溶解结晶物,于酶联免疫检测仪上选择490 nm波长,测定各孔吸光度(A)值。
1.2.4 细胞形态学观察倒置相差显微镜观察细胞表型转化过程中的形态变化,透射电镜观察其超微结构改变。
1.2.5 免疫细胞化学染色将盖玻片预先置于6孔培养板内,然后将MCs以5×105个/ml接种于6孔板内,以含10%FCS的RPMI 1640培养液培养24 h,换无血清培养液使多数细胞同步后,将其进行同上分组,培养7 d后,行SABC法免疫细胞化学染色。以已知阳性结果为阳性对照,以磷酸盐缓冲液(PBS)代替一抗为阴性对照。结果以胞浆内出现棕黄色颗粒为阳性信号,阴性为无着色。高倍镜下(×400倍)观察200个细胞,计数-SMA染色阳性的细胞数。
1.2.6 Western blot测定-SMA、CTGF蛋白表达收集经不同浓度LDL刺激的生长状态良好、培养7 d的MCs,加细胞裂解液后离心,取上清,测定蛋白浓度。加上样液于10%十二烷基硫酸钠-聚丙烯酰胺凝胶进行电泳分离,电转移至硝酸纤维素膜上,5%脱脂奶粉封闭,加小鼠/兔抗大鼠-SMA或CTGF一抗孵育,4℃过夜,加辣根过氧化物酶标记的抗小鼠/兔IgG孵育,37℃ 1 h,二氨基联苯胺(DAB)显色。结果采用图形分析软件Quantity One(美国BioBod公司)对Western blot特异性条带进行灰度扫描,以积分吸光度×面积(mm2)代表特异性条带的信号强弱,以此对目的蛋白水平进行半定量比较。
1.3 统计分析应用SPSS 10.0软件进行分析,多个样本均数的比较采用单因素方差分析、直线相关分析。
2 结 果 2.1 LDL对MCs活细胞生长的影响台盼蓝染色结果显示,各浓度LDL作用24,36和48 h后,活细胞计数均在95%以上,说明该实验中各浓度LDL对MCs增殖、表型转化和ECM产量的影响,均为对95%以上的活MCs产生作用。实验证明,25~150 g/ml LDL对MCs无毒性作用。
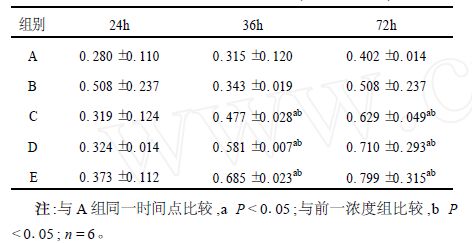
2.2 LDL对MCs增殖的影响(表 1)各浓度LDL均能促进MCs增殖,但25 g/ml LDL与MCs共孵育后与正常对照组比较,MCs增殖差异无统计学意义(P>0.05)。随着LDL浓度增加和刺激时间的延长,其增殖程度明显增强,差异有统计学意义(P<0.05),呈时间和浓度依赖性。
| 表 1 LDL对MCs增殖的影响( A 值, x ±s) |
2.3 MCs形态学观察
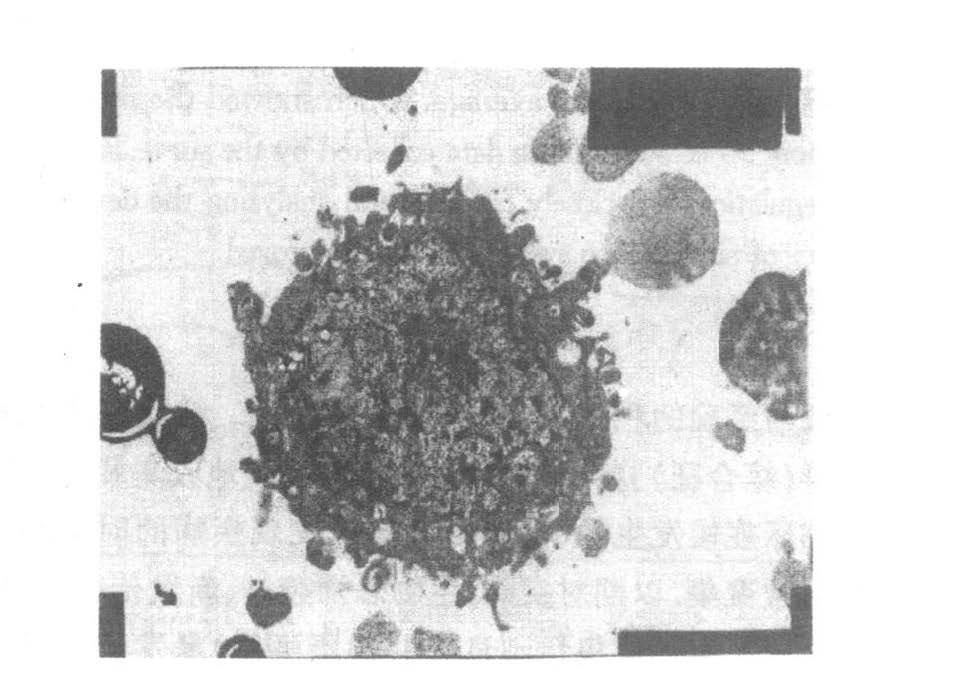
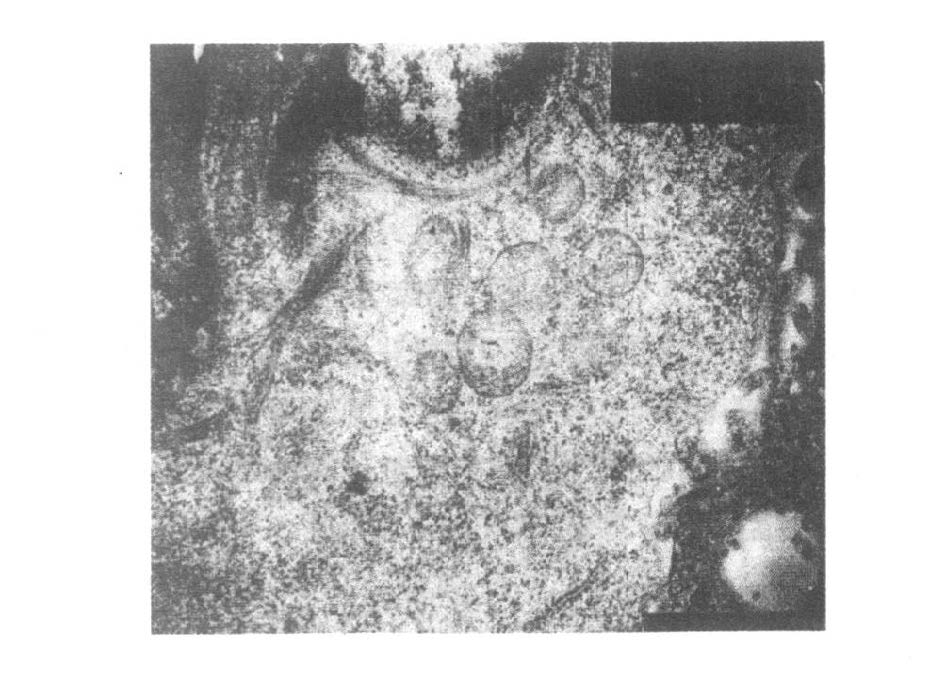
倒置相差显微镜下,正常MCs呈紧密单层融合的卵石样或铺路石样贴壁生长,透射电镜下细胞表面微绒毛密集(图 1),长而细,细胞内未见肌动蛋白中间丝结构。经LDL刺激7 d后,MCs呈典型的肌成纤维细胞形态学改变:细胞呈两端突起的长梭形,体积增大。透射电镜下,细胞表面微绒毛变短变粗融合,数量减少,粗面内质网明显增加,部分细胞内出现沿细胞轴分布的呈束状排列的肌动蛋白样结构(图 2),显示这种已转分化成功的MCs呈典型的肌成纤维细胞形态学特征。
|
图 1 透射电镜下细胞表面微绒毛( ×6000) |
|
图 2 细胞内肌动蛋白样结构( ×15000) |
2.4 LDL作用下MCs表型转化(表 2) 表 2 LDL对MCs表达-SMA的影响(略)注:与A组比较,a P<0.05。
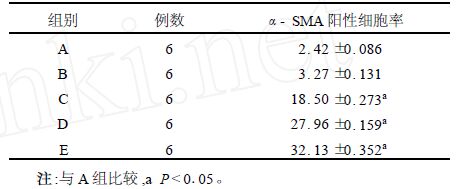
(1)免疫细胞化学染色 经LDL刺激7 d后,MCs肌性标记物-SMA呈现不同程度的阳性染色结果,-SMA阳性表达率与LDL浓度有关(r=0.82,P<0.05)。正常对照组未见-SMA明显表达。(2)Western blot正常MCs未见-SMA明显表达,经不同浓度LDL刺激7 d后,-SMA表达明显增强,且具有浓度依赖性。
| 表 2 LDL 对MCs 表达α- SMA的影响(α- SMA+ %, x ±s) |
2.5 LDL作用下CTGF蛋白表达
免疫细胞化学染色及Western blot结果显示,正常MCs未见CTGF蛋白表达,经LDL刺激7 d后,其蛋白表达增加,以100 g/ml LDL为最强,表达的最高峰为刺激后3 d。
3 讨 论目前,众多学者认为高脂血症是肾小球硬化的独立危险因素[3],而高脂血症条件下LDL能否促进MCs发生表型转化及其能否促进肾脏硬化尚缺乏相关的实验研究。
本实验结果表明,实验所采用的各浓度LDL对MCs均无细胞毒性作用,并能使MCs大量增殖。透射电镜发现经LDL诱导的MCs的超微结构发生明显变化并表达-SMA,免疫细胞化学染色及Western blot结果亦与上述发现一致,表明LDL在50~150 g/ml范围内与许多其他细胞因子一样可活化基质产生细胞并起调控作用[4],诱导MCs发生表型转化。
免疫细胞化学染色及Western blot结果显示,LDL在诱导MCs分化为肌纤维母细胞的同时,伴有CTGF蛋白表达增加。TGF-β是目前已明确的最强的前纤维化因子[5]。它能破坏ECM代谢的动态平衡,促进纤维化的发展[6],而CTGF是近年新发现的与肾脏纤维化密切相关的一个生长因子,是TGF-β的下游效应介质及TGF-β致前纤维化的标志[7]。实验中CTGF表达增加,与文献[7]研究结果一致,表明CTGF是致肾脏纤维化的关键因子之一。研究结果显示,在肾间质纤维化中表达的CTGF与TGF-β的细胞来源不完全相同[8],它只发挥TGF-β双向作用中的负面效应。目前,对CTGF的了解尚少[9]。已知TGF-β是诱导肾小管上皮细胞发生表型转化的中心环节[10],而作为TGF-β下游介质的CTGF在本实验中的表达明显增多,其与肾小球MCs的表型转化有无相关性,CTGF自身在实验中是否发挥了中介或放大作用,LDL能否在转录水平促进系膜细胞表达CTGF,还有待进一步研究。
实验结果表明,由于脂质代谢紊乱,LDL异常升高可以诱导MCs发生表型转化。这种转分化的MCs与肾小球纤维化的发生发展有着密切的关系。因此,若能阻断MCs发生表型转化及其可能存在的中间介导作用,从而抑制CTGF等细胞因子的产生,可能对治疗肾脏纤维化有重要意义。
| [1] | Moorhead J F, Chan MK, El-Nahas M, et al. Lipid nephrotoxicity in chronic progressive glomerular and tubulointersticial disease[J]. Lancet, 1982, 2 : 1309–1311. |
| [2] | Chevalier RL. Pathogenesis of renal injury in obstructive uropathy[J]. CurrOpin Pediatr, 2006, 18(2) : 153–160. |
| [3] | 钟文旗, 蔡政维, 朱正庭, 等. 中西结合治疗肾病综合征型紫癜性肾炎54 例体会[J]. 疑难病杂志, 2005, 4(1) : 16–18. |
| [4] | Rook M, Lely AT, Kramer AB, et al. Individual differences in re2 nal ACE activity in healthy rats predict susceptibility to adriamycin-induced renal damage[J]. Nephrol Dial Transplant, 2005, 20(1) : 59–64. DOI:10.1093/ndt/gfh579 |
| [5] | Forino M, Torregrossa R, Ceo M, et al. TGF-beta1 induces ep2 ithelial-mesenchymal transition, but not myofibroblast transdif2 ferentiation of human kidney tubular epithelial cells in primary cul2 ture[J]. Int J Exp Patho, 2006, 87(3) : 197–208. DOI:10.1111/iep.2006.87.issue-3 |
| [6] | Mary HB, Jeffery BK. TGF-βand fibrosis[J]. J Microbes Infec2 tion, 1999, 1 : 1349–1365. DOI:10.1016/S1286-4579(99)00250-6 |
| [7] | Blom IE, Goldschmeding R, LeaskA. Gene regulation of connective tissue growth factor :new targets for antifibrotic therapy[J]. Ma2 trix Biol, 2002, 21(6) : 473. |
| [8] | 赵青, 陈楠, 王伟铭, 等. 结缔组织生长因子在肾间质纤维化中的表达及其意义[J]. 肾脏病与透析肾移植杂志, 2002, 11 : 21–26. |
| [9] | Wahab, Nadia Abde Mason, Roger M, et al. Connective tissue growth factor and renal diseases : some answers, more questions[J]. Current Opinion in Nephrology and Hypertension, 2004, 13(1) : 53. DOI:10.1097/00041552-200401000-00008 |
| [10] | Roberts AB, Tian F, Byfield SD, et al. Smad3 is key to TGF-beta mediated epithelial-to-mesenchymal transition,fibrosis, tumor suppression and metastasis[J]. Cytokine Growth Factor Rev, 2006, 17(1-2) : 19–27. DOI:10.1016/j.cytogfr.2005.09.008 |
 2007, Vol. 23
2007, Vol. 23