胰腺癌是人体常见的恶性肿瘤之一,近年来在全球范围内呈明显上升态势,其恶性程度高、转移早、早期诊断困难,预后极差,90%以上病例死于发病后1年,5年存活率仅为0.4%~3%[1]。早期转移是影响胰腺癌预后的主要因素之一。文献报道,新生血管的生成是肿瘤生长、侵袭及转移的重要因素,而环氧合酶-2(COX-2)是新近被证实具有促进肿瘤生长的调节物质[2]。因此,选择性阻断COX-2的活性,可能有利于胰腺癌的预防和治疗。本实验旨在通过观察COX-2选择性抑制剂瑞芝清对人胰腺癌PANC-1细胞COX-2和血管内皮生长因子(VEGF)表达的影响,探讨瑞芝清抑制肿瘤血管生成的机制,为开辟新的抗癌途径提供基础依据。
1 材料与方法 1.1 材料人胰腺癌细胞株PANC-1(中科院上海细胞所),常规培养于Dulbecco's Modifided Eagle's Medium(DMEM)培养基(含10%胎牛血清、100U/ml青霉素、100U/ml链霉素)中,在37℃、5%C02培养箱中贴壁培养,取对数生长期的PANC-1细胞用于实验。瑞芝清(美国Sigma公司);TRIzol、DMEM、二甲基亚砜(DMSO)(美国Invitrogen公司);胎牛血清(美国Gibco公司),COX-2和VEGF小鼠单克隆抗体(美国Santa Cruz公司);其他试剂均为市售分析纯。瑞芝清用DMSO溶解后配成400mmol/L的储备液,实验时用DMEM培养液稀释到所需浓度。
1.2 方法 1.2.1 免疫组化检测瑞芝清对COX-2和VEGF蛋白表达的影响将对数生长期的PANC-1细胞按每孔5×105个细胞接种于6孔板中,每培养孔放置直径12mm经多聚赖氨酸处理的无菌盖玻片,置37℃、5%CO2及饱和湿度条件下,待24h贴壁生长后换液,分别加入不同浓度瑞芝清,使其终浓度分别为50,100,200,400µmol/L。设未进行药物干预的细胞为对照组,每组平行5个样本。继续培养48h取出玻片,磷酸盐缓冲液(PBS)冲洗,4%甲醛固定5min,放置于37℃恒温箱2h后取出,进行免疫组化染色。采用Power VisionTM两步法,操作步骤按试剂说明书进行。COX-2、VEGF皆为胞质着色,胞浆出现棕色或棕褐色颗粒为阳性细胞,高倍镜观察10个视野,计算阳性细胞占所有细胞的比率。
1.2.2 RT-PCR检测瑞芝清对PANC-1细胞COX-2 mRNA表达的影响收取不同药物浓度处理48h后细胞,应用TRIzo1常规提取细胞总RNA,经紫外微量分光光度仪定量后,取3µg总RNA,随机引物法逆转录合成cDNA。以磷酸甘油醛脱氢酶(GAPDH)作为内对照,进行半定量聚合酶链反应(PCR)。COX-2上游引物:5'-TGAAACCCACTCCAAACACAG-3',下游引物:5'-TCATCAGGCACAGGAGGAAG-3';目的片段大小为232bp。GAPDH上游引物:5'-ATGCTGGCGCTGAGTACGTC-3',下游引物:5'-AGGCCATGCCAGTGAGCTTC-3';目的片段大小为431bp。PCR反应条件为:94℃4min预变性后,94℃1min,56℃1min,72℃1min,共32个循环,72℃延伸10min,4℃保存。6µ1 PCR扩增产物在1.5%琼脂糖凝胶中电泳,采用Kodak DNA analysis 2.0凝胶成像系统吸光度扫描分析。
1.2.3 RT-PCR检测瑞芝清对PANC-1细胞VEGFmRNA表达的影响收取不同药物浓度处理48h后细胞,应用TRIzol常规提取细胞总RNA,经紫外微量分光光度仪定量后,取3µg总RNA,随机引物法逆转录合成cDNA。以β-actin作为内对照,进行RT-PCR。VEGF引物序列上游:5'-AGGAGGGCAGAATCATCACG-3',下游:5'-TATGTGCTGGCCTFGGTGAG-3',目的片段大小为405bp。β-actin:上游5'-TCGTACCACTGGCATTGTGA-3',下游5'-TCCTGCTTGCTGATCCACAT-3',目的扩增产物预期长度为765bp。PCR反应条件为:94℃4min预变性后,94℃1min,55℃1min,72℃1min,共30个循环,72℃延伸10min,4℃保存。6µl PCR扩增产物在1.5%琼脂糖凝胶中电泳,采用Kodak DNA analysis 2.0凝胶成像系统吸光度扫描分析。
1.3 统计分析采用SPSS 11.0软件进行方差分析及q检验,不同参数之间进行Pearson相关分析。
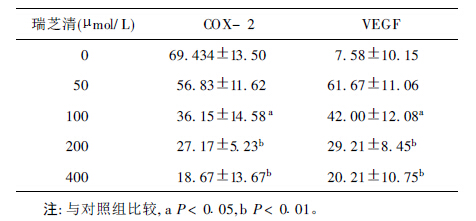
2 结 果 2.1 瑞芝清对COX-2和VEGF蛋白表达的影响(表 1)免疫组化结果显示,不同浓度瑞芝清处PANC-1细胞48h后,随着药物浓度的增大,COX-2和VEGF蛋白表达水平逐渐降低,且具有剂量依赖性,与对照组比较,差异有统计学意义(P<0.05);并且COX-2与VEGF之间具有良好的相关性(r=0.785,P<0.05)。
| 表 1 不同浓度瑞芝清对COX- 2 和VEGF 蛋白表达的影响( x±s, %) |
2.2 瑞芝清对PANC-1细胞COX-2 mRNA、VEGF mRNA表达的影响
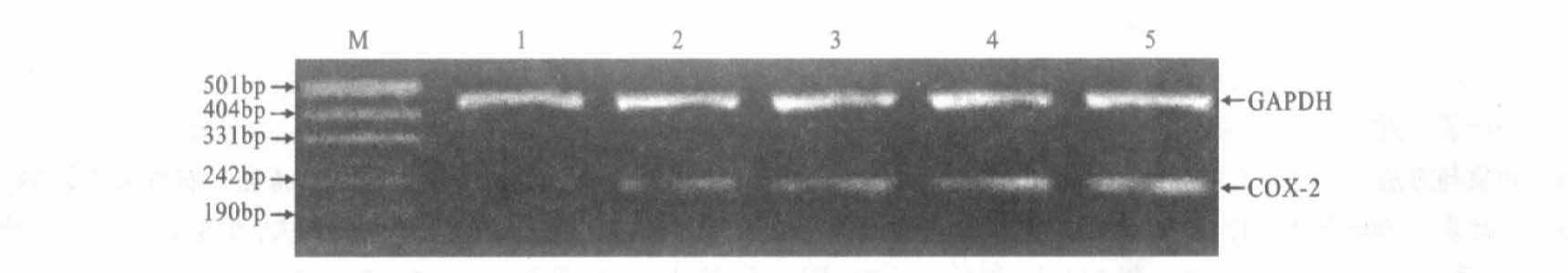
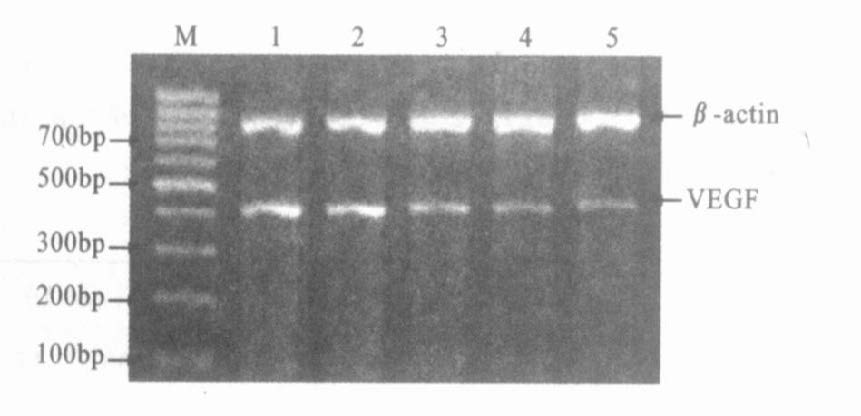
RT-PCR结果显示,不同浓度瑞芝清处理PANC-1细胞48h后,随着药物浓度的增加,COX-2 mRNA和VEGFmRNA表达水平逐渐下降,且呈现剂量依赖性(图 1,图 2)。
|
M: Maker;1: 400µLmol/ L; 2: 200µLmol/ L; 3: 100µLmol/ L; 4: 50µLmol/ L; 5: 对照组 图 1 不同浓度瑞芝清对PANC- 1 细胞COX- 2 mRNA 表达影响 |
|
M: Maker; 1: 对照组; 2: 50µLmol/ L; 3: 100µLmol/ L; 4: 200µLmol/ L; 5: 400µLmol/L 。 图 2 不同浓度瑞芝清对PANC- 1 细胞VEGF mRNA 表达影响 |
3 讨 论
环氧合酶(Cyclooxygenase,COX)存在COX-1和COX-2两种异构体,COX-1呈构成性表达,是维持机体正常生理功能的看家基因,在胃肠道的保护、维持正常的肾功能及凝血功能等方面起重要作用;COX-2是前列腺素(prostaglandin,P G)生物合成过程中的一个重要限速酶,可被缺氧、炎症、细胞因子、生长因子、有丝分裂原及肿瘤促进因子等多种因素诱导产生,是非甾体类抗炎药(NSAIDs)作用的靶基因[3]。COX-2不仅是抗炎作用的中心环节,而且在多种肿瘤组织中表达上调,在肿瘤的发生和发展中起着重要作用[4]。肿瘤的浸润转移与COX-2、VEGF的高表达有关[5]。VEGF是一高特异性血管内皮细胞有丝分裂原,是肿瘤新生血管生成的重要调控因子,不仅参与肿瘤血管生成、增殖,还直接与肿瘤浸润、转移有关。有关研究亦证实,VEGF是迄今所发现最强、最特异的促血管生成因子之一,在肿瘤新生血管形成过程中起关键作用[6]。COX-2是新近被证实具有促进肿瘤生长的调节物质,且其表达的程度与肿瘤的病程密切相关。Tsujii等[7]体外实验发现,COX-2可能通过调节血管生成因子而促进结肠癌新生血管生成。Liu等[8]体内研究揭示,选择性COX-2抑制剂NS-398能显著抑制前列腺癌新生血管的生成。
文献报道[9],血管生成剂TNP-470单独或联合应用抗代谢剂顺铂可显著抑制小鼠胰腺癌肝脏转移,提示抑制血管生成对胰腺癌生长与转移可能具有一定的干预作用。本研究发现,不同浓度瑞芝清作用于胰腺癌PANC-1细胞48h后,COX-2和VEGF蛋白表达率与对照组比较明显降低(P<0.05),并且COX-2与VEGF之间具有良好的相关性(r=0.785,P<0.05)。RT-PCR结果也显示,随着药物浓度的增大,COX-2mRNA和VEGFmRNA表达逐渐减弱。由此可见,在胰腺癌中COX-2促进新生血管生成的机制可能与其上调VEGF等因子有关。提示抑制COX-2的表达及由此引起的VEGF表达降低,在非甾体类抗炎药抑制肿瘤血管生成机制中可能具有一定作用。
| [1] | Safiol eas MC, Moulakakis KG. Pan creat ic cancer today[J]. Hepat ogastro Enterology, 2004, 51(57) : 862–868. |
| [2] | 王兴鹏, 徐选福, 谢传高, 等. 环氧合酶- 2 对胰腺癌新生血管生 成的调节作用及其机制[J]. 中华肝胆外科杂志, 2002, 8(9) : 552–556. |
| [3] | Henschman HR. Prostaglandin synthease 2[J]. Biochim Biophys Acta, 1996, 1299 : 125–140. DOI:10.1016/0005-2760(95)00194-8 |
| [4] | Leng J, Han C, Demet ris AJ, et al. Cyclooxygenase- 2 promot es hepatocellular carcinoma cell grow th through akt activat ion: ev-i dence for akt inhibit ion in celecoxib - induced apoptosis[J]. Hepatoloy, 2003, 38(3) : 756–764. DOI:10.1053/jhep.2003.50380 |
| [5] | 刘莹, 朱祖安, 费素娟. COX- 2、iNOS 及VEGF 在胃不典型增 生胃癌中的表达及意义[J]. 中国肿瘤临床, 2005, 32(8) : 428–430. |
| [6] | Chao Y, Li CP, Chau GY, et al. Prognostic signif icance of vascular endothelial grow th f act or, basic f ibroblast grow th factor, and angiogenin in pat ients with respectable hepatocellular carcinoma aft er surgery[J]. Ann Surg Oncol, 2003, 10(4) : 355–362. DOI:10.1245/ASO.2003.10.002 |
| [7] | T sujii M, Kaw ano S, T suji S, et al. Cyclooxygenase regulat es angiogenesis induced by colon cancer cell[J]. Cell, 1998, 93 : 705–716. DOI:10.1016/S0092-8674(00)81433-6 |
| [8] | Liu XH, Kischenbaum A, Yao S, et al. Inh ibit ion of cyclooxygenas e - 2 suppresses angiogenesis and the grow th of prostat e cancer in v i v o[J]. J U rol, 2000, 164 : 820–825. |
| [9] | Kaw arada Y, Ishikura H, Kishimoto T, et al. Inhibitory ef fects of the angiogenic agent TNP - 470on est alishment and grow th of hematogenous metast asis of human pancreat ic carcinoma in SC ID beige mice in v iv o[J]. Pancreas, 1997, 15 : 251–257. DOI:10.1097/00006676-199710000-00006 |
 2007, Vol. 23
2007, Vol. 23