精子的发生是一个复杂的生理过程。睾丸组织内局部环境的恒定,对保障精子发生的正常进行十分重要。局部环境的恒定有赖于睾丸组织中某些生化成分的维持。以往研究发现,其他因素引起的精子发生异常,往往伴随着睾丸组织中某些生化成分的异常〔1, 2〕。高原低氧对精子发生有抑制作用〔3, 4〕。为了解高原低氧对精子发生的抑制是否与睾丸组织局部微环境的代谢改变有关,我们通过观测低氧对睾丸组织内乳酸脱氢酶同工酶C4/乳酸脱氢酶(LDH-C4/LDH)、γ-谷氨酰胺转移酶(GGT)活性和果糖、丙二醛(MDA)含量的影响,来了解低氧对精子发生局部环境的影响。
1 材料与方法 1.1 材料 1.1.1 实验动物选用180~220 g Wistar大鼠(本校附属第三医院动物所)。将30只大鼠随机分为常氧组(n=8)、低氧5 d组(n=8)、低氧15 d组(n=6)和低氧30 d组(n=8)。低氧的3个组置低压舱中喂养,每天开舱40 min打扫卫生、更换食物。常氧组置低压舱外喂养。各组每天光照12 h。
1.1.2 主要试剂丙酮酸、十二烷基磺酸钠(SDS,上海生工公司);2-酮基己酸、还原型烟酰胺腺瞟呤二核苷酸(NADH)(美国Sigma-Aldrich公司);D-果糖、间苯二酚、硫代巴比妥酸、双甘氨酸(上海化学试剂公司);γ-glutamyl-p-nitromilide(上海生物化学研究所)。
1.2 方法 1.2.1 睾丸组织匀浆液的提取大鼠活杀后,取右侧睾丸,按1:10(W/V)比例加入0.1 mol/L磷酸缓冲液(pH 7.4),用玻璃匀浆器匀浆。4 ℃ 8 000 r/min离心10 min,取上清备用。
1.2.2 睾丸组织LDH-C4/LDH测定〔5〕(1) LDH总活性测定1.0 mmol/L丙酮酸0.5 ml,加入0.23 mmol/L NADH 0.5 ml溶液,在37 ℃孵浴5 min,加入15倍稀释(预实验确定)的睾丸组织匀浆液20 μl,在340 nm下记录3 min吸光度的变化值。(2) LDH-C4活性测定10.0 mmol/L2-酮基己酸0.5 ml和0.23 mmol/L NADH溶液0.5 ml,在37 ℃水浴5 min,加入5倍稀释(预实验确定)的睾丸组织匀浆液20 μl,在340 nm下记录3 min吸光度的变化值。③计算LDH-C4与LDH的比值比值=LDH-C4引起的吸光度变化值/LDH总活性吸光度的变化值。
1.2.3 睾丸组织γ-谷氨酰胺转移酶活性测定〔6〕取睾丸组织匀浆液100 μl,加入0.5 ml GGT反应底物(0.107 g γ-glutamyl-p-nitromilide,0.539 g双胱氨酸,0.224 g MgCl2·6H2O溶于100 ml 185 mmol/L pH 8.25 Tris-HCl中)。37 ℃孵育10 min,加入0.5 ml 25%(W/V)三氯乙酸。室温4 000 r/min离心10 min,上清在405 nm下比色。以每分钟转化1 μmol底物的酶量为一个单位。用Follin-酚法定量睾丸组织匀浆液中总蛋白质,酶活性以U/mg睾丸匀浆液总蛋白表示。
1.2.4 睾丸果糖含量测定采用倍比稀释法制备标准品浓度梯度,320, 160, 80, 40, 20和10 μmol/L果糖标准品(2 g/L安息香酸配制)。各取样本、标准品、纯水1.0 ml,加入1 g/L间苯二酚溶液1.0 ml和10 mol/L盐酸溶液3.0 ml。90 ℃水浴10 min。505 nm波长下比色。结果以μmol/mg睾丸匀浆液总蛋白表示。
1.2.5 低氧对大鼠睾丸丙二醛含量的影响〔7〕取100 μl睾丸匀浆液,加入10%SDS 0.5 ml,沉淀蛋白20 min;加入0.1 mol/L HCl 1.25 ml,1%硫代巴比妥酸0.5 ml;100 ℃沸水中煮40 min。流水冷却;加入1.75 ml正丁醇,振荡3~5 min;静置10 min,4000 r/min离心10 min;取上清,在535 nm下比色。结果以nmol/mg睾丸匀浆液总蛋白表示。
1.3 统计分析组间比较采用SPSS 10.0统计软件的One-way ANOVA程序进行单因素方差分析。
2 结果 2.1 低氧对大鼠睾丸组织LDH-C4/LDH的影响(图 1)
|
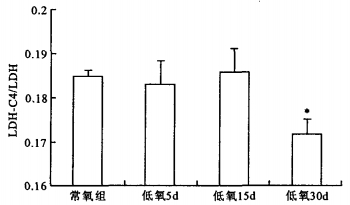
注:与常氧对照组比较, * P < 0.05 图 1 低氧对大鼠睾丸LD H-C4/ LD H的影响 |
低氧30 d组大鼠睾丸组织LDH-C4/LDH显著低于常氧对照组(P < 0.05)。低氧5 d组和低氧15 d组睾丸组织LDH-C4/LDH,与常氧组相比较差异无统计学意义(P > 0.05)。
2.2 低氧对大鼠睾丸组织GGT活性的影响(图 2)
|
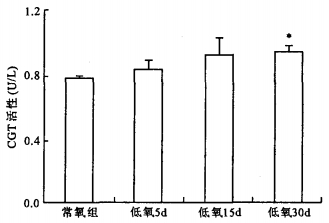
注:与常氧对照组比较, * P < 0.05 图 2 低氧对大鼠睾丸GGT活性的影响 |
低氧5 d组、15 d组大鼠睾丸组织GGT活性,与常氧对照组比较差异无统计学意义(P > 0.05)。低氧30 d组GGT活性升高,与常氧对照组比较差异有统计学意义(P < 0.05)。
2.3 低氧对大鼠睾丸组织果糖含量的影响(图 3)
|
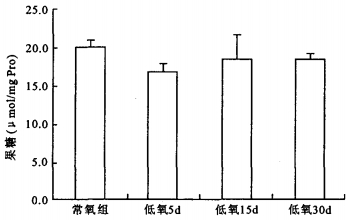
注:与常氧对照组比较, * P < 0.05 图 3 低氧对大鼠睾丸GGT活性的影响 |
低氧各组睾丸组织果糖含量,与常氧对照组相比差异无统计学意义(P > 0.05)。
2.4 低氧对睾丸组织丙二醛生成的影响(图 4)
|
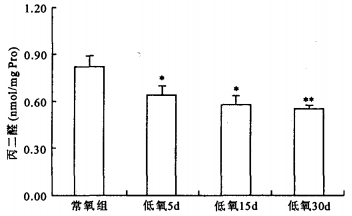
注:与常氧对照组比较, * P < 0.05, ** P < 0.01 图 4 低氧对大鼠睾丸组织丙二醛的影响 |
低氧5 d组、15 d组大鼠睾丸组织中丙二醛含量显著低于常氧对照组(P < 0.05)。低氧30 d组大鼠睾丸组织丙二醛含量非常显著地低于常氧对照组(P < 0.01)。
3 讨论LDH-C4是睾丸组织和精子细胞的一种特异酶,与睾丸生精功能有关,也是精子能量代谢的一个关键酶〔8〕。文献报道多种生殖毒性物质均可引起LDH-C4相对活性降低〔9, 10〕。LDH-C4抗血清对大鼠有生殖抑制作用〔4〕。低氧30 d该酶的相对活性显著下降, 提示慢性低氧对睾丸生精有抑制作用。
GGT对抗氧化剂谷胱甘肽(GSH)的生成很重要。研究发现抗生精复合物CDRI-84/35〔11〕和硫酸镍〔12〕能引起大鼠、小鼠睾丸GGT活性升高。GGT活性升高的机制不清。本研究中低氧30 d组GGT活性显著升高的机制可能与此类似。
自由基增多是男性不育的重要因素。本实验发现,低氧能抑制睾丸组织产生自由基。这可能与低氧时睾丸组织氧供减少有关。低氧时MDA降低,GGT活性不变或增高,说明低氧时睾丸生精功能的抑制作用与自由基的毒性作用无关。低氧是否抑制了活性氧自由基(ROS)介导的信号传导通路,由此抑制了精子的发生需要进一步研究。
低氧时,果糖可通过磷酸化进入糖酵解途径。但本研究发现,低氧各组睾丸组织中果糖含量并无显著变化。这可能是由于催化果糖酵解的限速酶己糖激酶在精子细胞中的活性显著低于其他糖酵解酶的活性。并且这些细胞的糖酵解主要是通过葡萄糖转化为乳酸盐,而不是转化为6-磷酸葡萄糖来完成〔13〕。
| [1] | 徐莉春, 王沭沂, 王心如. 镉对大鼠睾丸毒作用的酶学研究[J]. 中国公共卫生, 2000, 16(2) : 119–120. |
| [2] | 徐宏伟, 马爱国. 维生素A缺乏对大鼠生精能力及睾丸标志酶活性的影响[J]. 中国公共卫生, 2002, 18(11) : 1298–1299. |
| [3] | 史小均, 杜继增, 熊忠. 缺氧对雄性大鼠性腺的影响[J]. 中国病理生理杂志, 1998, 14(2) : 137–140. |
| [4] | Fahim MS, Messiha FS, Girgis SM. Effect of acute and chronic simulated high altitude on male reproduction and testosterone level[J]. Arch Androl, 1980, 4(3) : 217–219. DOI:10.3109/01485018008986966 |
| [5] | 丛玉隆, 马骏龙, 秦晓玲. 当代体液分析技术与临床[M]. 北京: 中国科学技术出版社, 1999: 138-139. |
| [6] | Roomi MW, Goldberg DM. Comparison of gamma-glutamyl transferase induction by phenobarbital in the rat, guinea pig and rabbit[J]. Biochem Pharmacol, 1981, 30(12) : 1563–1571. DOI:10.1016/0006-2952(81)90382-8 |
| [7] | 黄虹. 血清脂质过氧化代谢产物丙二醛测定方法的改进[J]. 镇江医学院学报, 1999, 9(3) : 457–458. |
| [8] | 李明. 精子乳酸脱氢酶同工酶的研究进展[J]. 临床检验杂志, 2001, 19(6) : 375–378. |
| [9] | Xiao G, Pan C, Cai Y, et al. Effect of benzene, toluene, xylene on the semen quality and the function of accessory gonad exposed workers[J]. Ind Health, 2001, 39(2) : 206–210. DOI:10.2486/indhealth.39.206 |
| [10] | 陈龙, 任文华, 朱善良, 等. 慢性镉负荷雄性大鼠的睾丸及生殖内分泌功能活动[J]. 生理学报, 2002, 54(3) : 258–262. |
| [11] | Gupta G, Naikhuri JP, Dwivedi AK, et al. Effect of antispermatogenic compound CDRI-84/35 on marker enzymes of rat testis cells[J]. A Study on Site of Action Contraception, 1997, 56(6) : 395–400. |
| [12] | Pandey R, Kumar R, Singh SP, et al. Male reproductive effect of nickel sulphate in mice[J]. Biometals, 1999, 12(4) : 339–346. DOI:10.1023/A:1009291816033 |
| [13] | Nakamura M, Fujiwara A, Yasumasu F, et al. Regulation of glucose metabolism by adenine nucleotides in round spermatids from rat testes[J]. J Biol Chem, 1982, 257(23) : 13945–13950. |
 2007, Vol. 23
2007, Vol. 23

 , 蔡明春, 蒋春华, 吴艺, 陈建
, 蔡明春, 蒋春华, 吴艺, 陈建