2. 广东医学院预防医学教研室;
3. 中国疾病顶防控制中心性病艾滋病预防与控制中心病毒免疫室;
4. 广西壮族自治区疾病预防控制中心;
5. 广西横县卫生防疫站
人类免疫缺陷病毒-1 (HIV -1)高度变异, 不同亚型毒株其生物学特性及; 分子流行病学特征均有所不同〔1〕, 若能快速、准确地对HIV进行基因分型不仅有助于了解HIV -1转播规律, 而且可为阐明HIV基因型与生物表型关系、药物耐药性等研究提供资料。近年来, 我国学者〔2〕建立了一种多重巢式PCR法对我国HIV -1主要流行株进行鉴定亚型。然而, 由于HIV -1的基因变异度极高, 在传播过程中可产生许多具有相对独立的基因序列型别, 使得不同地区各亚型间具有其自身的特异性。广西壮族自治区为国内HIV感染的高发区, 大部分感染发生在经济尚不发达地区的人群中。因此, 建立广西HIV -1主要流行株快速基因分型方法十分必要。目前, 广西的优势流行株为CRF01 -AE和CRF08 -BC重组毒株〔3, 4〕。为此, 本研究针对这2种重组毒株gag基因区建立了一种亚型特异性引物PCR法的快速基因分型法。
1 材料与方法 1.1 样本来源从广西HIV -I主要流行区采集54份样本, 经ELISA初筛和免疫蛋白印迹(WB)确认为HIV阳性样本。
1.2 核酸提取采用QIAamp Bloodes Mini Kit试剂盒(德国QiaGen公司)从每位感染者的抗凝全血中提取细胞DNA, 并冻存于-80 ℃冰柜备用。
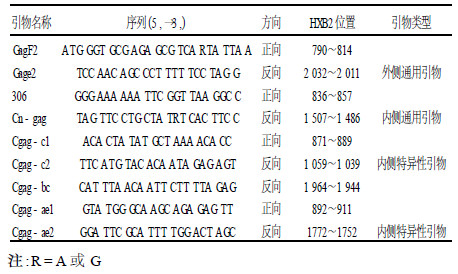
1.3 HIV -1亚型特异性引物的设计亚型特异性引物的设计是整个方法建立的关键。设计的基本原则:设计的引物位点必须在各个亚型间高度特异, 而在同一种亚型内部高度保守。在Primer5.0软件的帮助下设计出gag区的亚型特异性引物(表 1)。
| 表 1 gag区PCR扩增使用的引物 |
1.4 HIV -1 gag基因区的扩增
用nested -PCR对HIV -1gag基因区进行扩增, 第1轮使用引物GagF2/ Gage2, 模板15μl, 反应条件: 94 ℃ 5 min, 52 ℃ 1 min, 72 ℃ 2 min 30 s, 1个循环; 94 ℃ 30 s, 52 ℃ 30 s, 72 ℃ 1 min 30 s, 30个循环; 72 ℃ 10 min。第2轮模板5μl, 使用分别检测C亚型和CRF01 -AE重组型的2套亚型特异性引物(Cag -c1/ Cag -c2, Cag -ae1/ Cag -ae2), 争套引物放入同一反应管中, 为减少非特异性反应, 使用热启动和降落PCR (TD -PCR)技术〔5〕, 94 ℃ 5 min, 52 ℃ 1 min, 72 ℃ 2 min 30 s, 1个循环; 94 ℃30 s, 52 ℃30 s, 72 ℃1 min, 3个循环; 94 ℃30 s, 51 ℃ 30 s, 72 ℃ 1 min, 3个循环; 94 ℃ 30 s, 50 ℃ 30 s, 72 ℃ 1 min, 3个循环; 94 ℃30 s, 49 ℃30 s, 72 ℃1 min, 3个循环; 94 ℃30 s, 48 ℃ 30 s, 72 ℃ 1 min, 25个循环, 72 ℃ 10 min。如果特异性引物PCR扩增出的目的条带判断为C亚型, 则用专门用于检测B’/ C重组毒株(包括CRF07 -BC和CRF08 -BC)的亚型特异性引物Cgag -c1/ Cgag -bc为内侧引物再进行PCR扩增, 以判断是否为重组形式。反应条件: 94 ℃ 2 min, 48 ℃ 1 min, 72 ℃ 2 min, 1个循环; 94 ℃ 30 s, 48 ℃ 30 s, 72 ℃ 1 min, 35个循环; 72 ℃ 10 min。同时使用引物306/ Cn -gag扩增所有样本并进行基因测序, 用于系统树分析及亚型鉴定以验证特异性引物分型结果是否正确。反应条件:94 ℃ 2 min, 50 ℃ 50 s, 72 ℃ 1 min, 1个循环; 94 ℃ 30 s, 50 ℃ 30 s, 72 ℃ 1 min, 35个循环; 72 ℃ 10 min。第1轮和第2轮PCR反应体系均为50μl, dNT/P浓度为200μmol/ L, Taq酶为2.5 U, 引物浓度为0.4μmol/ L, MgCl2浓度为1.5 mmol/ L。
1.5 PCR产物检测取5μl第2轮PCR扩增产物在2%琼脂糖凝胶中电泳, 溴化乙锭(EB)染色检测, 紫外摄影拍照, 根据Markers分子量大小来判定结果。C亚型片段190 bp; CRF01 -AE片段881 bp; B’/ C片段1 079 bp。
1.6 序列测定对于全部经引物306/ Cn -gag扩增的样本, 经切胶, 纯化后, 以306为测序引物, 提纯的PCR产物为模板, 采用DNA测序试剂盒(美国ABI公司), 在PTC-220型多通道PCR仪(美国MJ公司)上进行测序反应。反应产物经提纯后, 采用310型全自动毛细管DNA测序仪(美国ABI公司)进行序列测定和分析。
1.7 序列分析(美国Los Alamos国家实验室HIV核酸序列库中提供)基因分型工具BLAST程序进行基因型鉴定; 用Clustal X进行排序和MEGA version 2.1软件进行分析。亚型分析使用的各个亚型参考序列来自美国Los Alamos HIV基因数据库。
1.8 检测该方法的重复性在CRF01 -AE样本中随机选取12份, CRF08 -BC 4份, 共16份样本使用上述方法重复5次。
2 结果 2.1 样本基因测序和系统树分析54份阳性样本中通过引物306/ Cn -gag扩增最终获得50份样本的基因序列, 经BLAST程序鉴定出4份样本gxmu0402, gxmu0416、gx2 mu0418和gxmu0419为CRF08 -BC重组毒株, 余下46份为CRF01 -AE重组毒株。将50份基因序列与国际各亚型标准株的基因序列进行系统树分析显示。4份CRF08 -BC样本与CRF08 -BC198CN006和CRF08 -BC197CNGX7f靠得很近, 而46份CRF01 -AE中, 有44份与CRF01 -AE197CNGX2f聚成一簇, 另外2份样本gxmu0432和gx2 mu0439与CRF01 -AE193J PNH 1和CRF01 -AE93TH057十分接近。
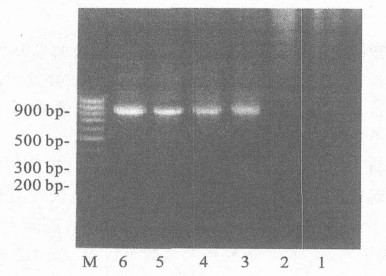
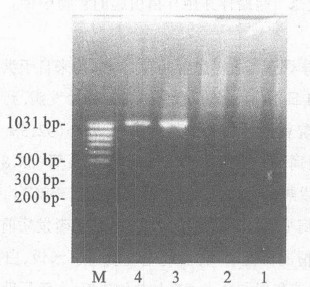
2.2 亚型特异性引物PCR扩增部分样本经亚型特异性引物PCR扩增后的电泳结果见图 1和图 2。根据不同亚型扩增出的目的带位点不同, 判断出亚型结果。54份样本中, 采用特异性引物共扩增出49份样本, 其中C亚型4份, CRF01 -AE重组毒株45份(97.83%, 45/ 46)。进一步使用B’/ C重组特异性引物扩增C亚型特异性引物鉴定出来的4份样本, 发现这4分样本均为B’/ C重组毒株(100%, 4/ 4)。以基因测序法为金标准, 可知亚型特异性引物PCR法的灵敏度为98%, 特异性为100%。
|
M:DNA 分子量;1 :H2O ;2 :阴性对照;3 :gxmu0433 ; 4 :gxmu0440 ;5 :gxmu0451 ;6 :gxmu0462 图 1 部分CRF01 -AE样本琼脂糖电泳结果 |
|
M:DNA 分子量;1 :H2O ;2 :阴性对照; 3 :gxmu0418 ;4 :gxmu0419 图 2 B’/ C样本琼脂糖电泳结果 |
2.3 亚型特异性引物PCR法的重复性
重复实验采用4份CRF08 -BC样本和12份CRF01 -AE随机样本进行5次重复。结果显示, CRF08 -BC重组毒株平均重复性为100% (20/ 20), 而CRF01 -AE在5次重复中有1次出现1份样本检测不出, 其平均重复性为98.3%(59/ 60)。
2.4 基因测序法与亚型特异性引物PCR法比较54份己确认的阳性样本, 基因测序法检测并正确分型的样本是50份, 检出率为92.60%, 特异性引物PCR法为49份, 检出率为90.74%。2种方法检测结果经差异性检验显示, χ2=0, P > 0.05, 差异无统计学意义, 结果一致性高达98.15%。
3 讨论本研究结果表明, 亚型特异性引物PCR方法对于亚型的鉴定结果与基因测序、系统树分析得到的结果是吻合的, 该方法的特异性达100%。用亚型特异性引物扩增样本时, 有时一会出现非特异性扩增条带, 干扰实验结果。非特异性条带位置一般不在特异性位置。为防止误判, 可以通过跑厚胶并且延长电泳时间, 使目的条带与非特异性条带充分分开。通常在紫外灯下, 非特异性条带要比目的条带弱。出现非特异性扩增条带通常有如下的原因: (1)引物与模板错配扩增产生, 引物与模板亚型相符, 不仅能在特异性位点上与模板结合, 亦能在远离特异性位点的地方与模板结合, 这种情况错配通常靠近引物5′端的位置, 电泳时会出现两条带; (2)引物之间形成的引物二聚体, 一般出现在80 bp左右的位置, 通过长时间电泳可使此条带消失; (3)某一亚型的特异性引物与另一亚型的模板错配扩增产生, 因2套引物放入同一反应管中, 所以可能出现此情况, 为了避免此情况发生, 因此, 在设计引物时使引物在3′端与别亚型的模板至少有2个碱基产生错配。
用本研究所建立起的方法对54份样本的gag基因区进行检测, 发现有些样本在1 200 bp左右的位置会出现一条非特异性扩增, 因第1轮PCR扩增的条带位置在1 242 bp, 因此怀疑此非特异性扩增条带为第1轮PCR扩增出的目的带, 将第1轮PCR产物与用亚型特异性引物扩增出的第2轮产物同时进行电泳, 证实了这一推测。为了减少此情况的发生, 可减少第1轮反应的模板量, 同时在加入反应体系、模板和酶后尽量减少室温放置时间或在冰盒上操作。
本实验结果表明, 亚型特异性引物PCR法, 灵敏度为98%, 特异性为100%, 结果显示, 其灵敏度和特异性均较好。重复性实验显示, B’/ C亚型的平均重复性为100%, CRF01 -AE重组毒株为98.3%, 说明一该方法在实际中是可行的。但由于CRF08 -BC样本例数不多, 因此, 本研究所建立起的方法对于HIV -1 B’/ C重组毒株分型的准确性有待扩大样本量进一步证实。
| [1] | 杰伊A, 利维. 艾滋病病毒与艾滋病的发病机制[J]. 2版.北京:科学出版社, 2000 : 126–132. |
| [2] | Wei M, Guang Q, Liang H, et al. Simple subtyping assay for human immunodeficiency virus type 1 subtypes B, C, CRF01-AE, CRF07-BC, and CRF08-BC[J]. J Clin Microbiol, 2004, 42 : 4261–4267. DOI:10.1128/JCM.42.9.4261-4267.2004 |
| [3] | Yang R, Kusagawa S, Zhang C, et al. Identification and characteri2 zation of a new class of human immunodeficiency virus type 1 re2 combinants comprised of two circulating recombinant forms, CRF07-BC and CRF08-BC, in China[J]. J Virol, 2003, 77 : 685–695. DOI:10.1128/JVI.77.1.685-695.2003 |
| [4] | Piyasirisilp S, McCutchan FE, Carr J K, et al. A recent outbreak of human immunodeficiency virus type 1 infection is Southern China was initiated by two highly homogeneous, geographically separated strains, circulating recombinant form AE and a novel BC recombi2 nant[J]. J Virol, 2000, 74 : 11286–11295. DOI:10.1128/JVI.74.23.11286-11295.2000 |
| [5] | 迪芬巴赫CW, 德维克斯勒GS著, 黄培堂, 俞炜源, 陈添弥, 等译. PCR技术实验指南[J].北京:科学出版社, 1998 :33-40. |
 2007, Vol. 23
2007, Vol. 23

 , 邵一鸣3, 张志勇1, 邢辉3, 刘伟4, 卢灿健5, 沈菁1
, 邵一鸣3, 张志勇1, 邢辉3, 刘伟4, 卢灿健5, 沈菁1